基於納米氧化銅測定尿素的方法與流程
2023-04-23 22:42:51 4
本發明涉及尿素在脲酶催化下水解產生氨,抑制納米氧化銅模擬鹼性過氧化物酶在鹼性條件下催化過氧化氫氧化對羥基苯丙酸形成螢光產物的活性,建立測定尿素的螢光分析方法,屬於分析化學和納米技術領域。
背景技術:
過氧化物酶主要存在於細胞的過氧化物酶體中,可催化過氧化氫氧化酚類和胺類化合物,繼而清除過氧化氫、酚類和胺類毒性的作用。天然過氧化物酶含量少,價格昂貴,容易受外界環境幹擾失去催化活性,納米人工模擬酶由於其結構穩定、經濟、易於大規模製備以及可調催化活性等優點,已被廣泛用於生物分析和生物技術應用。天然過氧化物酶及其模擬物通常在酸性或中性條件下發揮最佳性能。然而,在鹼性條件下進行的研究很少。因此,鹼性過氧化物酶模擬物的發現對於實際應用具有重要意義。
尿素是一種由碳、氧、氮及氫元素構成的有機小分子,是血液和其他體液的基本組成成分。尿素是胺基酸代謝的最終產物,在肝臟內合成,一般隨尿液排出體外。但是40%~50%在腎小球的髓質部被動的重吸收,當人體尿素的含量超過了自身的吸收能力之後,將會對人體的肝、腎、肺泡等造成危害。尿素在診斷腎臟和肝臟疾病中起重要作用。腎衰竭(急性或慢性)、尿道梗阻、脫水、休克、燒傷和胃腸道出血等疾病會引起尿素水平增加,肝衰竭,腎炎症候群、惡病質(低蛋白和高碳水化合物飲食)等嚴重疾病也會引起尿素水平降低。因此,尿素的檢測對於臨床診斷中具有重要意義。
本發明基於納米氧化銅作為模擬鹼性過氧化物酶催化過氧化氫氧化對羥基苯丙酸,結合脲酶催化尿素水解產生氨的反應,提供一種以納米氧化銅為催化劑測定尿素的螢光分析方法。
技術實現要素:
本發明的目的是基於納米氧化銅良好的模擬鹼性過氧化物酶活性,結合脲酶可以選擇性水解尿素生成氨和二氧化碳,再通過氨抑制納米氧化銅催化過氧化氫氧化對羥基苯丙酸的過程,減少二聚體螢光產物的生成,提供一種以納米氧化銅為催化劑測定尿素的螢光分析方法。
為了實現上述目的,本發明採用以下技術方案:所述一種以納米氧化銅為催化劑測定尿素的螢光分析方法,其特徵是首先將尿素、脲酶和磷酸鹽緩衝液三者混合在溫浴下進行脲酶酶促反應,然後向其中加入對羥基苯丙酸、過氧化氫、納米氧化銅溶液和磷酸鹽緩衝液繼續溫浴進行螢光反應,用螢光分光光度計測定上述螢光反應產物的螢光強度;所述的納米氧化銅由如下步驟製得:1)取0.02 mol/L的醋酸銅溶液150 ml和0.5 ml冰醋酸加入到裝有冷凝管的三頸瓶中,攪拌加熱至沸騰;2)快速加入0.04 g/ml的氫氧化鈉溶液10 ml,加完後繼續攪拌5分鐘,得到黑色氧化銅沉澱;3)將反應得到的黑色氧化銅沉澱離心,用無水乙醇洗滌三次,減壓乾燥,即得納米氧化銅粉體。
所述的一種以納米氧化銅為催化劑測定尿素的螢光分析方法,其特徵是螢光反應產物的最大激發波長和發射波長分別為320 nm和409 nm。
所述的一種以納米氧化銅為催化劑測定尿素的螢光分析方法,其特徵是脲酶酶促反應體系pH值為7.0,脲酶濃度為0.3 U/mL,反應溫度為37 ℃,反應時間為30分鐘。
螢光反應體系的pH值為10.25,氧化銅濃度為0.4 mg/L,對羥基苯丙酸濃度為4 mmol/L,反應溫度為65℃,反應時間為15分鐘。
所述的一種以納米氧化銅為催化劑測定尿素的螢光分析方法,其特徵是將150 µL用濃度為10mmol/L,pH為7.0的磷酸鹽緩衝液配製成的不同濃度的尿素溶液和50 µL濃度為6 U/mL的脲酶溶液混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2mg/L的納米氧化銅溶液和500 µL濃度為100mmol/L、pH為10.25的磷酸鹽緩衝溶液中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm,以螢光強度差值對尿素濃度對數值作圖得到標準曲線用於測定尿素。
所述的一種以納米氧化銅為催化劑測定尿素的螢光分析方法,其特徵是尿素檢測線性範圍為0.0375~0.3 mmol/L,檢測限為27 µmol/L。
本發明利用納米氧化銅為催化劑測定尿液尿素含量的螢光分析方法,其特徵是它由以下步驟組成:(1)在EP管中分別加入用磷酸鹽緩衝液稀釋後的尿液和脲酶混合溫浴;(2)向上述EP管中加入磷酸鹽緩衝液,過氧化氫,對羥基苯丙酸和納米氧化銅溶液繼續溫浴;(3)將反應產物置於螢光分光光度計中檢測螢光強度,根據尿素標準曲線測定尿液中尿素濃度;所述的納米氧化銅由如下步驟製得:1)取0.02 mol/L的醋酸銅溶液150 ml和0.5 ml冰醋酸加入到裝有冷凝管的三頸瓶中,攪拌加熱至沸騰;2)快速加入0.04 g/ml的氫氧化鈉溶液10 ml,加完後繼續攪拌5分鐘,得到黑色氧化銅沉澱;3)將反應得到的黑色氧化銅沉澱離心,用無水乙醇洗滌三次,減壓乾燥,即得納米氧化銅粉體。
所述的利用納米氧化銅為催化劑測定尿液尿素含量的螢光分析方法,其特徵是在EP管中分別加入150 µL用濃度為10 mmol/L、pH為7.0的磷酸鹽緩衝液稀釋600倍的尿液樣品和50 µL濃度為6 U/mL的脲酶溶液混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2 mg/L的納米氧化銅溶液和500 µL濃度為100mmol/L、pH為10.25的磷酸鹽緩衝溶液中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm。
所述的脲酶酶促反應體系pH值優選為7.0,脲酶濃度優選為0.3U/mL。
所述的脲酶酶促反應溫度優選為37 ℃,反應時間優選為30分鐘。
所述的螢光反應體系的pH值優選為10.25,納米氧化銅濃度優選為0.4mg/L,對羥基苯丙酸濃度優選為4mmol/L。
所述的螢光反應溫度優選為65℃,反應時間優選為15分鐘。
本發明的技術方案具體步驟如下:
(一)納米氧化銅的製備:
取醋酸銅溶液和冰醋酸加入到裝有冷凝管的三頸瓶中,攪拌加熱至沸騰,快速加入氫氧化鈉溶液,加完後,繼續攪拌後,得到黑色氧化銅。將反應得到的黑色氧化銅立即離心,用無水乙醇洗滌,減壓乾燥,即得納米氧化銅粉體。將納米氧化銅粉體分散於二次蒸餾水中得到棕色納米氧化銅膠體溶液。
納米氧化銅具體製備步驟如下:
(1)取0.02 mol/L的醋酸銅溶液150 ml和0.5 ml冰醋酸加入到裝有冷凝管的三頸瓶中,攪拌加熱至沸騰;
(2)快速加入0.04 g/ml的氫氧化鈉溶液10 ml,加完後繼續攪拌5分鐘,得到黑色氧化銅沉澱;
(3)將反應得到的黑色氧化銅沉澱離心,用無水乙醇洗滌三次,減壓乾燥,即得納米氧化銅粉體。
(二)尿素的測定
首先將尿素、脲酶和磷酸鹽緩衝液三者混合,混合液放入37℃溫浴30分鐘進行脲酶酶促反應,然後向其中加入對羥基苯丙酸、過氧化氫、納米氧化銅和磷酸鹽緩衝液後65 ℃溫浴反應15分鐘,測定螢光強度,以螢光強度差值對尿素濃度對數值作圖得到標準曲線以用於測定尿素。
(三)尿液中尿素的測定
將尿素替換為稀釋後的尿液樣品重複步驟二,將所得螢光強度代入標準曲線即可得到尿液中尿素的濃度。
本發明的優點:
本發明利用納米氧化銅的模擬鹼性過氧化物酶特性,成功構建了一種檢測尿素的螢光分析方法。該技術測定尿素的線性範圍為0.0375~0.3 mmol/L,其檢測限為27 µmol/L。本發明具有靈敏度高,樣品需求量少,重現性好,成本低等優點,可應用於尿液樣品中尿素的測定。
附圖說明
圖1為螢光體系的螢光光譜圖。
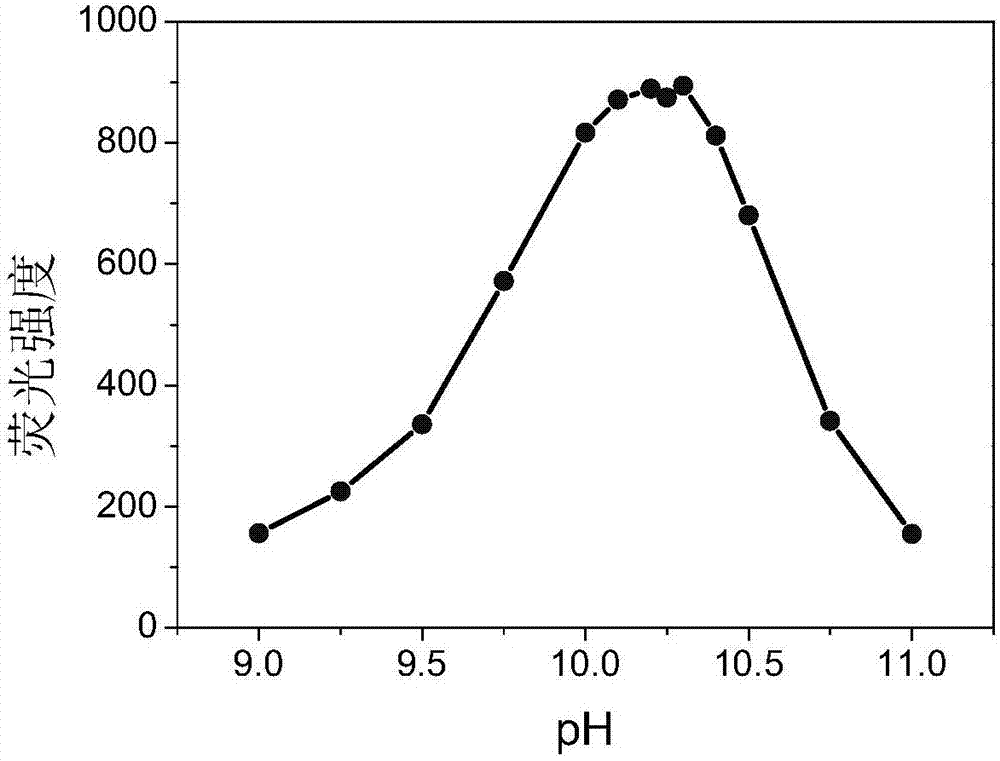
圖2為pH值對螢光強度的影響圖。
圖3為納米氧化銅濃度對螢光強度的影響圖。
圖4為對羥基苯丙酸濃度對螢光強度的影響圖。
圖5為尿素濃度對螢光強度的影響圖。
圖6為脲酶濃度對螢光強度的影響圖。
圖7為尿素的標準曲線圖。
具體實施方式
以下通過實施例對本發明做進一步說明,但是本發明不僅限於此。
實例1:
納米氧化銅具體製備步驟如下:(1)取0.02 mol/L的醋酸銅溶液150 ml和0.5 ml冰醋酸加入到裝有冷凝管的三頸瓶中,攪拌加熱至沸騰;(2)快速加入0.04 g/ml的氫氧化鈉溶液10 ml,加完後繼續攪拌5分鐘,得到黑色氧化銅沉澱;(3)將反應得到的黑色氧化銅沉澱離心,用無水乙醇洗滌三次,減壓乾燥,即得直徑為6 nm的納米氧化銅粉體。
實例2:
將50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸和200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液加入到700 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合搖勻後置於65℃溫浴,15分鐘後測定其螢光光譜。如圖1所示,螢光產物激發波長為320 nm,發射波長為409 nm。
實例3:
將50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸和200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液加入到700 µL濃度為100mmol/L不同pH的磷酸鹽緩衝溶液(pH 9~11)中,混合搖勻後置於65℃溫浴,15分鐘後測定其在409 nm處的螢光強度(激發波長為320 nm)。如圖2所示,螢光強度在pH為10.1~10.3之間達到最大值。
實例4:
將50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸和200 µL不同濃度的實例1製備的納米氧化銅溶液(0~5 mg/L)加入到700 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合搖勻後置於65℃溫浴,15分鐘後測定其在409 nm處的螢光強度(激發波長為320 nm)。如圖3所示,螢光強度隨混合液中納米氧化銅濃度增大而增大並在終濃度為0.4 mg/L時達到最大。
實例5:
將50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL不同濃度的對羥基苯丙酸(0~80 mmol/L)和200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液加入到700 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合搖勻後置於65℃溫浴,15分鐘後測定其在409 nm處的螢光強度(激發波長為320 nm)。如圖4所示,螢光強度隨混合液中對羥基苯丙酸濃度增大而增大,在終濃度為3.5 mmol/L時,螢光強度達到最大值。
實例6:
將150 µL不同濃度的尿素溶液(0~15 mmol/L,用濃度為10mmol/L,pH為7.0的磷酸鹽緩衝液配製)和50 µL濃度為6 U/mL的脲酶溶液混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液和500 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm,如圖5所示,螢光強度差值隨混合液中尿素濃度增大而增大,在終濃度為0.75 mmol/L時,螢光強度達到穩定值。
實例7:
將150 µL濃度為15 mmol/L的尿素溶液(用濃度為10mmol/L,pH為7.0的磷酸鹽緩衝液配製)和50 µL不同濃度的脲酶溶液(0.04~6 U/mL)混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液和500 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm,如圖6所示,螢光強度差值隨混合液中脲酶濃度增大而增大,在終濃度為0.1 U/mL時,螢光強度達到穩定值。
實例8:
將150 µL不同濃度的尿素溶液(0.25~2 mmol/L,用濃度為10mmol/L,pH為7.0的磷酸鹽緩衝液配製)和50 µL濃度為6 U/mL的脲酶溶液混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2mg/L的實例1製備的納米氧化銅溶液和500 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm,以螢光強度差值對尿素濃度對數值作圖得到尿素標準曲線。如圖7所示,螢光強度與尿素濃度在0.0375~0.3 mmol/L範圍內呈線性關係,檢測限為27 µmol/L。
實例9:
在EP管中分別加入150 µL用濃度為10mmol/L,pH為7.0的磷酸鹽緩衝液稀釋600倍的尿液樣品和50 µL濃度為6 U/mL的脲酶溶液混合,混合液在37 ℃溫浴水解反應30分鐘,隨後向混合液中依次加入50 µL濃度為120 mmol/L的過氧化氫溶液,50 µL濃度為80 mmol/L的對羥基苯丙酸,200 µL濃度為2mg/L的納米氧化銅溶液和500 µL濃度為100mmol/L的磷酸鹽緩衝溶液(pH 10.25)中,混合液在65 ℃溫浴,15分鐘後分別測定其在409 nm處的螢光強度,激發波長為320 nm。經實例8所得尿素標準曲線計算得出尿液樣品中尿素含量,此數值與二乙醯一肟法得到的數據一致。樣品回收率93.5~105.6%,相對標準偏差1.0%~3.1%,由此可見本方法可靠適用。
以上所述僅為本發明的較佳實施例而已,並不用以限制本發明,凡在本發明的精神和原則之內所作的任何修改,等同替換和改進等,均應包含在本發明的保護範圍之內。
