腹瀉相關病毒多重基因檢測體系及其試劑盒和應用的製作方法
2023-04-24 08:01:40 2
本發明涉及一種多重基因檢測產品以及該產品所用到的檢測體系,屬於生物技術領域。
背景技術:
感染性腹瀉是由多種病原體引起的腸道傳染病,是全世界範圍內最高發的消化系統感染性疾病之一。全球每年患腹瀉病達20億人次左右,我國每年發病約8億人次。感染性腹瀉已經成為僅次於呼吸道感染、影響人類健康的第二大感染性疾病。
病原學診斷對感染性腹瀉的防治具有重要意義。《世界胃腸病學組織全球指南—成人和兒童急性腹瀉:全球觀點(2012)》和《中國成人急性感染性腹瀉診療專家共識(2013)》明確指出:「感染性腹瀉的診斷包括臨床診斷和病原學診斷,後者不僅為合理治療提供依據,同時為流行病學調查以及預防和控制腹瀉病的傳播和流行提供重要線索」。由於引起腹瀉的病原體種類繁多,腸道病毒是感染性腹瀉最重要的病原體之一,在兒童感染性腹瀉中尤為常見。而常規的檢測方法局限性大,難以實現精準的病原學診斷,導致臨床治療盲目、耐藥菌產生,使得感染性腹瀉未能得到最及時和有效地控制。
但是,感染性腹瀉病原體的常規檢測方法、檢測流程、臨床治療方案都具有局限性。
目前國內外檢測腹瀉相關病毒的常規方法包括:①免疫學方法:通過直接檢測糞便中病原體的特異性抗原或者血液中的特異性抗體進行病原學診斷。該方法耗時短,但敏感性和特異性低,尤其是血液中特異性抗體的產生有一個窗口期(從感染到產生可以檢測到的抗體成分),導致該方法假陰性率高。同時該方法也無法同時檢測和鑑別數十種感染性腹瀉相關的抗原或抗體。②特異性核苷酸檢測法:通過特異性檢測感染性腹瀉相關病原體的基因片段進行診斷。其優點是特異性和敏感性高,但缺點是無法同時檢測和鑑定感染性腹瀉相關的多種病原體,而且成本高。
不同的病原體引起的感染性腹瀉的治療和隔離的方法各不相同。細菌導致的感染性腹瀉,必須及時應用敏感的抗菌藥物;而病毒所致的腹瀉往往是自限性感染,不需要應用抗菌藥物,但必須維持水和電解質平衡。故治療藥物的應用必須根據患者的症狀、體徵和實驗室檢查結果,明確診斷後可應用。但是,目前的常規檢測方法存在檢出率低、耗時長、尤其無法同時對多種病原體進行準確鑑定等缺點,無法為臨床提供及時、全面和準確的病原體診斷依據,導致臨床普遍採用經驗性治療,造成療效低下、不能及時控制腹瀉和消化菌群紊亂等問題。
綜上所述,目前腹瀉病原體檢測和診斷方法不能滿足臨床需求,迫切需要開發新技術。
技術實現要素:
本發明要解決的技術問題是提供一種可以快速、全面、準確、低成本的腹瀉相關病毒多重基因檢測體系及其試劑盒,以及採用該檢測體系在製備診斷產品方面的應用。
本發明為解決上述技術問題提出的一種技術方案是:一種腹瀉相關病毒多重基因檢測體系,包括分別針對人星狀病毒、諾如病毒ii、人腸道腺病毒、輪狀病毒a、輪狀病毒b和輪狀病毒c進行檢測的正反向pcr擴增引物。
針對人星狀病毒的正向引物的核苷酸序列如seqidno.27所示,對應人星狀病毒的反向引物的核苷酸序列如seqidno.28所示;
針對諾如病毒ii的正向引物的核苷酸序列如seqidno.29所示,針對諾如病毒ii的反向引物的核苷酸序列如seqidno.30所示;
針對人腸道腺病毒的正向引物的核苷酸序列如seqidno.31所示,以及針對人腸道腺病毒的反向引物的核苷酸序列如seqidno.32所示;
針對輪狀病毒a的正向引物的核苷酸序列如seqidno.33所示,以及針對輪狀病毒a的反向引物的核苷酸序列如seqidno.34所示;
針對輪狀病毒b的正向引物的核苷酸序列如seqidno.35所示,以及針對輪狀病毒b的反向引物的核苷酸序列如seqidno.36所示;
針對輪狀病毒c的正向引物的核苷酸序列如seqidno.37所示,以及針對輪狀病毒c的反向引物的核苷酸序列如seqidno.38所示。
3.根據權利要求2所述的腹瀉病原體多重基因檢測體系,其特徵在於:還包括針對人rna內參、人dna內參、系統質控內參進行檢測的正反向pcr擴增引物;
所述人rna內參是b2m,人dna內參是rnasep,系統質控內參是含有卡那黴素抗性基因的質粒;
針對人rna內參的正向引物的核苷酸序列如seqidno.39所示,以及針對人rna內參的反向引物的核苷酸序列如seqidno.40所示;
針對人dna內參的正向引物的核苷酸序列如seqidno.41所示,以及針對人dna內參的反向引物的核苷酸序列如seqidno.42所示;
針對系統質控內參的正向引物的核苷酸序列如seqidno.43所示,以及針對系統質控內參的反向引物的核苷酸序列如seqidno.44所示。
上述針對輪狀病毒b的正向引物在檢測體系中的終濃度均為200nm;所述針對諾如病毒ii、輪狀病毒c的正向引物在檢測體系中的終濃度均為100nm,所述針對人星狀病毒的正向引物在檢測體系中的終濃度均為300nm,所述針對人腸道腺病毒的正向引物在檢測體系中的終濃度均為450nm,所述針對輪狀病毒a的正向引物在檢測體系中的終濃度均為400nm;
所述針對人腸道腺病毒、輪狀病毒b、輪狀病毒c的反向引物在檢測體系中的終濃度均為100nm,所述針對人星狀病毒、諾如病毒ii的反向引物在檢測體系中的終濃度均為400nm,所述針對輪狀病毒a的反向引物在檢測體系中的終濃度均為450nm;
針對人rna內參、人dna內參、和系統質控內參的正反向引物在檢測體系中的終濃度均為1μm。
上述腹瀉相關病毒多重基因檢測體系還包括pcr緩衝液,mgcl2溶液,dntps,以及熱啟動dna聚合酶和逆轉錄酶混合液。
上述螢光標記為cy5或cy3或fam。
上述腹瀉病原體多重基因檢測體系還包括陽性對照液和陰性對照物;所述陽性對照物是包括所有目的基因靶點的質粒混合物;所述陰性對照液是無核酸酶超純水。
反應時體系中的組分用量為5×的pcr緩衝液2體積,10μm的dntps共0.35體積,25mmol/l的mgcl2溶液0.25體積,引物混合物1體積,5u/μl的熱啟動dna聚合酶和5u/μl的逆轉錄酶混合液0.4體積,1u/μl的udg酶0.1體積dna模板2.5體積,純水2.5體積;所述基因模板的使用量為5~50ng/體系。
本發明為解決上述技術問題提出的另一種技術方案是:一種採用上述的檢測體系的腹瀉相關病毒多重基因檢測試劑盒。
本發明為解決上述技術問題提出的又一種技術方案是:一種採用上述的檢測體系製備腹瀉相關病毒的檢測和診斷產品的應用。本發明具有積極的效果:
(1)本發明的腹瀉相關病毒多重基因檢測體系及試劑盒,將所有目的基因的質粒等拷貝數混合在一起,通過調整各病原體的引物濃度,使各靶點出現的峰高相當,達到等效擴增所有靶基因的目的。
(2)本發明的腹瀉相關病毒多重基因檢測體系及試劑盒優化了反應體系,加入了防汙染的ung酶,在基因擴增前有效消除基因擴增片段汙染,確保結果的準確性和可靠性。同時,加入了反轉錄酶,實現了反轉錄和基因擴增一步完成,簡化檢測流程和縮短檢測時間,也有效降低繁瑣的操作引起的汙染。
(3)本發明的腹瀉相關病毒多重基因檢測體系及試劑盒結合毛細管電泳及螢光檢測技術,不同於傳統凝膠電泳分析模式,可將非特異性擴增產物、引物二聚體和特異性擴增產物分離,最大程度降低假陽性。該試劑盒的檢測結果無雜峰,特異性高。可檢測低至10個拷貝的病原體,靈敏度高。
(4)本發明的腹瀉相關病毒多重基因檢測體系及試劑盒不需要採用腹瀉病原體常規檢測等步驟,在同一反應體系直接對組織樣本進行多重腹瀉相關病毒的同步檢測和分析,一次檢測得出所有結果,彌補了常規檢測方法通量低、步驟多、耗時長和檢出率低等缺點,成本低、便捷性好,第一時間為臨床提供全面、精準、低成本的病原學診斷。
(5)不同的病原體引起的感染性腹瀉的治療和隔離的方法各不相同。《國家衛計委2015年抗菌藥物臨床應用指導原則》明確指出:「抗菌藥物的應用必須根據患者的症狀、體徵和實驗室檢查結果,明確診斷後可應用」。但是,目前的常規檢測方法存在檢出率低、耗時長、尤其無法同時對多種病原體進行準確鑑定等缺點,導致臨床普遍採用光譜性抗菌藥物進行經驗性治療,造成療效低下、不能及時控制腹瀉、耐藥菌株高發和消化菌群紊亂等問題。本發明採用建立了一種高通量、快速、準確、低成本的腹瀉相關病毒快速鑑定系統,可以同步檢測6種感染性腹瀉相關病毒,有效彌補常規檢測方法檢出率低、耗時長和不能同時進行多種病原體鑑定等缺點,可在第一時間內明確病原體種類,以便臨床採取正確的治療方案和隔離措施,有效防止感染擴散和減少耐藥菌株的產生。
附圖說明
圖1是本發明實施例1的試劑盒對混合腹瀉病原菌陽性對照進行pcr反應後進行毛細管電泳分析後的圖譜;
圖2是本發明實施例1的試劑盒對腹瀉病原菌系列稀釋並進行pcr反應後進行毛細管電泳分析後的圖譜;
圖3是本發明實施例1的試劑盒對樣本1進行pcr反應後進行毛細管電泳分析後的圖譜;
圖4是本發明實施例1的試劑盒對樣本2進行pcr反應後進行毛細管電泳分析後的圖譜;
圖5是本發明實施例1的試劑盒對樣本3進行pcr反應後進行毛細管電泳分析後的圖譜;
圖6是本發明實施例1的試劑盒對樣本4進行pcr反應後進行毛細管電泳分析後的圖譜。
具體實施方式
下面通過實施例對本發明進行具體的描述,有必要在此指出的是以下實施例只用於對本發明進行進一步說明,不能理解為對本發明保護範圍的限制,該領域的技術人員可以根據上述本發明內容對本發明作出一些非本質的改進和調整。下述實施例中,若非特意表明,所用的試劑均為分析純,所用試劑均可從商業渠道獲得。文中未註明具體條件的實驗方法,通常按照常規條件如j.薩姆布魯克等編著的科學出版社2002年出版的《分子克隆實驗指南》一書中所述的條件,或按照製造商所建議的條件。除非另行定義,文中所使用的所有專業與科學用語與本領域熟練人員所熟悉的意義相同。此外,任何與所記載內容相似或均等的方法及材料皆可應用於本發明中。
實施例1
一、試劑盒的組成
本實施例的腹瀉病原體多重基因檢測試劑盒檢測試劑盒包括:引物混合物、pcr緩衝液(5×pcrbuffer)、mgcl2溶液、dntps、熱啟動dna聚合酶和逆轉錄酶混合液、udg酶、陽性對照物和陰性對照物。
pcr緩衝液、熱啟動dna聚合酶和逆轉錄酶混合液均來自qiagen公司(貨號:210212)。
熱啟動dna聚合酶和逆轉錄酶混合在一起形成混合液,其中熱啟動dna聚合酶在反應體系中的濃度是0.1u/μl,逆轉錄酶在混合液中的濃度是0.1u/μl。
陽性對照液是包括所有目的基因靶點的質粒混合物。
陰性對照液是無核酸酶超純水。
引物混合物中包括:針對空腸彎曲菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對志賀氏菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對艱難梭菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸炎沙門菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對鼠傷寒沙門菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸產毒性大腸埃希菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸出血性大腸埃希菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸致病性大腸埃希菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸黏附性大腸埃希菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對弧菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對腸侵襲性大腸埃希菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對小腸結腸炎耶爾森菌的正向引物的核苷酸序列和反向引物的核苷酸序列;針對大腸埃希菌o157的正向引物的核苷酸序列和反向引物的核苷酸序列;針對人星狀病毒的正向引物的核苷酸序列和反向引物的核苷酸序列;針對諾如病毒ii的正向引物的核苷酸序列和反向引物的核苷酸序列;針對人腸道腺病毒的正向引物的核苷酸序列和反向引物的核苷酸序列;針對輪狀病毒a的正向引物的核苷酸序列和反向引物的核苷酸序列;針對輪狀病毒b的正向引物的核苷酸序列和反向引物的核苷酸序列;針對輪狀病毒c的正向引物的核苷酸序列和反向引物的核苷酸序列;針對人rna內參的正向引物的核苷酸序列和反向引物的核苷酸序列;針對人dna內參的正向引物的核苷酸序列和反向引物的核苷酸序列;針對系統質控內參的正向引物的核苷酸序列和反向引物的核苷酸序列。
人rna內參是b2m,人dna內參是rnasep,系統質控內參是含有卡那黴素抗性基因的質粒。
各引物的特徵如表1所示。引物均由上海桑尼生物科技有限公司合成。
表1腹瀉病原體引物序列特徵表
二、試劑盒的使用方法
本實施例的腹瀉病原體檢測試劑盒的具體檢測步驟如下:
1.樣本採集
將腹瀉患者的糞便組織標本浸入生理鹽水中,採用天跟抽提試劑盒提取樣本總基因組,具體的操作參見抽提試劑盒產品說明書。
獲得樣本核酸基因後,經紫外分光光度計測定濃度和od260/od280的比值控制樣本核酸質量。樣本核酸的優選濃度為10ng/μl~100ng/μl。od260/od280的比值的優選範圍為1.7~1.9。
2.pcr反應
採用本實施例的試劑盒中的試劑分別與基因模板(樣本核酸、陽性對照液或陰性對照液)配製pcr反應體系,具體組分如表2所示。
表2pcr反應體系組分表
然後在pcr儀(abiveriti96well)上進行pcr反應程序,最優反應程序如表3所示。
表3pcr反應程序表
3.毛細管電泳片段分析
在96孔樣品板的每個孔中加入9μl的甲醯胺(absciex公司,貨號:608082)和0.25μl的內標(dnasizestandard500,absciex公司,貨號:608098),再將1μl的pcr產物加入其中。
根據ab3500dx毛細管電泳分析儀的操作手冊,將樣品板放入機器,運行fragment分離程序。執行默認的分析方法,最後保存數據。
針對各個基因的pcr產物片段大小不同,得到的毛細管電泳峰圖,其中橫坐標表示片段長度,縱坐標表示螢光強度。
4.結果分析
毛細管電泳分析儀自動進行數據分析。
三、試劑盒的檢測結果判定
1.試劑盒有效性判定
同時滿足下列條件,才可進行結果判定:
1)陰性對照:只檢測到系統質控內參特異峰。
2)陽性對照:在各擴增片段長度處各檢測到一個螢光信號,且螢光信號值高於300。
2.樣本有效性判定:
2)若檢測樣本的螢光信號值至少有一個高於32000,則樣本加入過量,建議對pcr產物進行適當稀釋後再進行毛細管電泳檢測。
3)若檢測樣本的螢光信號值均低於300,則樣本加入量較低,可適當增加pcr產物加入量或增加pcr反應循環數;若仍然不符合要求,需重新製備樣本。
3.結果判定標準
腹瀉病原體感染鑑定
人dna內參、人rna內參、系統質控內參和腹瀉病原體基因的目的片段區域出現了相應的峰且螢光信號值均高於300,可以判斷感染了腹瀉病原體。
4.結果判斷實例
採用本實施例的試劑盒對單個陽性對照分別進行pcr反應後採用毛細管電泳分析。基因的目標片段區域空腸彎曲菌、志賀菌、艱難梭菌、腸炎沙門菌、鼠傷寒沙門菌、腸產毒性大腸埃希菌、腸出血性大腸埃希菌、腸致病性大腸埃希菌、腸黏附性大腸埃希菌、腸侵襲性大腸埃希菌、大腸埃希菌o157、弧菌、小腸結腸炎耶爾森菌、人星狀病毒、諾如病毒ii、人腸道腺病毒、輪狀病毒a、輪狀病毒b和輪狀病毒c的19種病原體均出現了相應的峰。該結果非常直觀,基因均擴增良好。說明每對引物能有效擴增對應的目的基因,特異性好。
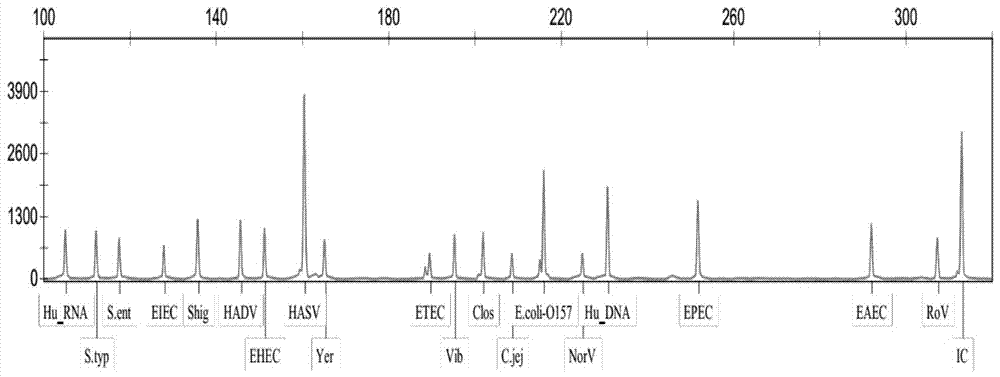
採用本實施例的試劑盒對所有陽性對照的混合進行pcr反應後採用毛細管電泳分析後圖譜如圖1所示。基因的目標片段區域空腸彎曲菌、志賀菌、艱難梭菌、腸炎沙門菌、鼠傷寒沙門菌、腸產毒性大腸埃希菌、腸出血性大腸埃希菌、腸致病性大腸埃希菌、腸黏附性大腸埃希菌、腸侵襲性大腸埃希菌、大腸埃希菌o157、弧菌、小腸結腸炎耶爾森菌、人星狀病毒、諾如病毒ii、人腸道腺病毒、輪狀病毒a、輪狀病毒b和輪狀病毒c19種病原體均出現了相應的峰。該結果非常直觀,基因均擴增良好。說明各引物之間沒有幹擾,能同時有效擴增所有目的基因。
採用本實施例的試劑盒對陰性對照進行pcr反應後採用毛細管電泳分析,沒有出現任何目的基因峰,只在小於100nt處有非特異性背景螢光信號。說明該檢測體系特異性非常好。
採用本實施例的試劑盒對單個腹瀉病原體陽性對照進行系列稀釋後,進行pcr反應後採用毛細管電泳分析後的圖譜如表4所示,檢測最低靈敏度艱難梭菌、腸產毒性大腸埃希菌、腸黏附性大腸埃希菌、腸炎沙門菌、鼠傷寒沙門菌、弧菌、小腸結腸炎耶爾森菌和輪狀病毒可達到1000個拷貝;空腸彎曲菌、腸出血性大腸埃希菌、腸致病性大腸埃希菌、腸侵襲性大腸埃希菌和人星狀病毒可達到100個拷貝;志賀菌、諾如病毒ii型和人腸道腺病毒可達到10個拷貝。說明該檢測系統對腹瀉病原體單重感染檢測的靈敏度很高。
表4腹瀉病原體檢測靈敏度
採用本實施例的試劑盒對所有的腹瀉病原體陽性對照進行混合後並系列稀釋後,進行pcr反應後採用毛細管電泳分析後的圖譜如圖2所示,在1000個拷貝/反應的稀釋度時19種目標病原體都可以被檢測出,且信號值均高於300,結果清晰易判讀。說明該檢測體系對腹瀉病原體多重感染檢測靈敏度也很高。
採用本實施例的試劑盒對樣本1進行pcr反應後採用毛細管電泳分析後的圖譜如圖3所示。人rna內參、人dna內參和系統質控內參同時出現且信號值大於300,艱難梭菌(c.difficile)基因的目標片段區域均出現了相應的峰且信號值大於300。根據結果判定標準,說明該患者感染了艱難梭菌。檢測結果非常直觀。
採用本實施例的試劑盒對樣本2進行pcr反應後採用毛細管電泳分析後的圖譜如圖4所示。人rna內參、人dna內參和系統質控內參同時出現且信號值大於300,鼠傷寒沙門(s.typhimurium)基因的目標片段區域均出現了相應的峰且信號值大於300。根據結果判定標準,說明該患者感染了鼠傷寒沙門。檢測結果非常直觀。
採用本實施例的試劑盒對樣本3進行pcr反應後採用毛細管電泳分析後的圖譜如圖5所示。人rna內參、人dna內參和系統質控內參同時出現且信號值大於300,輪狀病毒(rov)基因的目標片段區域均出現了相應的峰且信號值大於300。根據結果判定標準,說明該患者感染了輪狀病毒。檢測結果非常直觀。
採用本實施例的試劑盒對樣本4進行pcr反應後採用毛細管電泳分析後的圖譜如圖6所示。人rna內參、人dna內參和系統質控內參同時出現且信號值大於300,艱難梭菌、鼠傷寒沙門菌和人腸道腺病毒(s.typhimurium、c.difficile、hadv)基因的目標片段區域均出現了相應的峰且信號值大於300。根據結果判定標準,說明該患者同時感染了艱難梭菌、鼠傷寒沙門菌和人腸道腺病毒。檢測結果非常直觀。
實施例2
本實施例的腹瀉病原菌多重基因檢測試劑盒檢測試劑盒其餘部分與實施例1相同,不同之處在於:引物混合物中僅包括:分別針對人星狀病毒、諾如病毒ii、人腸道腺病毒、輪狀病毒a、輪狀病毒b和輪狀病毒c進行檢測的正反向pcr擴增引物,以及針對人rna內參、人dna內參、系統質控內參進行檢測的正反向pcr擴增引物。用於同步檢測6種感染性腹瀉相關病毒。
顯然,上述實施例僅僅是為清楚地說明本發明所作的舉例,而並非是對本發明的實施方式的限定。對於所屬領域的普通技術人員來說,在上述說明的基礎上還可以做出其它不同形式的變化或變動。這裡無需也無法對所有的實施方式一一列舉。而這些屬於本發明的精神所引伸出的顯而易見的變化或變動仍處於本發明的保護範圍之中。
sequencelisting
華東醫院
腹瀉相關病毒多重基因檢測體系及其試劑盒和應用
無
44
patentinversion3.3
1
28
dna
人工合成
1
gtccttcttttaaatcataaaatctatg28
2
26
dna
人工合成
2
acaagatacttttgctcaagttaatc26
3
24
dna
人工合成
3
gtcttcctctgtggaacacatata24
4
23
dna
人工合成
4
agagattgcagtgtcgtttttag23
5
23
dna
人工合成
5
gtagctgagtctgaaggagcatt23
6
27
dna
人工合成
6
tatatgttattgatggtgatgaaaaga27
7
22
dna
人工合成
7
tgtgttttatctgatgcaagag22
8
18
dna
人工合成
8
gctcgctgcacaaaagcg18
9
20
dna
人工合成
9
gcgtcttcagcgaccagttc20
10
23
dna
人工合成
10
atcttaagctacatcatcggctg23
11
27
dna
人工合成
11
ggattacatcgtaacagggaatataga27
12
24
dna
人工合成
12
caattacaggtgatacttgtaatg24
13
23
dna
人工合成
13
gacatcggtgtctgttattaacc23
14
21
dna
人工合成
14
ttgccgtattaacgaacccgg21
15
18
dna
人工合成
15
ggcgattacgcgaaagat18
16
19
dna
人工合成
16
aggaacaaacgctggccag19
17
23
dna
人工合成
17
gacacaaaagaaggaagcaatac23
18
26
dna
人工合成
18
ttgaatcatcattatgatcgatactc26
19
18
dna
人工合成
19
gcagggaaatgttccgcc18
20
18
dna
人工合成
20
agagctgaagtttctctg18
21
20
dna
人工合成
21
acatcacccatgacggtgat20
22
20
dna
人工合成
22
gggctgaaagtggcatcgac20
23
31
dna
人工合成
23
gacctgaagtaccgttatgaactcgatgata31
24
25
dna
人工合成
24
catattcgttratgcggaaagatgg25
25
24
dna
人工合成
25
gctctgcggtcctagttagaattg24
26
24
dna
人工合成
26
ttggcatgacgttataggctacaa24
27
17
dna
人工合成
27
tagragacagcccggac17
28
17
dna
人工合成
28
gtgccrctggtgtttga17
29
23
dna
人工合成
29
gacccctggattagaacaaattt23
30
19
dna
人工合成
30
cggcggcgaagaggatctt19
31
18
dna
人工合成
31
caacatcggcacccctct18
32
27
dna
人工合成
32
ggaccaagattgattattaacttagag27
33
22
dna
人工合成
33
gagggtttgaractgatagaga22
34
27
dna
人工合成
34
cttattytttgaaaaaagtagctgttc27
35
25
dna
人工合成
35
ctctcacatatggagtattagctga25
36
29
dna
人工合成
36
ggatgcaacrccatgatatcttattattt29
37
27
dna
人工合成
37
tgtcaagctatgatgttcacaatttct27
38
27
dna
人工合成
38
ggtgatgayactaatttygctaatgat27
39
19
dna
人工合成
39
gatgagtatgcctgccgtg19
40
19
dna
人工合成
40
atgcggcatcttcaaacct19
41
24
dna
人工合成
41
gtggatgctacttgtccaatgatg24
42
24
dna
人工合成
42
acaattctccgatccgtccctaac24
43
22
dna
人工合成
43
gtggccgcttttctggattcat22
44
20
dna
人工合成
44
tgaaggcacagtcgaggctg20
