多種轉基因元件同時快速檢測的方法與流程
2023-05-06 09:31:51 2
本發明屬於螢光共振能量轉移領域,特指多種轉基因元件同時快速檢測的方法,具體為螢光共振能量轉移傳感器的製備及對轉基因中啟動子和終止子的快速檢測方法。
背景技術:
轉基因作物(Genetically Modified Organisms,簡稱GMOs)是指利用生物技術,把從動物、植物或微生物等生物體中經鑑定、分離的基因插入植物基因組中,改變其遺傳組成,產生新的農藝性狀的植物,所引入的外源基因一般包括啟動子,目的基因,終止子。目前轉基因檢測方法主要有酶聯免疫吸附法(ELISA)、免疫試紙條法和蛋白質晶片,聚合酶鏈式反應(PCR)法等。但是基於蛋白的檢測方法背景信號高、蛋白質活性難以長久保持、開發特異性抗體的成本高、加工過的轉基因產品其蛋白質發生變性而無法進行檢測。基於RAN的檢測收到RNA容易降解和對實驗條件要求較高的限制,從而較難普及。而儘管PCR方法是高靈敏度的DNA水平檢測方法,但是常伴有各種假性結果出現:一方面,DNA提取時產生的各種反應抑制因子,可能使PCR呈假陰性;另一方面,PCR過程中容易引入非特異性擴增,從而使PCR呈假陽性。此外,PCR樣品需要量大,操作繁瑣,檢測時間長,還容易造成定量不準確等一系列問題。因此,發展一種非PCR擴增的快速檢測方法成為GMO檢測所追求的目標。
石墨烯納米帶(Graphene Nanoribbons,GNRs)是最近被發現的又一種新型碳質納米材料,其結構介於一維碳納米管和二維石墨烯納米片之間,被認為是拉長的石墨帶,具有準一維蜂窩構型單層帶狀結構,以及優異的性能,如導電性較好、材料容易製備、表面含有大量的含氧官能團而容易功能化等,研究者們已初步將其應用於電子學、光學、磁學、生物醫學、催化、傳感器等諸多領域。石墨烯材料自身具有螢光性能,能夠通過螢光共振能量轉移(fluorescence resonance energy transfer,FRET)來有效猝滅其他分子的螢光,傳統的螢光能量轉移速率由供體與受體距離(d)的負6次方決定,而石墨烯材料與螢光分子的螢光能量轉移速率取決於d的負4次方,螢光淬滅效率更高。但是,石墨烯納米片之間由於存在強烈的相互作用,易於重新堆砌成石墨,這給石墨烯的應用研究造成嚴重的障礙。通過選擇合適的功能材料與其雜化,形成石墨烯雜化材料,不僅可以有效地阻止石墨烯納米片的重新聚集,而且所製備的石墨烯雜化材料還可能會被賦予更加優異的物理化學性能[153]。最近的研究發現,通過將碳納米管與石墨烯進行複合,所得到的MWCNTs/GONRs,不僅可以保持碳納米管良好的機械性能,而且可以有效增加石墨烯納米片的層間距使其不易團聚,具有良好的分散性。
量子點是一種新型螢光納米材料,相對於傳統有機螢光染料分子,量子點的發射光譜窄而且不拖尾,因而,以量子點為給體的螢光共振能量轉移,可減少給體與受體發射光譜的重疊;量子點的激發光譜範圍較寬,當它作為能量給體時,可以更自由地選擇激發波長,從而最大限度地避免對受體的直接激發;量子點的發射光譜可調,也就是說它可以為吸收光譜在可見區的任一生色團作能量給體。所以,量子點應用於螢光共振能量轉移的研究,已受到廣大科研工作者的廣泛關注。由於具有良好的化學惰性、生物相容性和較低的生物毒性,在生物成像、疾病檢測、藥物輸送和光電器件應用領域中引起了極大關注。而碲化鎘量子點(CdTe QDs)可通過控制反應時間,得到不同的螢光顏色,可實現單一檢測溶液中多種目標物的同時檢測。
綠色CdTeQDs(記作:gQDs)和紅色CdTeQDs(記作:rQDs)同時作為FRET中的能量供體,而MWCNTs/GONRs作為FRET傳感器的受體。終止子的探針(記作:NP)和啟動子的探針(記作:PP)末端修飾氨基,分別與gQDs)和rQDs的羧基通過醯胺反應,形成NP-gQDs和PP-rQDs;然後兩者與MWCNTs/GONRs通過π-π疊加作用,使NP-gQDs和PP-rQDs吸附於MWCNTs/GONRs表面,淬滅QDs的螢光;當加入待檢測目標DNA,即終止子NOS和啟動子P35s後,目標DNA和NP-gQDs和PP-rQDs雜交互補配對,形成QDs-dsDNA,從而把NP-gQDs和PP-rQDs從MWCNTs/GONRs表面解離,從而使QDs的螢光恢復。
技術實現要素:
本發明旨在發明一種多元、高靈敏度、高選擇性、簡單易操作等優點為一體的FRET方法,提供一種製備工藝簡單,靈敏度高,測量範圍寬,成本低的檢測含有啟動子P35s和終止子NOS的轉基因作物及產品的方法,解決現有檢測成本高、檢測方案複雜、檢測時間過長、靈敏度較低、檢測目標單一的難題。
多元轉基因元件檢測的螢光共振能量轉移傳感器的製備方法:發出螢光信號的QDs通過醯胺反應和捕獲探針結合,形成QDs-探針;通過探針與MWCNTs/GONRs的π-π疊加作用,使QDs-探針吸附於MWCNTs/GONRs表面,淬滅QDs的螢光;當加入待檢測目標DNA,即終止子NOS和啟動子P35s後,終止子NOS和啟動子P35s分別和捕獲探針雜交互補配對,形成QDs-雙鏈DNA,從而把QDs-探針從MWCNTs/GONRs表面解離,從而使QDs的螢光恢復。通過所恢復的螢光強度的測定,檢測轉基因大豆中是否含有終止子NOS和啟動子P35s以區分轉基因和非轉基因大豆。
本發明是通過如下技術方案實現的:
多種轉基因元件同時快速檢測的方法,包括如下步驟:
步驟1、多壁碳納米管/氧化石墨烯納米帶MWCNTs/GONRs分散液的製備;
步驟2、綠色碲化鎘量子點溶液和紅色碲化鎘量子點溶液的製備;
步驟3、碲化鎘量子點-捕獲探針分散液的製備:
取步驟2製備的綠色碲化鎘量子點溶液和紅色碲化鎘量子點溶液超聲分散,採用HCl調節綠色碲化鎘量子點溶液的pH值,得到混合液A;採用HCl調節紅色碲化鎘量子點溶液的pH值,得到混合液B;向混合液A中加入1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液,振蕩均勻,加入N-羥基琥珀醯亞胺(NHS)溶液,振蕩均勻,加入終止子的探針(NP),在室溫下反應,得到綠色碲化鎘量子點-捕獲探針,記作NP-gQDs;向混合液B中加入1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液,振蕩均勻,加入N-羥基琥珀醯亞胺(NHS)溶液,振蕩均勻,加入啟動子的探針(PP);在室溫下反應,得到紅色碲化鎘量子點-捕獲探針,記作PP-rQDs;之後用乙醇洗滌,離心,最後將NP-gQDs和PP-rQDs分別分散於Tris-HCl緩衝液中,分別得到NP-gQDs分散液和PP-rQDs分散液,備用;
步驟4、螢光共振能量轉移傳感體系的構建:
將MWCNTs/GONRs分散液與NP-gQDs溶液和PP-rQDs溶液混合,超聲分散,得到混合液,靜置後,測定其螢光強度;
步驟5、標準曲線的構建:
將不同濃度的終止子NOS溶液和啟動子P35s溶液加入到步驟4所得的混合液中,超聲,靜置後,測量其螢光恢復程度,構建標準曲線;
步驟6、基於螢光共振能量轉移傳感體系對轉基因大豆的檢測:
採用植物DNA提取試劑盒提取轉基因大豆的DNA溶液,之後將轉基因大豆的DNA加入到步驟4構建的螢光共振能量轉移傳感體系中,測定其螢光恢復強度與標準曲線進行對比,得出是否含有NOS和P35s的結論。
步驟3中,製備NP-gQDs時,所使用的綠色碲化鎘量子點溶液、1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液、N-羥基琥珀醯亞胺(NHS)溶液與捕獲探針儲備液的體積比為42:2:2:1;製備PP-rQDs時,所使用的紅色碲化鎘量子點溶液、1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液、N-羥基琥珀醯亞胺(NHS)溶液與捕獲探針儲備液的體積比為42:2:2:1;製備NP-gQDs和PP-rQDs時,所使用的1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液的濃度為400mM,所使用的N-羥基琥珀醯亞胺(NHS)溶液的濃度為200mM,所使用的捕獲探針儲備液的濃度為100μM;所使用的HCl濃度為10M,所調至的pH值為5,所述的在室溫下反應的時間為40min;所使用的Tris-HCl緩衝溶液濃度為10mM,pH=7.4,所使用的Tris-HCl緩衝溶液與所使用的綠色碲化鎘量子點溶液的體積比為47:42,所使用的Tris-HCl緩衝溶液與所使用的紅色碲化鎘量子點溶液的體積比為47:42。
步驟4中,所使用的MWCNTs/GONRs分散液的濃度為1.5mg/mL,MWCNTs/GONRs分散液、NP-gQDs分散液和PP-gQDs分散液的體積比為1:750:750。
步驟5中,所使用終止子NOS溶液和啟動子P35s溶液與步驟4中的MWCNTs/GONRs分散液體積比為15:15:4,終止子NOS溶液和啟動子P35s溶液的濃度均為0~1000nM;所述超聲時間為5min,靜置時間為5min。
步驟6中,所使用轉基因大豆所提取的DNA溶液與與步驟4中的MWCNTs/GONRs-QDs-探針分散液體積比為5:1。
所用的DNA序列如下:
啟動子P35s:GGCAGAGGCATCTTCAACGATGGCC,
終止子NOS:GATTAGAGTCCCGCAATTATACATT,
啟動子的探針(PP):H2N-GGCCATCGTTGAAGATGCCTCTGCC,
終止子的探針(NP):H2N-AATGATTAATTGCGGGACTCTAATC。
所述的標準曲線是指傳感器與不同濃度的終止子和啟動子作用,通過雜交互補配對原則,目標DNA和捕獲探針結合,從而使QDs-探針從MWCNTs/GONRs表面脫離,從而發生螢光恢復。根據各個濃度所恢復的螢光繪製的標準曲線。
有益效果:
本發明基於DNA雜交互補配對的原則,使FRET傳感器的螢光得以恢復,所建立的檢測終止子和啟動子的方法,為轉基因作物中多元外源基因的同時檢測提供了一種新的方法途徑。該方法較轉基因檢測方法,具有如下優點:
(1)該傳感器的製備是基於DNA互補配對雜交特異性作用所構建的,因而相對於免疫反應而言有與目標分子結合力強、特異性高、長時間暴露不容易變性、對周圍環境要求不高等特點。
(2)傳感器構建的設計思路清晰,採用QDs為能量供體,MWCNTs/GONRs為能量受體構建了螢光共振能量轉移傳感器。
(3)該方法所有試劑具有無毒,低價,合成方法簡單等優點,相對於其他方法成本降低很多。
(4)該方法具有FRET傳感器所具有的操作簡便靈活、分析速度快、可實現多元目標的同時檢測的特點,適用於多元目標的快速檢測分析。
附圖說明
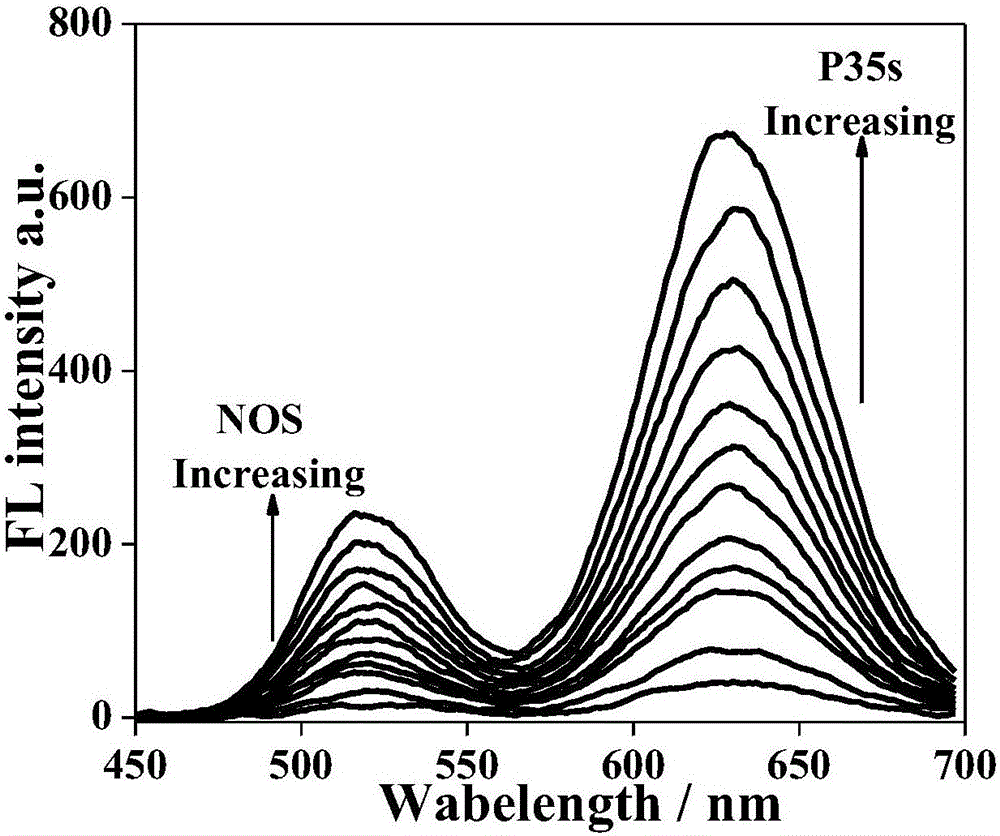
圖1為檢測不同濃度終止子和啟動子的標準曲線圖,其中濃度自下而上依次為0,1.5,2.5,5,7.5,10,20,50,100,200,500,1000nM。
具體實施方式
下面結合具體實施例對本發明作進一步描述:
實施例1:
(1)MWCNTs/GONRs的製備
MWCNTs/GONRs採用氧化剪切多壁碳納米管制得,具體過程如下:稱取120mg多壁碳納米管加入圓底燒瓶中,向燒瓶中加入40mL H2SO4/H3PO4(9:1)並攪拌,然後向上述混合溶液中加入600mg KMnO4,並在65℃油浴下繼續攪拌2h。將反應後溶液冷卻至室溫,將其倒入400mL含0.375%H2O2的冰水中,溶液經PTFE膜(孔徑0.2μm)過濾得到固體產物MWCNTs/GONRs,並繼續水洗數次。
(2)碲化鎘QDs的製備
將0.0673g硼氫化鈉和0.0957g碲粉加入10mL比色管中,加入4mL二次水,通氮除氧15min,於4℃冰箱內反應得到上清液呈紫色透明的硼氫化鈉溶液;在100mL三頸燒瓶中,加入50mL二次水,0.1142g氯化鉻和75μL巰基丙酸,在攪拌條件下通氮保護,加入氫氧化鈉調節溶液pH至8.5;迅速加入2mL上述新鮮製備的碲氫化鈉溶液,充分攪拌後,100℃下分別回流0.5h和10h得到巰基丙酸修飾的綠色和紅色碲化鎘量子點;純化步驟後,將其重新分散在10mL二次水中,置於4℃冰箱中保存備用。
(3)QDs-探針分散液的製備
取420μL QDs溶液超聲分散15分鐘後,加入20μL 400mM的1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC),振蕩2分鐘後,加入20μL 200mM的N-羥基琥珀醯亞胺(NHS),繼續振蕩20分鐘。加入10μL 100μM捕獲探針在室溫下反應40分鐘,得到QDs-探針之後用乙醇洗滌離心,最後分散於470μL的10mM Tris-HCl(pH 7.4)緩衝液中,得到QDs-探針分散液。
(4)MWCNTs/GONRs和QDs-探針FRET傳感器的構建
將4μL 1.5mg/mL的MWCNTs/GONRs加入到含有3.0mL NP-gQDs分散液和3.0mL PP-gQDs分散液的混合液中,超聲5min,靜置5min後,測定螢光強度。
實施例2:該FRET傳感器對目標DNA標準曲線的構建
將4μL 1.5mg/mL的MWCNTs/GONRs加入到含有3.0mL NP-gQDs分散液和3.0mL PP-gQDs分散液的混合液中,超聲5min,靜置5min後,測定螢光強度,隨後加入15μL不同濃度的終止子和15μL不同濃度的啟動子,超聲5min後,靜置40min測量其螢光恢復程度,構建標準曲線。
圖1中顯示,當加入NP-gQDs和PP-gQDs和MWCNTs/GONRs時,綠色碲化鎘量子點和紅色碲化鎘量子點的螢光均被淬滅,而加入不同濃度的目標NOS終止子和P35s啟動子後,隨著目標物濃度的增大,兩種量子點的螢光得到不同程度的恢復。根據螢光恢復程度可同時定量檢測兩種目標DNA。
實施例3:
基於MWCNTs/GONRs-QDs-探針構建的FRET傳感器對轉基因大豆中啟動子和終止子的檢測:
採用植物DNA提取試劑盒提取轉基因大豆的DNA。之後將20μL轉基因大豆的DNA加入到MWCNTs/GONRs和NP-gQDs和PP-gQDs的FRET傳感體系中,測定其螢光恢復強度與標準曲線進行對比,得出是否含有終止子和啟動子的結論,如存在,則可進一步得出終止子和啟動子濃度。
FRET為螢光共振能量轉移。
本發明中所用的DNA序列如下:
啟動子P35s:GGCAGAGGCATCTTCAACGATGGCC,
終止子NOS:GATTAGAGTCCCGCAATTATACATT,
啟動子的探針(PP):H2N-GGCCATCGTTGAAGATGCCTCTGCC,
終止子的探針(NP):H2N-AATGATTAATTGCGGGACTCTAATC。
SEQUENCE LISTING
江蘇大學
多種轉基因元件同時快速檢測的方法
多種轉基因元件同時快速檢測的方法
4
PatentIn version 3.5
1
25
DNA
人工序列
1
ggcagaggca tcttcaacga tggcc 25
2
25
DNA
人工序列
2
gattagagtc ccgcaattat acatt 25
3
25
DNA
人工序列
3
ggccatcgtt gaagatgcct ctgcc 25
4
25
DNA
人工序列
4
aatgattaat tgcgggactc taatc 25
