一種能與人β-Klotho受體特異性結合的抗體及其用途的製作方法
2023-04-28 09:38:06 3
本發明涉及基因工程技術領域,特別涉及一種能與人β-klotho受體特異性結合的抗體及其用途。
背景技術:
成纖維細胞生長因子21(fibroblastgrowthfactor21,fgf21)是成纖維細胞生長因子家族(fgf19,fgf21和fgf23)的一名新成員,屬於分泌型蛋白質(itohetal.,(2004)trendgenet.20:563-69)。fgfs與存在於細胞表面的生長因子受體(fgfrs)結合,將信號傳遞到細胞內。fgfrs有4種亞型(fgfrl-4),屬跨膜蛋白,主要由三個部分組成:即胞外區、跨膜區和胞內區,包含多個可變剪切體,如fgfr1c,fgfr2c,fgfr3c和fgfr4。與多數生長因子受體一樣,fgfrs都是酪氨酸激酶受體,在與配體結合後發生二聚化,從而激活酪氨酸激酶活性,導致下遊信號活化,包括mapks、raf1、akt1及stats(kharitonenkovetat.,(2008)biodrugs22:37-44)。fgf21不能與肝素特異性結合,在肝素的參與下,也不能與可溶性fgfrs結合,它需要另外一種跨膜蛋白β-klotho的參與,才能穩定地結合fgfr1c,從而激活fgf21的信號轉導。在對小鼠3t3-l1細胞(表面主要表達fgfrlc,低表達fgfr2c)的研究表明,β-klotho作為支架蛋白,先與fgfr1c形成複合物,通過變構活化後,促進fgf21與fgfr1c的結合,引起fgfr受體二聚化,激活下遊信號通路(ogawaetal.,(2007)pnas104:7432-7)。
過表達fgf21的轉基因小鼠表現為低胰島素、低膽固醇及低甘油三酯,胰島素敏感性提高,阻止高脂食物引起的體重增加(kharitonenkovetal.,(2005)jclininvest115:1627-35);相反,fgf21基因敲除小鼠表現為體重增加、糖耐量受損。這些數據表明,fgf21通過作用於脂肪組織及胰腺來改善血糖、三醯甘油和胰高血糖素,改善胰島β細胞的功能,從而預防飲食誘導的肥胖及胰島素抵抗。fgf21也被證明可作為一種主要的內源性調控因子,在禁食和酮症時起著關鍵的調控作用。更為重要的是,通過給予fgf21,不會導致低血糖症。因此,作為一種不依賴胰島素的血糖調節因子,fgf21目前已被看作治療ii型糖尿病的潛在的新型治療手段。
儘管目前有很多通過基因工程的方法改造天然的fgf21,使之成為新的治療藥物的例子(adamsetal.,(2013)plosone8(6):e65763),但是,改造後的fgf21在有些藥學特性還遠遠不能滿足要求,比如藥代動力學、穩定性、溶解性等等。而另外一種可行的辦法是產生全新的、具有類似fgf21活性的蛋白質,比如抗體。
β-klotho已被證明是fgf19和fgf21所必需的共受體,它特異性地表達在肝臟、胰腺及脂肪組織中(ogawaetal.,(2007)pnas104:7432-7)。相對於fgfrs廣泛表達於各種組織,加上單克隆抗體具有很好的結合特異性,給予抗β-klotho抗體可以有效地降低藥物的毒副作用。本發明提供了一類新的,可以和β-klotho跨膜蛋白特異性結合的抗體,通過蛋白與蛋白之間的相互作用,模擬fgf21的作用,激活人β-klotho/fgfr1c複合受體,引起細胞內erk的磷酸化,以及製備和應用這類生物大分子的方法。
技術實現要素:
本發明的目的在於提供一種能與人β-klotho受體特異性結合的抗體,能與成纖維細胞生長因子21(fibroblastgrowthfactor21,fgf21)的輔助受體β-klotho特異性結合,可以激活人β-klotho/fgfr1c複合受體的功能,本發明抗體可以應用於治療或預防哺乳動物中的ii型糖尿病以及相關疾病。
本發明解決其技術問題所採用的技術方案是:
一種能與人β-klotho受體特異性結合的抗體,所述抗體包含以下方案之一的胺基酸序列:
a.選自以下序列之一的輕鏈cdr3序列:
與選自l1-l3的輕鏈cdr3序列:seqidno:15、seqidno:24、seqidno:34其中之一相差總共不超過三個胺基酸添加、替換和/或缺失的輕鏈cdr3序列;
優選的,與選自l1-l3的輕鏈cdr3序列:seqidno:15、seqidno:24、seqidno:34其中之一相差總共不超過兩個胺基酸添加、替換和/或缺失的輕鏈cdr3序列;更優選,與選自l1-l3的輕鏈cdr3序列:seqidno:15、seqidno:24、seqidno:34其中之一相差總共不超過一個胺基酸添加、替換和/或缺失的輕鏈cdr3序列。
b.選自以下序列之一的重鏈cdr3序列:
與選自h1-h3的重鏈cdr3序列:seqidno:10、seqidno:19、seqidno:29其中之一相差總共不超過四個胺基酸添加、替換和/或缺失的重鏈cdr3序列;
優選的,與選自h1-h3的重鏈cdr3序列:seqidno:10、seqidno:19、seqidno:29其中之一相差總共不超過三個胺基酸添加、替換和/或缺失的重鏈cdr3序列;
優選的,與選自h1-h3的重鏈cdr3序列:seqidno:10、seqidno:19、seqidno:29其中之一相差總共不超過兩個胺基酸添加、替換和/或缺失的重鏈cdr3序列;
更優選,與選自h1-h3的重鏈cdr3序列:seqidno:10、seqidno:19、seqidno:29其中之一相差總共不超過一個胺基酸添加、替換和/或缺失的重鏈cdr3序列。
c.方案a的輕鏈cdr3序列和方案b的重鏈cdr3序列。
作為優選,所述抗體還包含以下方案的一種或幾種組合的胺基酸序列:
a.選自以下之一的輕鏈cdr1序列:
與選自l1-l3的輕鏈cdr1序列:seqidno:13、seqidno:22、seqidno:32其中之一相差不超過三個胺基酸添加、替換和/或缺失的輕鏈cdr1序列;
優選的,與選自l1-l3的輕鏈cdr1序列:seqidno:13、seqidno:22、seqidno:32其中之一相差不超過兩個胺基酸添加、替換和/或缺失的輕鏈cdr1序列;
更優選,與選自l1-l3的輕鏈cdr1序列:seqidno:13、seqidno:22、seqidno:32其中之一相差不超過一個胺基酸添加、替換和/或缺失的輕鏈cdr1序列。
b.選自以下之一的輕鏈cdr2序列:
與選自l1-l3的輕鏈cdr2序列:seqidno:14、seqidno:23、seqidno:33其中之一相差不超過兩個胺基酸添加、替換和/或缺失的輕鏈cdr2序列;
優選的,與選自l1-l3的輕鏈cdr2序列:seqidno:14、seqidno:23、seqidno:33其中之一相差不超過一個胺基酸添加、替換和/或缺失的輕鏈cdr2序列。
c.選自以下之一的重鏈cdr1序列:
與選自h1-h3的重鏈cdr1序列:seqidno:8、seqidno:18、seqidno:27其中之一相差不超過兩個胺基酸添加、替換和/或缺失的重鏈cdr1序列;
優選的,與選自h1-h3的重鏈cdr1序列:seqidno:8、seqidno:18、seqidno:27其中之一相差不超過一個胺基酸添加、替換和/或缺失的重鏈cdr1序列。
d.選自以下之一的重鏈cdr2序列:
與選自h1-h3的重鏈cdr2序列:seqidno:9、seqidno:28其中之一相差不超過三個胺基酸添加、替換和/或缺失的重鏈cdr2序列;
優選的,與選自h1-h3的重鏈cdr2序列:seqidno:9、seqidno:28其中之一相差不超過兩個胺基酸添加、替換和/或缺失的重鏈cdr2序列;更優選,與選自h1-h3的重鏈cdr2序列:seqidno:9、seqidno:28其中之一相差不超過一個胺基酸添加、替換和/或缺失的重鏈cdr2序列。 一種能與人β-klotho受體特異性結合的抗體,
所述抗體包含以下方案之一:
方案a:包含輕鏈cdr1序列、輕鏈cdr2序列、輕鏈cdr3序列中的一種或幾種的輕鏈可變結構域,所述輕鏈cdr1序列選自seqidno:13、seqidno:22、seqidno:32其中之一;所述輕鏈cdr2序列選自seqidno:14、seqidno:23、seqidno:33其中之一;所述輕鏈cdr3序列選自seqidno:15、seqidno:24、seqidno:34其中之一;
方案b:包含重鏈cdr1序列、重鏈cdr2序列、重鏈cdr3序列中的一種或幾種的重鏈可變結構域,所述重鏈cdr1序列選自seqidno:8、seqidno:18、seqidno:27其中之一;所述重鏈cdr2序列選自seqidno:9、seqidno:28其中之一;所述重鏈cdr3序列選自seqidno:10、seqidno:19、seqidno:29其中之一;
方案c:方案a的輕鏈可變結構域和方案b的重鏈可變結構域的組合。
一種能與人β-klotho受體特異性結合的抗體,所述抗體包含以下方案之一的胺基酸序列:
方案a.選自以下選項之一的輕鏈可變結構域序列:
i.具有與選自l1-l3的輕鏈可變結構域序列:seqidno:16、seqidno:25、seqidno:35其中之一至少80%相同的胺基酸序列;
ii.具有與編碼l1-l3的輕鏈可變結構域序列的多聚核苷酸序列:seqidno:12、seqidno:21、seqidno:31其中之一至少80%相同的多聚核苷酸序列編碼的胺基酸序列;
方案b.選自以下選項之一的重鏈可變結構域序列:
i.具有與h1-h3的重鏈可變結構域序列:seqidno:11、seqidno:20、seqidno:30其中之一至少80%相同的胺基酸序列;
ii.具有與編碼h1-h3的重鏈可變結構域序列的多聚核苷酸序列:seqidno:7、seqidno:17、seqidno:26其中之一至少80%相同的多聚核苷酸序列編碼的胺基酸序列;
方案c.方案a的輕鏈可變結構域序列和方案b的重鏈可變結構域序列的組合。
作為優選,所述抗體包含以下方案之一的胺基酸序列:
方案a.選自l1-l3的輕鏈可變結構域序列:seqidno:16、seqidno:25、seqidno:35其中之一的輕鏈可變結構域序列;
方案b.選自h1-h3的重鏈可變結構域序列:seqidno:11、seqidno:20、seqidno:30其中之一的重鏈可變結構域序列;
方案c.方案a的輕鏈可變結構域序列和方案b的重鏈可變結構域序列的組合。
作為優選,方案c中方案a的輕鏈可變結構域序列與方案b的重鏈可變結構域序列的組合選自以下之一:l1h1、l2h2、l3h3。
作為優選,所述抗體為鼠源抗體、人源化抗體、嵌合抗體、單克隆抗體、多克隆抗體、重組抗體、抗原結合抗體片段、單鏈抗體、雙鏈抗體、三鏈抗體、四鏈抗體、fab片段、f(ab』)x片段、結構域抗體、igd抗體、ige抗體、igm抗體、iggl抗體、igg2抗體、igg3抗體、igg4抗體中的一種。
作為優選,當所述抗體與人β-klotho受體結合時:
a.以與成纖維細胞生長因子21(fgf21)基本相同的kd與人β-klotho受體結合;
b.以與fgf21基本相同的ec50激活人β-klotho/fgfr1c受體複合物;
c.在人β-klotho受體上與fgf21沒有交叉競爭結合。
作為優選,所述抗體為鼠源抗體或人源化抗體時,當其與人β-klotho受體結合時:
a.以≤200nm的ec50值增強人β-klotho信號傳導;
b.在ii型糖尿病大鼠模型或ii型糖尿病小鼠模型中改善ii型糖尿病;
c.a和b兩者。
一種藥用組合物,其包含與藥用可接受載體混合的本發明的抗體。
作為優選,所述抗體選自鼠源抗體或人源化抗體。
一種分離的核酸,其包含編碼本發明的抗體的輕鏈可變結構域、重鏈可變結構域或輕鏈可變結構域和重鏈可變結構域兩者的多聚核苷酸序列。
作為優選,編碼本發明的抗體的輕鏈可變結構域的多聚核苷酸序列選自seqidno:12、seqidno:21、seqidno:31其中之一;
編碼本發明的抗體的重鏈可變結構域的多聚核苷酸序列選自seqidno:7、seqidno:17、seqidno:26其中之一。
一種重組表達載體,其包含本發明的核酸。
一種宿主細胞,其包含本發明的載體。
一種生產能與人β-klotho受體特異性結合的抗體的方法,包括在允許表達 所述抗體的條件下培養本發明的宿主細胞。
一種本發明的藥用組合物在製備用於治療ii型糖尿病以及相關病症的藥物中的用途。
本發明的有益效果是:
(a)本發明的單克隆抗體針對人β-klotho受體有高親和力和激活活性,在細胞水平可以明顯激活β-klotho/fgfr1c複合受體信號通路。
(b)本發明的單克隆抗體針對人β-klotho受體,目前在國內外均無針對相同靶標的抗體專利或藥物。
因此,本發明的高親和力、高特異性的單克隆抗體在臨床上具有重要的價值。
附圖說明
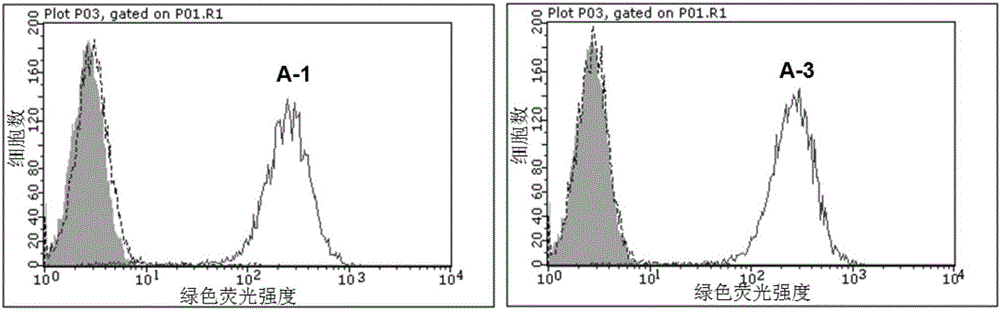
圖1顯示了流式細胞術(facs)檢測雜交瘤細胞上清的anti-klb(a-1,a-3)與人klb的特異性結合結果。從左至右:灰色峰為陰性對照,虛線表示anti-klb與cho-dhfr的結合曲線,實線表示anti-klb與cho-dhfr-klb的結合曲線。
圖2顯示了流式細胞術(facs)檢測重組表達的anti-klb(a-1,a-3)與人klb的特異性結合結果。從左至右:灰色峰為陰性對照,虛線表示anti-klb與cho-dhfr的結合曲線,實線表示anti-klb與cho-dhfr-klb的結合曲線。
圖3顯示了報告基因實驗檢測重組表達的anti-klb(a-1,a-2,a-3)與 人klb的濃度梯度激活曲線(ec50=3.29nm,r2=0.94)(a-1),(ec50=5.89nm,r2=0.95)(a-2),(ec50=33.90nm,r2=0.97)(a-3)。
圖4顯示了重組表達的anti-klb(a-1,a-2)在10nm的濃度下,均可引起細胞內erk的磷酸化升高。
具體實施方式
下面通過具體實施例,並結合附圖,對本發明的技術方案作進一步的具體說明。
本發明中,若非特指,所採用的原料和設備等均可從市場購得或是本領域常用的。下述實施例中的方法,如無特別說明,均為本領域的常規方法。
本發明涉及抗體例如可與人β-klotho受體(klb)特異性結合的抗體。這些包括與人klb結合併激活人β-klotho/fgfr1c複合受體的抗體。在一個實施方案中提供了包括激活性抗體的可改善動物模型ii型糖尿病的鼠源抗體。
本發明進一步提供可特異性結合至人β-klotho受體的抗體相關的組合物、試劑盒和方法。也提供了核酸分子及其衍生物和片段,其包含編碼與β-klotho受體結合的多肽的全部或部分的多聚核苷酸,例如編碼全部或部分抗β-klotho受體抗體、抗體片段或抗體衍生物的核酸。本發明進一步提供包含該類核酸的載體和質粒以及包含該類核酸和/或載體和質粒的細胞和細胞系。所提供方法包括,例如,製備、鑑定或分離與人klb結合的抗體例如抗klb抗體的方法,測定該抗體是否與klb結合的方法、以及將 與klb結合的抗體給予動物模型的方法。
定義
使用標準的單字母或三字母縮寫表明多聚核苷酸和多肽序列。除非另外指明,多肽序列的氨基端在左而它們的羧基端在右,單鏈核酸序列和雙鏈核酸序列的上遊鏈的5』端在左而它們的3』端在右。多肽的具體部分可由胺基酸殘基編號表示,例如胺基酸80至130,或由該位點的實際殘基表示例如lys80至lys130。也可通過解釋其與參比序列的差異描述具體的多肽或多聚核苷酸序列。具體輕鏈和重鏈可變結構域的多聚核苷酸和多肽可表示為l1(「輕鏈可變結構域1」),h1(「重鏈可變結構域1」)。包含輕鏈和重鏈的抗體可通過結合輕鏈的名稱和重鏈可變結構域的名稱表示。例如,「l1h1"表示包含l1輕鏈可變結構域和h1重鏈可變結構域的抗體。
除非本文另外定義,與本文相關的科學和技術術語應具有本領域普通技術人員所理解的含義。
抗體
一方面,本發明提供與人β-klotho受體特異性結合的抗體(例如,抗體、抗體片段、抗體衍生物、抗體突變蛋白和抗體變異體)。在一個實施方案中該抗體為鼠源抗體或其人源化抗體。
根據本發明的抗體包括與人β-klotho受體結合併通過β-klotho受體激活人β-klotho/fgfr1c複合受體介導信號傳導的抗體。在一個實施方案中,該抗體的ec50值為200nm或更低。另一方面,該抗體與β-klotho受體特異性結合,激活信號傳導並顯示出治療性生物作用,例如改善動物模 型的ii型糖尿病。在一個實施方案中,該抗體為與β-klotho受體特異性結合併通過人β-klotho/fgfr1c複合受體激活信號傳導的鼠源抗體。在另一實施方案中,該抗體為與β-klotho體特異性結合、通過人β-klotho/fgfr1c複合受體激活信號傳導並可以改善ii型糖尿病的鼠源抗體。
在一個實施方案中,該抗體包含與下表中a-1至a-3的cdr序列各相差5、4、3、2、1或0個單胺基酸添加、替換和/或缺失的序列。如本文所使用,與表1所示的cdr序列最多不超過例如四個胺基酸添加、瞽換和或缺失的cdr序列指與表1中的序列相比具有4、3、2、1或0個單胺基酸添加、替換和/或缺失的序列。
在另一個實施方案中,該抗體包含一個或多個cdr一致序列(consensussequences)。提供了輕鏈cdr1、cdr2、cdr3和重鏈cdr1、cdr2和cdr3的一致序列。
抗體a-1-a-3的輕鏈cdrs以及示例性抗體a-1-a-3的重鏈cdrs見表1。a-1至a-3對應於下文的ll至l3以及下文的h1至h3。也顯示了編碼cdrs胺基酸序列的多聚核苷酸序列。
另一方面,本發明提供包含選自l1-l3的輕鏈可變區或選自h1-h3的重鏈可變區及其片段、衍生物、突變蛋白或變異體的抗體。可用名稱「lxhy」表示該類抗體,其中「x」對應於輕鏈可變區並且「y」對應於重鏈可變區。例如,l2h1指具有包含如下文表2所示l2胺基酸序列的輕鏈可變區和包含h1胺基酸序列的重鏈可變區的抗體。本發明抗體包括例如包含選 自組合l1h1、l2h2、l3h3的輕鏈和重鏈可變結構域的組合。在一個實施方案中,該抗體為鼠源抗體或其人源化抗體。
表1:輕、重鏈可變區序列
表2提供了編碼示例性klb抗體的可變輕鏈和可變重鏈結構域的胺基酸序列的多聚核苷酸(dna)序列。
表2:輕、重鏈可變區多聚核苷酸和胺基酸序列
本發明抗體的具體實施方案包含與一個或多個上文所列cdrs和/或frs(骨架區)的胺基酸序列相同的一個或多個胺基酸序列。在一個實施方案中,該抗體包含上文所列輕鏈cdr1序列。在另一個實施方案中,該抗體包含上文所列的輕鏈cdr2序列。在另一個實施方案中,該抗體包含上文所列的輕鏈cdr3序列。在另一個實施方案中,該抗體包含上文所列的重鏈cdr1序列。在另一個實施方案中,該抗體包含上文所列的重鏈cdr2序列。在另一個實施方案中,該抗體包含上文所列的重鏈cdr3序列。在另一個實施方案中,該抗體包含上文所列的輕鏈fr1序列。在另一個實施方案中,該抗體包含上文所列的輕鏈fr2序列。在另一個實施方案中,該抗體包含上文所列輕鏈fr3序列。在另一個實施方案中,該抗體包含上文所列輕鏈fr4序列。在另一個實施方案中,該抗體包含上文所列重鏈fr1序列。在另一個實施方案中,該抗體包含上文所列重鏈fr2序列。在另一個實施方案中,該抗體包含上文所列重鏈fr3厚列。在另一個實施方案中,該抗體包含上文所列重鏈fr4序列。
在另一個實施方案中,至少一個抗體的cdr3序列與來自a-1至a-3的cdr3序列的差異最多不超過6、5、4、3、2、1或0個單胺基酸添加、替換和/或缺失。在另一個實施方案中,抗體的輕鏈cdr3序列與上述a-1 至a-3的輕鏈cdr3序列的差異不得超過6、5、4、3、2、1或0個單胺基酸添加、替換和/或缺失並且抗體的重鏈cdr3序列與上文所述a-1至a-3的重鏈cdr3序列的差異最多不超過6、5、4、3、2、1或0個單胺基酸添加、替換和/或缺失。在另一個實施方案中,抗體進一步包含1、2、3、4或5個cdr序列,各序列獨自與a-1至a-3的cdr序列的差異最多不超過6、5、4、3、2、1或0個單胺基酸差異。在另一個實施方案中,抗體包含上文所列輕鏈可變區的cdrs和重鏈可變區的cdrs。在另一實施方案中,抗體包含上文所述的1、2、3、4、5和/或6個一致cdr序列。在進一步的實施方案中,該抗體包含l1h1、l2h2、l3h3中任何之一的cdrs。在一個實施方案中,該抗體為鼠源抗體。
在一個實施方案中,該抗體(例如抗體或抗體片段)包含輕鏈可變結構域,其包含與選自l1-l3的輕鏈可變結構域序列存在15、14、13、12、11、10、9、8、7、6、5、4、3、2、1或0個胺基酸差異的胺基酸序列,其中各該序列的差異獨立為一個胺基酸殘基的缺失、插入或替換。在另一個實施方案中,該輕鏈可變結構域包含與選自l1-l3的輕鏈可變結構域至少70%、75%、80%、85%、90%、95%、97%或99%相同的胺基酸序列。在另一個實施方案中,該輕鏈可變結構域包含與下文所列l1-l3多聚核苷酸序列至少70%、75%、80%、85%、90%、95%、97%或99%相同的核苷酸序列編碼的胺基酸序列。在另一個實施方案中,該輕鏈可變結構域包含在中等條件下與編碼選自l1-l3的輕鏈可變結構域的多聚核苷酸互補序列雜交的多聚核苷酸編碼的胺基酸序列。在另一個實施方棠中,該輕鏈可變結 構域包含在嚴格條件下與編碼選自l1-l3的輕鏈可變結構域的多聚核苷酸的互補序列雜交的多聚核苷酸編碼的胺基酸序列。
在另一個實施方案中,本發明提供包含重鏈可變結構域的抗體,該可變結構域包含選自h1-h3的重鏈可變結構域序列存在15、14、13、12、11、10、9、8、7、6、5、4、3、2、1或0個殘基存在差異的胺基酸序列,其中各該序列差異獨立為一個胺基酸的缺失、插入或替換。在另一個實施方案中,該重鏈可變結構域包含與選自h1-h3的重鏈可變結構域序列至少70%、75%、80%、85%、90%、95%、97%或99%相同的胺基酸序列。在另一個實施方案中,該重鏈可變結構域包含在中等嚴格條件下與編碼選自h1-h3的重鏈可變結構域的多聚核苷酸互補序列雜交的多聚核苷酸編碼的胺基酸序列。在一個實施方案中,該重鏈可變結構域包含在嚴格條件下與編碼選自h1-h3的重鏈可變結構域的多聚核苷酸互補序列雜交的的多聚核苷酸編碼的胺基酸序列。
生產鼠單克隆抗體的可選擇方法為將雜交瘤細胞注入同系基因小鼠的腹膜腔,例如經處理(例如姥鮫烷初次免疫)促進形成包含單克隆抗體的腹水的小鼠。可通過多種已確立的技術分離和純化單克隆抗體。該類分離技術包括使用蛋白a-瓊脂糖的親和色譜法、分子排阻色譜法和高子交換色譜法(參見,例如,coligan第2.7.1-2.7.12頁和第2.9.1-2.9.3頁;baines等,「purificationofimmunoglobuling(igg),」methodsinmolecularbiology,第10卷,第79-104頁(thehumanapress,inc.,1992)。可使用基於抗體的特殊性質(例如,重鏈或輕鏈同種型、結合特異性等)篩選的適當配基通過親 和色譜法純化單克隆抗體。固定化於固體載體的適當配基的實例包括蛋白a、蛋白g、抗恆定區(輕鏈或重鏈)抗體、抗獨特型抗體以及tgf-p結合蛋白或其片段或變異體。
可使用抗體結合位點中央的互補決定區(cdrs)的分子進化分離親和性增加的抗體,例如對c-erbb-2親和性增加的抗體,如schier等,1996,j.mol.biol.263:551所述。因此,該類技術可用於製備人β-klotho受體的抗體。
例如可在檢測是否存在β-klotho受體的體外或體內測定法中使用針對人β-klotho受體的抗體。
也可通過任何傳統技術製備抗體。例如,可從天然表達這些抗體的細胞將其純化(例如,可從生產抗體的雜交瘤將其純化)或使用本領域任何已知的技術在重組表達系統中生產。參見,例如,monoclonalantibodies,hybridomas:anewdimensioninbiologicalanalyses,kennet等編輯,plenumpress(1980);和antibodies:alaboratorymanual,harlowandland編輯,coldspringharborlaboratorypress(1988)。這在下文的核酸部分討論。
可通過任何已知技術製備抗體並篩選期望性質。一些技術涉及分離編碼相關抗體(例如,抗β-klotho受體抗體)的多肽鏈(或其部分)的核酸,並通過重組dna技術操作核酸。該核酸可與另一相關核酸融合或經修飾(例如通過誘變或其它傳統技術)以添加、缺失或替換一個或多個胺基酸殘基。
在另一方面本發明提供包含編碼本發明多肽或其部分的核酸的載體。 載體的實例包括但是不限於質粒、病毒載體、非游離基因哺乳動物載體和表達載體,例如重組表達載體。
本發明的重組表達載體可包含適於該核酸在宿主細胞中表達的形式的本發明核酸。該重組表達載體包括一個或多個調控序列,基於用於表達的宿主細胞進行篩選,其與該預表達的核酸序列可操作性相連。調控序列包括引導核苷酸序列在多個種類宿主細胞中組成型表達的(例如,sv40早期基因增強劑、勞斯氏肉瘤病毒啟動子和細胞巨化病毒啟動子),引導僅在某些宿主細胞中核苷酸序列的表達的(例如,組織特異調控序列,參見voss等,1986,trendsbiochem.sci.11:287,maniatis等,1987,science236:1237,其完整內容以參考形式並於本文)以及引導核苷酸序列響應具體處理或條件的誘導型表達的(例如,原核和真核系統二者中的四環黴素反應(tet-responsive)啟動子和/或鏈黴素反應啟動子)。本領域技術人員應理解表達載體的設計取決於例如用於轉化的宿主細胞的選擇、所需蛋白表達水平等因素。本發明的表達載體可引入宿主細胞,藉此生產由本文所述核酸編碼的蛋白或肽,包括融合蛋白或肽。
另一方面,本發明提供可引入本發明表達載體的宿主細胞。宿主細胞可為任何原核或真核細胞。原核宿主細胞包括革蘭氏陰性或革蘭氏陽性生物體,例如大腸桿菌或桿菌。更高級的真核細胞包括昆蟲細胞、酵母細胞以及哺乳動物源的確立細胞系。適當哺乳動物宿主細胞系的實例包括中國倉鼠卵巢(cho)細胞或它們的衍生物例如veggiecho和在無血清培養基中生長的相關細胞系(參見rasmussen等,1998,cytotechnology28:31)或 cho株dxb-11,其缺失dhfr(參見urlaub等,1980,proc.natl.acad,sci.usa77:4216-20)。其它cho細胞系包括cho-k1(atcc#ccl-61)、em9(atcc#crl-1861),和uv20(atcc#crl-1862),其它宿主細胞包括猴腎細胞的cos-7系(atcc#crl-1651)(參見gluzman等,1981,cell23:175)、l細胞、c127細胞、3t3細胞(atccccl-163),am-1/d細胞(描述於美國專利序列號6210924)、hela細胞、bhk(atcccrl-10)細胞系、來源於非洲綠猴腎細胞系cv1的cv1/ebna細胞系(atccccl-70)(參見mcmahan等,1991,emboj.10:2821)、人胚腎細胞例如293,293ebna或msr293、人上皮a431細胞、人c010205細胞、其它經轉化靈長動物細胞系、正常二倍體細胞、來源於初生組織體外培養物的細胞株、初移植體、hl-60、u937、hak或jurkat細胞。用於細菌、真菌、酵母和哺乳細胞宿主的適當克隆和表達載體描述於pouwels等(cloningvectors:alaboratorymanual,elsevier,1985)。
可通過傳統轉化或轉染技術將載體dna引入原核或真核細胞中。對於穩定的哺乳動物轉染而言,取決於使用的表達載體和轉染技術,已知只有一小部分細胞可將外源dna鏊合入它們的基因組中。為了鑑定和篩選這些整合子,通常將編碼篩選標記(例如抗生素抗性)的基因與所關注基因一起引入宿主細胞。優選的篩選標記包括可賦予藥物(如g418、潮黴素和甲氨喋呤)抗性的那些。在其它方法中可通過藥物篩選鑑別包含被引入核酸的穩定轉染細胞(例如,整合了篩選基因的細胞可存活,而其它細胞則死亡)。
可在提高多肽表達的條件下培養已轉化細胞,可通過常規蛋白純化方法回收多肽。一種該純化方法描述於下文實施例。預用於本文的多肽包括基本同源的重組哺乳動物抗β-klotho受體抗體多肽,其基本不含汙染性內源材料。
適應症
糖尿病尤其是ii型糖尿病及其併發症已經成為全世界日益嚴重的問題。通常,該疾病由胰臟β細胞胰島素生成受損引起。在ii型糖尿病(此疾病最常見的形式)中,人們認為遺傳和環境因素聯合引起β細胞衰竭,使得在人體中引起胰島素分泌和活性受損以及胰島素抵抗。一般認為肥胖症是促使成人甚至兒童中ii型糖尿病增加的病症。
人們還認為血脂異常,或者異常hdl(高密度脂蛋白)和ldl(低密度脂蛋白)均與ii型糖尿病相關。ii型糖尿病的特徵為肌肉和其它器官不能響應正常循環濃度的胰島素。隨後胰臟β細胞分泌胰島素增多,即高胰島素血症的病症。最終β細胞無法再補償,導致葡萄糖耐量降低、空腹葡萄糖濃度受損、慢性高血糖和組織損傷。此外,人們認為早發ii型糖尿病與血脂異常,或者異常hdl(高密度脂蛋白)和ldl(低密度脂蛋白)有關。代謝綜合症患者都表現血脂異常和高血糖症。
本發明提供抗原結合蛋白,尤其是可與人β-klotho受體體內結合、降低動物模型血糖濃度的人類抗體。抗原結合蛋白還可改善葡萄糖耐量。在一個實施方案中,本發明提供具有體內效價的人源化抗體。對ob/ob小鼠單次注射抗體的作用可在注射後數天內降低血糖,為高血糖、ii型糖尿病 以及相關病症提供了有效、持久的治療。單次注射抗體也可改善在下文所述食蟹猴上進行的葡萄糖耐量試驗(gtt)中血樣的葡萄糖清除率(改善葡萄糖耐量)。本發明的抗原結合蛋白,尤其是人類抗體可用於降低血液或血漿葡萄糖,改善葡萄糖耐量降低,改善空腹葡萄糖水平以及改善血脂異常。這樣,本發明的抗原結合蛋白,尤其是人類抗體可用於治療高血糖症、ii型糖尿病、代謝綜合症和包括血脂異常的其它相關症狀。此外,已顯示降低血糖可在某些情況下用於預防和治療具體的癌症例如結腸癌,如richardson等,natureclinpractoncol2:48-53(2005);giovannucci等,gastroenterology132:2208-2225(2007);krone等,integrativecancerther4:25-31(2005);chang等,diabetologia46:595-607(2003);jee等,yonseimedj46:449-55(2005)所述。
本發明提供可與人β-klotho受體特異性結合,改善動物模型ii型糖尿病的抗體。可以明顯改善動物模型的ii型糖尿病的症狀。
治療方法
另一方面,治療受試者的方法,包括給予治療劑量的本發明提供的抗體。在一個實施方案中,抗體為鼠源抗體或人源化抗體。本文中,術語「受試者」指哺乳動物,包括人類,可與術語「患者」交替使用。鼠源抗體或其人源化抗體可用於治療和控制患者體內ii型糖尿病為特點的病症或症狀。術語「治療」包括減輕或預防至少一種症狀或病症的其它方面,或者減輕疾病嚴重性,等等。本發明的抗體不需要產生完全治癒的效果,或根除疾病的所有症狀或表現,即可構成有效治療劑。如相關領域所公認,作為治療劑 的藥物可減少給定疾病狀態的嚴重程度,但不需消除疾病的所有表現即可被認為是有效的治療劑。相似地,預防給藥治療不需在預防症狀出現上完全有效即可構成有效預防劑。只減少疾病的影響(例如,通過減少其症狀的數量或嚴重度,或通過提高另一治療效果,或通過產生另一有效作用),或者減少受試者中疾病發生或加重的可能性就已經足夠。本發明的一個實施方案涉及包含以足以誘導反應具體病症嚴重性的指示劑高於基線水平的持續改善的量和時間給予患者抗體的方法。
給藥劑量和頻率可根據以下因素而改變:給藥途徑、所用具體抗體、所治疾病的性質和嚴重度、症狀為急性還是慢性以及患者的體積和總體症狀。可通過本領域熟知的方法確定適當劑量,例如在臨床試驗中包括劑量放大研究。
本發明抗體可在例如一段時間內按規律間隔給藥一次或多次。在具體實施方案中,在至少一個月或更長時間給藥一次給予鼠源抗體或人源化抗體,例如一個、兩個或三個月或者甚至不確定。對於治療慢性症狀,長期治療通常最有效。但是,對於治療急性症狀,短期給藥例如從一周至六周就已足夠。通常,給予人類抗體直至患者表現出所選體徵或指示劑高於基線水平的醫學相關改善度為止。
本發明方法和組合物的具體實施方案涉及使用例如抗體和一個或多個β-klotho拮抗劑、兩個或更多本發明抗體,或者本發明抗體和一個或更多其它β-klotho拮抗劑。在進一步的實施方案中,單獨或與其它用於治療使患者痛苦的症狀的藥劑組合給予抗體。這些藥劑的實例包括蛋白質以及非 蛋白質藥物。當聯合給予多種藥物時,如本領域所熟知其劑量應相應調整。「聯合給藥」組合療法不限於同時給藥,也包括在涉及給予患者至少一種其它治療劑的療程中至少給予一次抗原和蛋白的治療方案。
另一方面,本發明提供治療ii型糖尿病及相關病症藥用組合物,其包含本發明抗體與藥學可接受輔料中的混合物,用於治療ii型糖尿病的相關病症。藥劑製備方法如上所述。
具體實施例:
1、免疫用抗原細胞穩定株的構建
接種cho-dhfr細胞(中科院細胞庫)至6孔板中,培養24h後轉染含v5-hklb基因的質粒(市售)於6孔板中的細胞,轉染前更換培養液,按照invitrogen公司推薦lipofectamine2000的轉染條件進行轉染。48小時後,再換為含有10nm甲氨碟呤(methotrexate,mtx)的完全培養基,每隔3天換液,待兩周左右,出現穩定生長的克隆,消化分散細胞集落,待長至50%癒合度時,逐漸提高mtx的濃度進行加壓篩選,最高至10um濃度的mtx。構建的穩定細胞株分別進行facs檢測,利用klb蛋白n』-端v5標籤抗體(fitc-anti-v5,invitrogen)鑑定加壓後的細胞群體,篩選後的cho-dhfr-v5-hklb細胞膜上hklb有大量表達,最後經過亞克隆、鑑定獲得2株klb高表達細胞穩定株。
2、抗體的製備
將在弗氏佐劑中乳化的cho-dhfr-v5-hklb全細胞,以2×106細胞/只的劑量皮下注射balb/c小鼠(6-8周齡)。2周後,使用不完全弗氏佐劑 乳化免疫原,加強免疫小鼠,此後每周加強一次。通過剪尾的方式採血,離心分離血清,進行facs檢測血清效價。直至達到適合抗體滴度時,斷頸處死小鼠,無菌狀態下獲取脾臟細胞。收集生長狀態處於對數生長期的sp2/0細胞,2000rpm,3min離心,沉澱用無血清培養至重懸,再次離心-重懸,計數。混合脾臟細胞和sp2/0細胞,保證sp2/0:脾臟細胞≥1:1,共「洗滌-離心」3次。彈散最後一次離心後的沉澱,逐滴加入1ml預溫的peg-1350(30s內滴完),上下吹吸1分鐘,緩慢加入30ml預熱的無血清培養基以終止peg的融合作用,1500rpm,5min離心,彈散細胞沉澱,加入融合培養基,按每孔20000個脾細胞及5000個飼養層細胞鋪於96孔板中,每孔100ul。融合後的雜交瘤細胞和飼養層細胞一起在96孔板中進行培養,並進行hat(次黃嘌呤、氨甲喋呤和胸苷)篩選,以除去非融合的細胞。10天後收取培養板中的雜交瘤細胞上清進行elisa檢測。
3、全細胞elisa篩選
將cho-dhfr-v5-hklb過表達hklb細胞和不表達hklb的cho-dhfr空白細胞分別接種至96孔板,長至90%癒合度。除去細胞培養上清,pbs洗兩遍,加入100ul100%甲醇,4℃固定10min。再加入100ul新鮮配製的0.6%h2o2-pbs,室溫處理20min,用pbs緩衝液洗滌2遍。經過pbs-1%bsa封閉後,加入雜交瘤細胞上清,4℃孵育90min。多次洗滌後,每孔加入100ul稀釋的gxm-hrp-fc二抗(bd,50倍稀釋),37℃孵育0.5h。洗滌5次後,每孔加入100ultmb顯色底物,37℃反應15min,2mh2so4終止,讀取od450值。陽性對照為免疫小鼠的血清;陰性對照 為細胞培養基上清。選取分泌抗hklb抗體的雜交瘤株,進行克隆化以獲得能穩定分泌針對hklb的細胞株。最後選取雜交瘤細胞分泌的抗體上清進行facs驗證。
4、陽性雜交瘤細胞上清流式分析鑑定(facs)
用含10mmedta的pbs消化、收集105個cho-dhfr-v5-hklb細胞,分別加入1.5mlep管,離心後棄上清,陰性對照樣本用流式上樣緩衝液(pbs,2%fbs)重懸。陽性處理組細胞每管加200ul抗體上清,室溫孵育;1500rpm離心,棄上清,用流式上樣緩衝液洗一次,再離心,重懸,加入1:50稀釋的fitc標記的羊抗鼠螢光二抗(bd,200ul/孔),室溫避光孵育30min;離心,棄上清,再用流式上樣緩衝液洗一次,離心,最後用流式上樣緩衝液重懸,上機檢測。如1和圖2所示,雜交瘤細胞上清和表達有klb的cho-dhfr細胞有特異性結合,灰色峰和虛線峰為陰性對照,雜交瘤細胞上清對應的實線峰有明顯右移。
5、抗體基因的克隆及亞克隆
收集分泌抗體的雜交瘤細胞,按照qiagen的mrna抽提試劑盒操作規程,提取雜交瘤細胞的mrna。然後將提取後的mrna反轉錄成cdna,逆轉錄引物為小鼠輕、重鏈恆定區的特異性引物,重鏈逆轉錄引物為(5』-tttggrgggaagatgaagac-3』)(seqidno:36),輕鏈逆轉錄引物為(5』-ttaacactctcccctgttgaa-3』)(seqidno:37)和(5』-ttaacactcattcctgttgaa-3』)(seqidno:38)。rt-pcr的反應條件為:25℃5min;50℃60min;70℃15min。將反轉錄的cdna用0.1mm 的te稀釋至500ul,加入到超濾離心管(amiconultra-0.5)中,2000×g離心10min;棄濾液,再加500ul的0.1mm的te,,2000×g離心10min;棄濾液,將製備管倒置到新的離心管中,2000×g離心10min,得到純化後的cdna;取10ul的純化後的cdna作為模板,加入4ul的5×tailingbuffer(promega),4ul的datp(1mm)和10u的末端轉移酶(promega)後混勻,37℃孵育5min後65℃5min;然後以加上polya尾的cdna為模板,pcr擴增抗體的輕、重鏈可變區基因。上遊引物均為oligodt,重鏈下遊引物為(5』-tggacagggatccagagttcc-3』)(seqidno:39)和(5』-tggacagggctccatagttcc-3』)(seqidno:40),輕鏈下遊引物為(5』-actcgtccttggtcaacgtg-3』)(seqidno:41)。pcr反應條件:95℃5min;95℃30s,56℃30s,72℃1min40cycles;72℃7min;pcr產物連接到pmd18-t載體(takara)後進行測序。克隆的抗體是:a-1,a-2,a-3。
基於已測序得到的抗體的dna序列設計pcr引物,從而將完整輕鏈、重鏈信號肽和可變域以及小鼠igg1恆定區與表達載體(市售)相連。
6.抗體的瞬時表達
接種5×105/ml的懸浮hek293或者cho表達細胞系至轉瓶中,經過24小時37℃,5%co2旋轉培養後,密度達到1×106/ml後被用於轉染。轉染過程中使用polyethylenimine(pei)作為轉染介質,將其與的dna(dna用量為每1×106個細胞0.5ug,其中抗體輕鏈和重鏈的比重為3:2混合,pei和dna的質量混合優選配比為3:1。兩者混合物在靜置孵育15分鐘後被加 入到細胞培養中。細胞在接受pei與dna混合物後繼續37℃,5%co2旋轉培24小時後,向細胞培養液中加入0.5%的胰蛋白腖作為表達需要的胺基酸源,最後在表達完成後(96小時以上)收集細胞上清用於抗體的純化分離。
7、抗體的純化分離
收集的細胞上清經過高速(8000rpm,15分鐘)離心去除細胞以及細胞碎片後,再用0.45um濾膜過濾澄清,澄清後的上清被用於純化。純化過程由層析儀完成。上清首先流過蛋白g親和層析柱,上清中包含的抗體在此期間與蛋白g親和層析柱的配基相結合後被滯留於柱內,然後低ph值(小於等於3.0)的洗脫緩衝液灌洗層析柱解離與層析柱結合的抗體,收集到的抗體洗脫液用1m的tris-hcl迅速中和以保護抗體不變性失活。得到的抗體洗脫液經過16小時的透析後置換成pbs緩衝液。
8、報告基因實驗檢測抗體體外激活人β-klotho/fgfr1c受體複合物的功能。
以每孔20000個接種共表達hklb/fgfr1c-sre-luciferase的cho-dhfr-細胞(在cho-dhfr-hklb細胞的基礎上,採用實例1中的方法轉染fgfr1c和sre-luciferase,潮黴素和g418抗生素篩選亞克隆,建立細胞穩定株)至96孔細胞培養板,37℃培養過夜。第二天除去培養基上清,用無血清培養基清洗細胞表面兩次,吸去殘液,再加入100μl用無血清培養基稀釋純化抗體或fgf21,37℃孵育4小時。刺激結束後,加入100μlpromega的brightglo化學發光底物,最後將細胞裂解物轉移至白色96孔板,在moleculardevices的spectramaxl酶標儀上讀取相對發光強度。 結果表明:重組表達的anti-klb(a-1,a-2,a-3)和fgf21一樣,均可激活人β-klotho/fgfr1c複合受體的功能(圖3)。
9、免疫印跡
以每孔20000個接種共表達hklb/fgfr1c的cho-dhfr-細胞(在cho-dhfr-hklb細胞的基礎上,採用實例1中的方法轉染fgfr1c,潮黴素篩選亞克隆,建立細胞穩定株)至96孔細胞培養板,37℃培養過夜。第二天除去培養基上清,用無血清培養基清洗細胞表面兩次,吸去殘液,無血清中飢餓30分鐘。吸去培養液後,再加入100μl用無血清培養基稀釋純化抗體或fgf21,37℃孵育15分鐘。刺激結束後,加入細胞裂解液(ripa,thermo)裂解細胞,抽取細胞裂解液上清蛋白進行sds-page電泳分離,半乾法轉膜,1%bsa-pbst封閉後的pvdf膜,按照廠家說明書的方法,分別用anti-erk和anti-p-erk抗體(cellsignalingtechnology)進行免疫印跡,曝光後的結果表明:重組表達的anti-klb(a-1,a-2)在10nm的濃度下,均可引起細胞內erk的磷酸化條帶變粗變濃,即刺激後細胞內erk磷酸化水平升高(圖4)。
以上所述的實施例只是本發明的一種較佳的方案,並非對本發明作任何形式上的限制,在不超出權利要求所記載的技術方案的前提下還有其它的變體及改型。
