一種化合物、其製備方法及用途與流程
2023-08-05 01:14:41 1
本發明涉及一種齊墩果型衍生物,尤其涉及一種齊墩果型醯胺類化合物、其製備方法及其用途。
背景技術:
齊墩果酸(Oleanolic acid,簡稱OA)是一種重要的五環三萜化合物,廣泛存在於自然界中,女貞子、青葉膽等植物中均富含齊墩果酸。齊墩果酸具有多種重要的生物活性,如保肝、抗炎、抗腫瘤、降血脂、抗潰瘍等,但大多數活性較弱而沒有實用價值;另外,齊墩果酸的水溶性很差,生物利用度低,這也大大限制了它在臨床上的應用;此外,齊墩果酸還以皂苷的形式廣泛分布在多種植物中,它的許多皂苷也具有重要的藥理作用,如抗腫瘤、降血糖等。
多數中藥成分作為抗腫瘤藥物的前體化合物,需經過適當的結構修飾才能表現出較強的抗腫瘤活性。目前,發現和引入活性關鍵基團是中藥抗腫瘤有效成分結構修飾的主要途徑,也是高效抗腫瘤藥物的研發重點。齊墩果酸類化合物具有獨特的立體結構和手性剛性骨架,衍生化後往往表現出更為優良的生物活性,並且在脂溶性、識別、跨膜能力等方面具有較強的潛在開發價值,將此類化合物修飾後應用於新型藥物分子中必能提高藥物的靶向能力和生物利用度。
近幾年,以齊墩果酸為基礎物質進行結構修飾後形成的一系列衍生物(CDDO-Im、CDDO-Me、AMR、AMR-Me等)受到科研工作者的重視,大量的體內和體外實驗表明,它們具有很強的生物學活性,可以通過多種途徑抑制腫瘤的生長。但是,卻較少有關它們對正常細胞影響的研究。如果此類衍生物能抑制腫瘤的同時對正常細胞產生較小危害,將會大大促進腫瘤治療學的發展。為了實現這一目的,當前最重要的待解決的問題是設計合成一系列新型的齊墩果酸衍生物,並通過細胞活性測試,以期達到高效、低毒、生物利用度及生物活性更好的效果。
技術實現要素:
本發明的目的在於提供一種具有抗癌、抗炎和治療C肝活性的齊墩果型醯胺類化合物。
為實現上述目的,本發明所採取的技術方案為:
一種化合物,其化學結構式如式I所示:
其中,所述R1為氫、C1-C12的烷基中任意一種;所述R2為2-甲基-2-羥基丙基、N,N-二甲基胺乙基、R3-(C=O)-CH2-中任意一種;所述R3選自氨基、C1-C12的直鏈、環狀和支鏈的脂肪胺基、C1-C12的取代或者未取代的芳香胺基、C5-C8的取代或者未取代的氮雜芳基中任意一種。
作為本發明所述化合物的優選實施方式,其中,所述R1為氫、C1-C8的烷基中任意一種;所述R2為2-甲基-2-羥基丙基、N,N-二甲基胺乙基、R3-(C=O)-CH2-中任意一種。
作為本發明所述化合物的更優選的實施方式,其中,所述R1為氫、C1-C4的烷基中任意一種;所述R2為2-甲基-2-羥基丙基、N,N-二甲基胺乙基、R3-(C=O)-CH2-中任意一種。
作為本發明所述化合物的更優選的實施方式,其中,所述R1為氫;所述R3選自氨基,C1-C12的直鏈、環狀和支鏈的脂肪胺基、C1-C12的取代或者未取代的芳香胺基、C5-C8的取代或者未取代的氮雜芳基中任意一種。
作為本發明所述化合物的優選實施方式,其中,所述R3選自氨基、C1-C12的直鏈、環狀和支鏈的脂肪胺基中任意一種。
作為本發明所述化合物的更優選的實施方式,其中,所述R3選自氨基、C1-C4的直鏈、環狀和支鏈的脂肪胺基中任意一種。
作為本發明所述化合物的更優選的實施方式,其中,所述R3選自環丙胺基、異丙胺基、異丁胺基、N,N-二甲基胺基、正丙胺基、正丁胺基、氨基、甲基氨基中任意一種。
在本發明所述化合物的某些實施例中,所述結構式I所示的化合物為下列化合物:
在本發明所述化合物的某些實施例中,所述結構式I所示的化合物為下列化合物:
在本發明所述化合物的某些實施例中,所述結構式I所示的化合物為下列化合物中任意一種:
此外,本發明的目的還在於提供如上所述化合物的合成方法,
為實現上述目的,本發明所採取的技術方案為:
當所述R2為2-甲基-2-羥基丙基或N,N-二甲基胺乙基時,所述方法包括以下步驟:
(1)0℃下,將CDDO用二氯甲烷溶解,向其中加入草醯氯的二氯甲烷溶液;
(2)減壓除去溶劑並除去多餘的草醯氯後,加入二氯甲烷溶解,得到CDDO的醯氯溶液;
(3)用二氯甲烷溶解胺類化合物,向其中加入三乙胺,降溫至0℃,低溫下向其中加入步驟(2)所得到的CDDO的醯氯溶液,常溫下反應,即可;
其中,所述胺類化合物與CDDO的摩爾比為3~5:1;草醯氯與CDDO的摩爾比為5~6:1;所述三乙胺與CDDO的摩爾比為2~3:1。
更為優選地,所述胺類化合物與CDDO的摩爾比為3:1;草醯氯與CDDO的摩爾比為5:1;所述三乙胺與CDDO的摩爾比為2:1。
當所述R2為R3-(C=O)-CH2-時,所述方法包括以下步驟:
(1)0℃下,將如結構式III所示的化合物用二氯甲烷或氯仿溶解;
(2)向步驟(1)所得溶液中加入N,N'-羰基二咪唑(CDI)後反應1~3小時;
(3)將胺類化合物用二氯甲烷溶解後,加入三乙胺,-1至-5℃下加入步驟(2)所得的反應液中,常溫下反應12~18小時,即可製備出入結構式II所示的化合物;
其中,所述胺類化合物與結構式III所示的化合物的摩爾比為3~5:1;N,N'-羰基二咪唑與結構式III所示的化合物的摩爾比為1~2:1;所述三乙胺與結構式III所示的化合物的摩爾比為2~3:1。
更為優選地,所述胺類化合物與結構式III所示的化合物的摩爾比為3:1;N,N'-羰基二咪唑與結構式III所示的化合物的摩爾比為1:1;所述三乙胺與結構式III所示的化合物的摩爾比為2:1。
此外,本發明的目的還在於提供如結構式I所述的化合物的用途。
本發明提供了如結構式I所述化合物在在製備抗癌藥物、抗炎症藥物中的用途;優選地,所述癌症為肝癌、肺癌、喉癌和食道癌;優選地,所述炎症為誘導型一氧化氮合成酶高表達所引發的炎症。
本發明提供了如結構式I所述化合物在製備治療C肝的藥物中的用途。
在下文中,為了表述方便,發明人將上述化學結構式I所示的化合物稱為「齊墩果型醯胺類化合物」。
值得注意的是,發明人經過一系列研究後證實,本發明所述的大多數齊墩果型醯胺類化合物在對癌細胞(例如,肝癌、肺癌、喉癌和食道癌等)的細胞毒性測試中,效果比癌症治療的常用化學藥物順鉑效果好。本發明所述的大多數齊墩果型醯胺類化合物對誘導一氧化氮合成酶(iNOS)的抑制效果與現有的抗炎藥物地塞米松效果相近,但比CDDO-Me效果更好。本發明所述的大多數齊墩果型醯胺類化合物對HCV-RNA聚合酶、HCV蛋白酶的抑制效果與現有的C肝治療藥物索非布韋(sofosbuvir)和雷迪帕韋(ledipasvir)相近,但比CDDO-Me效果更好。
此外,發明人還發現本發明所述的大多數齊墩果型醯胺類化合物對於正常肝細胞和腎細胞的毒性與雷迪帕韋(ledipasvir)相近,但比CDDO-Me小。
因此,本發明所述的齊墩果型醯胺類化合物有望成為新一代的抗癌、抗炎和治療C肝的藥物。
另外,本發明的目的還在於提供一種含有如結構式I所述化合物或其藥學上可接受的鹽的藥物組合物。
與現有技術相比,本發明的技術方案具有以下有益效果:
1、本發明所述的齊墩果型醯胺類化合物是一系列新型的齊墩果型衍生物,以上化合物骨架未見文獻報導。
2、本發明所述的齊墩果型醯胺類化合物在抗癌、抗炎和治療C肝方面具有良好的活性且對正常肝細胞和腎細胞毒性較小,有望成為新一代相關疾病的備選藥物。
附圖說明:
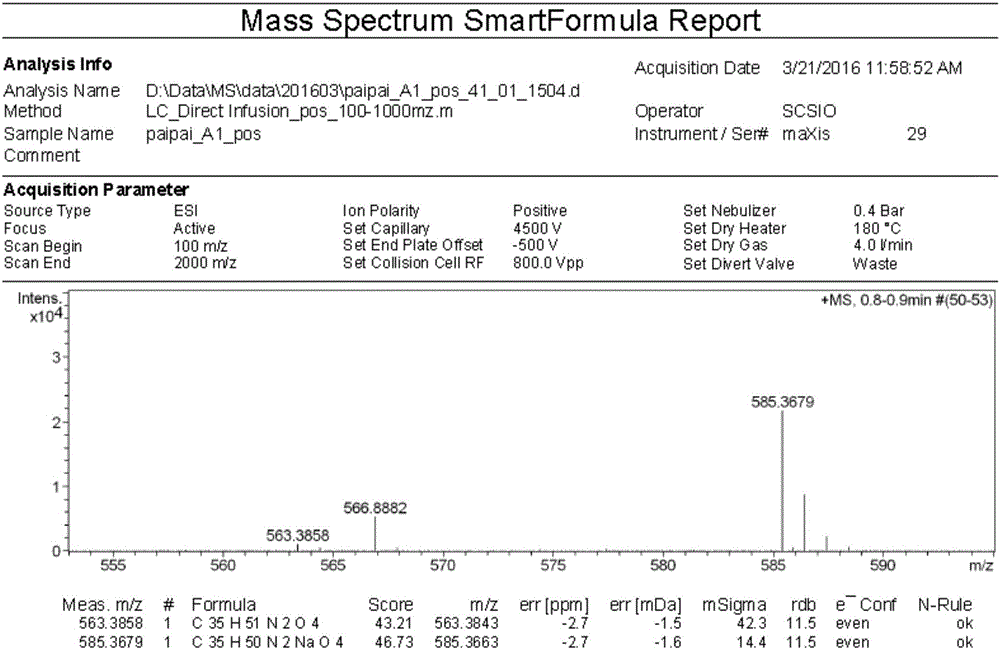
圖1為本發明所述的齊墩果型醯胺類化合物OAH1-1的質譜;
圖2為本發明所述的齊墩果型醯胺類化合物OAH1-1的核磁共振氫譜;
圖3為本發明所述的齊墩果型醯胺類化合物OAH1-1的核磁共振碳譜;
圖4為本發明所述的齊墩果型醯胺類化合物OAH1-2的質譜;
圖5為本發明所述的齊墩果型醯胺類化合物OAH1-2的核磁共振氫譜;
圖6為本發明所述的齊墩果型醯胺類化合物OAH1-2的核磁共振碳譜;
圖7為本發明的化合物OAH2-2的質譜;
圖8為本發明的化合物OAH2-2的核磁共振氫譜;
圖9為本發明的化合物OAH2-2的核磁共振碳譜;
圖10為本發明所述的齊墩果型醯胺類化合物OAH2-5的質譜;
圖11為本發明所述的齊墩果型醯胺類化合物OAH2-5的核磁共振氫譜;
圖12為本發明所述的齊墩果型醯胺類化合物OAH2-5的核磁共振碳譜;
圖13為本發明所述的齊墩果型醯胺類化合物OAH2-6的質譜;
圖14為本發明所述的齊墩果型醯胺類化合物OAH2-6的核磁共振氫譜;
圖15為本發明所述的齊墩果型醯胺類化合物OAH2-6的核磁共振碳譜;
圖16為本發明所述的齊墩果型醯胺類化合物OAH2-7的質譜;
圖17為本發明所述的齊墩果型醯胺類化合物OAH2-7的核磁共振氫譜;
圖18為本發明所述的齊墩果型醯胺類化合物OAH2-7的核磁共振碳譜;
圖19為本發明所述的齊墩果型醯胺類化合物OAH2-8的質譜;
圖20為本發明所述的齊墩果型醯胺類化合物OAH2-8的核磁共振氫譜;
圖21為本發明所述的齊墩果型醯胺類化合物OAH2-8的核磁共振碳譜;
圖22為本發明所述的齊墩果型醯胺類化合物OAH2-9的質譜;
圖23為本發明所述的齊墩果型醯胺類化合物OAH2-9的核磁共振氫譜;
圖24為本發明所述的齊墩果型醯胺類化合物OAH2-9的核磁共振碳譜;
圖25為本發明所述的齊墩果型醯胺類化合物OAH2-10的質譜;
圖26為本發明所述的齊墩果型醯胺類化合物OAH2-10的核磁共振氫譜;
圖27為本發明所述的齊墩果型醯胺類化合物OAH2-10的核磁共振碳譜;
圖28為本發明所述的齊墩果型醯胺類化合物OAH2-11的質譜;
圖29為本發明所述的齊墩果型醯胺類化合物OAH2-12的質譜;
圖30為本發明實施例15的測試原理示意圖。
具體實施方式
為更好的說明本發明的目的、技術方案和優點,下面結合具體實施例對本發明作進一步說明。
在本文中,術語「烷基」應理解為直鏈、環狀、支鏈的烷基。「C1-C12烷基」應理解為表示具有1、2、3、4、5、6、7、8、9、10、11或12個碳原子的直鏈、環狀、支鏈的烷基。例如,甲基、乙基、丙基、異丙基、環丙基、丁基、環丁基、異丁基、環丁基、戊基、環戊基、己基、環己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基或其同分異構體。「C1-C8烷基」應理解為表示具有1、2、3、4、5、6、7或8個碳原子的直鏈、環狀、支鏈的烷基。「C1-C4烷基」應理解為表示具有1、2、3或4個碳原子的直鏈、環狀、支鏈的烷基。
術語「取代的芳香胺基」指指其中的一個氮原子為基團連接部位且其芳基上被C1-C6烷基、C1-C6烷氧基、硝基、腈基、羥基、滷素等單取代或者多取代的芳香胺基。例如,苯胺基、萘胺基等。
術語「氮雜芳基」是指其中的一個氮原子為基團連接部位的五元、六元或多元氮雜芳基。例如,咪唑基、吡唑基、苯並咪唑基等。
一、化合物的合成及表徵
實施例1:
OAH1-1的合成
目的:CDDO和2-甲基-2-羥基丙胺(HA)的醯胺化反應
投料:
註:2-甲基-2-羥基丙胺(HA)自己製備
製備過程:0℃下,0.3gCDDO加10mL二氯甲烷溶解,滴加草醯氯的二氯甲烷溶液,低溫下反應2h;減壓除去溶劑,並除去多餘的草醯氯,並用5mL二氯甲烷溶解,得到CDDO的醯氯溶液,備用;2-甲基-2-羥基丙胺(HA)用10mL無水二氯甲烷溶解,向其中加入三乙胺,降溫至0℃,低溫下將CDDO的醯氯溶液緩慢滴入,常溫反應過夜。反應液經TLC檢測後,水洗,乙酸乙酯萃取,矽膠柱快速柱層析,得到OAH1-1純品。
化合物OAH1-1表徵數據:
1H NMR(500MHz,DMSO-d6)δ8.65(s,1H),7.42(q,J=5.7Hz,4H),6.21(s,1H),5.69(s,2H),4.63–4.42(m,4H),3.21–3.01(m,12H),2.87(d,J=13.9Hz,5H),2.43–2.35(m,3H),2.18(s,2H),1.92(s,4H),1.69(d,J=14.1Hz,7H),1.64–1.56(m,14H),1.42(d,J=15.1Hz,8H),1.24(s,8H),1.19–1.12(m,32H),1.10(d,J=9.2Hz,6H),1.08–1.03(m,35H),0.95(s,10H),0.88(d,J=13.8Hz,24H).13C NMR(126MHz,DMSO-d6)δ199.73,177.60,175.98,168.82,124.04,123.92,70.34,50.57,49.21,49.05,48.51,46.72,46.15,46.10,46.07,45.81,45.50,44.84,43.02,42.02,41.73,38.56,36.06,35.91,34.71,33.68,31.69,31.29,30.70,30.67,28.07,28.05,28.00,27.95,27.81,27.56,26.81,26.61,26.38,25.00,24.14,23.62,23.59,22.55,22.46,21.77,21.54,21.49,19.68,18.76,17.92.
實施例2
OAH1-2的合成
投料:
製備過程:
0℃下,0.3gCDDO加10mL二氯甲烷溶解,滴加草醯氯的二氯甲烷溶液,低溫下反應2h;減壓除去溶劑,並除去多餘的草醯氯,並用5mL二氯甲烷溶解,得到CDDO的醯氯溶液,備用;N,N-二甲基乙二胺用10mL無水二氯甲烷溶解,向其中加入三乙胺,降溫至0℃,低溫下將CDDO的醯氯溶液緩慢滴入,常溫反應過夜。反應液經TLC檢測後,水洗,乙酸乙酯萃取,矽膠柱快速柱層析,得到OAH1-2純品。
化合物OAH1-2表徵數據:
1H NMR(500MHz,DMSO-d6)δ7.63(d,J=5.7Hz,1H),5.68(s,1H),3.39–3.27(m,2H),3.10(dd,J=13.0,6.4Hz,2H),2.85(d,J=13.5Hz,2H),2.44–2.31(m,4H),2.21(d,J=5.1Hz,8H),1.90(d,J=10.4Hz,2H),1.76–1.54(m,9H),1.42(d,J=18.3Hz,3H),1.33–1.24(m,5H),1.23–1.17(m,5H),1.14(d,J=10.2Hz,7H),1.09–1.01(m,6H),0.96(s,2H),0.94(s,3H),0.87(d,J=15.2Hz,9H).13C NMR(126MHz,DMSO-d6)δ176.97,175.94,123.97,78.14,58.74,49.00,48.49,45.91,45.49,45.46,45.43,41.72,38.56,37.15,35.99,34.67,33.73,33.61,31.22,30.73,27.88,27.55,24.12,23.61,23.33,22.40,21.56,19.68,18.79.
實施例3
CDDO-甘氨酸醯胺類的化合物OAH2-5~OAH2-12的合成
通用合成路線:
實施例4
OAH2-2的合成:CDDO和甘氨酸甲酯的醯胺化
投料:
製備過程:0℃下,100mL單口瓶中加入3g CDDO,用30mL二氯甲烷溶解,加入0.9gCDI反應2h;甘氨酸甲酯鹽酸鹽用20mL無水二氯甲烷溶解,加入三乙胺,-1至-5℃下滴入到CDDO的反應溶液中,滴加完畢後常溫反應12~18h。反應液經TLC檢測後,水洗,乙酸乙酯萃取,矽膠柱快速柱層析,得到OAH2-2純品。
化合物OAH2-2表徵數據:
1H NMR(500MHz,DMSO-d6)δ8.65(s,1H),8.16(t,J=5.8Hz,1H),6.20(s,1H),3.90(dd,J=17.0,5.9Hz,1H),3.74(dd,J=17.0,5.6Hz,1H),3.62(s,3H),3.33(s,2H),3.07(d,J=4.7Hz,1H),2.86(dt,J=13.9,4.2Hz,1H),2.51(t,J=1.9Hz,2H),2.30–2.11(m,2H),1.98–1.79(m,5H),1.65(p,J=13.7,13.2Hz,6H),1.42(d,J=17.5Hz,9H),1.35(d,J=10.2Hz,2H),1.27(d,J=14.2Hz,7H),1.18(s,7H),1.08(s,6H),0.95(s,4H),0.88(d,J=16.6Hz,9H).13C NMR(126MHz,DMSO-d6)δ199.68,197.77,177.74,171.07,169.80,168.85,123.79,115.56,113.27,52.06,49.14,46.73,45.88,45.83,44.85,43.03,42.08,41.36,35.82,34.62,33.68,33.58,31.72,31.28,30.68,27.57,26.82,26.61,26.37,25.01,23.59,22.49,21.78,21.61,17.94.
實施例5
OAH2-4的合成:CDDO-甘氨酸甲酯的醯胺化
投料:
製備過程:100mL單口瓶中加入3g OAH2-2,用25mL甲醇溶解,將0.43g NaOH,用3mL水溶解,加入到OAH2-2的甲醇溶液中,室溫下反應2h。經TLC檢測反應完畢後,水洗,乙酸乙酯萃取,矽膠柱快速柱層析,得到OAH2-4純品。
實施例6
OAH2-5~OAH2-12系列化合物的合成:OAH2-4和胺類化合物的醯胺化
投料:
OAH2-5~OAH2-10系列化合物的通用製備過程:
0℃下,50mL單口瓶中加入0.3g OAH2-4,用10mL二氯甲烷溶解,加入0.09gCDI反應2h;amine用5mL無水二氯甲烷溶解,加入三乙胺,-1至-5℃下滴入到OAH2-4的反應溶液中,滴加完畢後常溫反應12~18h。反應液經TLC檢測後,水洗,乙酸乙酯萃取,矽膠柱快速柱層析,得到OAH2系列化合物純品。
實施例7
OAH2-5的合成:OAH2-4和環丙胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②環丙胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-5表徵數據:
1H NMR(500MHz,Chloroform-d)δ8.01(s,1H),6.87(t,J=5.3Hz,1H),6.78(d,J=3.2Hz,1H),5.91(s,1H),3.82(dd,J=8.7,5.1Hz,3H),3.41(s,2H),3.07(s,1H),2.99(d,J=4.7Hz,1H),2.93(s,2H),2.65–2.57(m,1H),1.97(s,2H),1.70(d,J=2.0Hz,6H),1.51(dd,J=22.7,10.2Hz,6H),1.41(s,5H),1.27(d,J=13.6Hz,8H),1.18(s,9H),1.15(d,J=7.4Hz,3H),1.09(s,4H),1.05(d,J=1.5Hz,1H),1.01(s,1H),0.94(d,J=8.2Hz,4H),0.91(s,4H),0.83(s,6H),0.70–0.65(m,3H),0.44(s,3H).13C NMR(126MHz,Chloroform-d)δ199.04,196.63,178.20,170.63,168.65,165.93,143.84,124.00,114.50,114.42,106.58,49.43,47.70,46.52,45.87,45.01,43.32,42.56,42.12,39.58,35.92,34.61,34.08,33.24,31.63,31.55,30.60,29.68,27.75,26.97,26.60,24.73,23.08,22.54,21.66,21.55,18.22,7.22,6.42,6.39.
實施例8
OAH2-6的合成:OAH2-4和一異丙胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②一異丙胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-6表徵數據:
1H NMR(500MHz,Chloroform-d)δ7.99(s,1H),5.92(s,1H),4.04(d,J=47.2Hz,3H),2.96(d,J=12.3Hz,2H),1.99(d,J=19.0Hz,1H),1.67(d,J=40.8Hz,7H),1.52(d,J=13.5Hz,3H),1.41(s,3H),1.36(s,1H),1.28(s,1H),1.27–1.21(m,4H),1.17(d,J=15.1Hz,13H),1.10(s,4H),1.04–0.97(m,1H),0.95(s,3H),0.91(s,3H),0.84(s,4H).13C NMR(126MHz,Chloroform-d)δ198.91,196.55,168.63,165.74,124.08,114.58,114.39,49.46,47.72,46.71,45.85,45.02,42.56,42.09,35.79,34.60,33.98,33.19,31.66,31.36,30.55,27.88,26.99,23.05,22.93,22.11,21.61,21.56,18.23.
實施例9
OAH2-7的合成:OAH2-4和一異丁胺醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②一異丁胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-7表徵數據:
1H NMR(500MHz,Chloroform-d)δ8.03(s,1H),3.07(d,J=84.9Hz,4H),2.05(s,2H),1.74(s,8H),1.59–1.39(m,5H),1.38–1.25(m,4H),1.20(d,J=13.2Hz,7H),1.14–1.05(m,4H),1.05–0.88(m,10H),0.83(d,J=15.3Hz,8H).13C NMR(126MHz,Chloroform-d)δ196.58,166.17,114.66,114.42,48.04,46.69,45.91,45.03,42.75,42.73,42.72,42.28,35.96,34.65,34.43,33.26,32.11,31.65,30.63,29.69,29.65,28.79,28.31,28.24,27.09,23.45,23.18,22.01,21.70,21.08,18.37.
實施例10
OAH2-8的合成:OAH2-4和二甲胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②二甲胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-8表徵數據:
1H NMR(500MHz,Chloroform-d)δ8.07(s,1H),5.97(s,1H),4.12(q,J=21.3,19.6Hz,2H),3.22–2.91(m,8H),2.06(dd,J=27.3,14.1Hz,1H),1.84(td,J=13.6,4.5Hz,2H),1.77(s,3H),1.70(dd,J=14.5,6.4Hz,1H),1.61(t,J=11.1Hz,3H),1.53(d,J=12.4Hz,2H),1.48(s,3H),1.31(s,5H),1.28(s,1H),1.25(d,J=2.8Hz,5H),1.23(s,2H),1.18(s,1H),1.16(d,J=1.8Hz,3H),1.08(dd,J=20.3,11.9Hz,1H),1.01(d,J=8.6Hz,6H),0.90(s,4H).13C NMR(126MHz,Chloroform-d)δ198.96,196.64,168.25,165.95,124.03,114.41,49.34,47.70,46.46,45.82,44.99,42.52,42.14,40.91,35.89,34.65,34.04,33.25,31.62,31.46,30.59,29.67,27.81,26.97,26.59,24.72,23.24,23.09,21.61,21.55,18.23.
實施例11
OAH2-9的合成:OAH2-4和一正丙胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②一正丙胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-9表徵數據:
1H NMR(500MHz,Chloroform-d)δ8.07(s,1H),6.05(s,1H),3.33(s,3H),3.05(s,2H),2.08(d,J=21.2Hz,2H),1.80(s,8H),1.73(d,J=7.5Hz,3H),1.66(s,5H),1.60(d,J=12.4Hz,10H),1.44(s,4H),1.38(s,3H),1.35(s,2H),1.28(d,J=6.3Hz,16H),1.20(d,J=8.9Hz,8H),1.13(s,3H),1.05(s,4H),0.97(d,J=21.1Hz,10H),0.94–0.81(m,10H).13C NMR(126MHz,Chloroform-d)δ199.00,196.55,168.88,165.84,114.61,114.40,47.78,46.77,45.95,45.02,42.61,42.10,35.79,34.59,34.04,33.19,31.76,31.41,30.55,29.69,28.00,27.03,26.91,23.07,22.95,22.38,21.70,21.61,18.27,11.63.
實施例12
OAH2-10的合成:OAH2-4和一正丁胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②一正丁胺用15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
化合物OAH2-10表徵數據:
1H NMR(500MHz,Chloroform-d)δ8.00(s,1H),5.92(s,1H),4.21–3.95(m,2H),3.22(d,J=14.5Hz,2H),2.96(d,J=10.3Hz,2H),1.99(d,J=16.4Hz,1H),1.71(s,5H),1.67–1.57(m,3H),1.56–1.44(m,6H),1.42(s,3H),1.36(s,1H),1.29(s,3H),1.26(s,1H),1.22(d,J=6.9Hz,3H),1.19(s,9H),1.12(s,1H),1.10(s,3H),1.08–0.99(m,2H),0.95(s,3H),0.91(s,3H),0.84(d,J=8.8Hz,8H),0.79–0.74(m,1H).13C NMR(126MHz,Chloroform-d)δ196.55,168.59,165.75,124.06,114.57,114.40,49.46,47.70,46.69,45.83,45.01,43.32,42.55,42.07,40.40,35.78,34.60,33.97,33.18,31.65,31.39,31.00,30.54,29.69,27.86,26.99,24.72,23.03,22.92,21.60,21.56,20.03,18.22,13.69.
實施例13
OAH2-11的合成:OAH2-4和一正丁胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②足量NH3通入到15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
實施例14
OAH2-12的合成:OAH2-4和一正丁胺的醯胺化
投料:
製備過程:
②0℃,OAH2-4加10mL二氯甲烷溶解,加CDI反應2h;
②足量CH3NH2通入到15mL無水二氯甲烷溶解,降溫至0℃,加入三乙胺,-1至-5℃下將①中溶液緩慢滴入,常溫反應過夜。
二、化合物的生物活性測試
實施例15
抑制誘導一氧化氮合成酶(iNOS)活性檢測,抗炎活性測試:
表1:對誘導一氧化碳合成酶(iNOS)半數抑制率IC50的結果
實驗原理:
應用雙抗體夾心法測定標本中一氧化氮合成酶(iNOS)水平。用純化的一氧化氮合成酶(NOS)抗體包被微孔板,製成固相抗體,往包被單抗的微孔中依次加入一氧化氮合成酶(NOS),再與HRP標記的一氧化氮合成酶(NOS)抗體結合,形成抗體-抗原-酶標抗體複合物,經過徹底洗滌後加底物TMB顯色。TMB在HRP酶的催化下轉化成藍色,並在酸的作用下轉化成最終的黃色。顏色的深淺和樣品中的一氧化氮合成酶(NOS)呈正相關。用酶標儀在450nm波長下測定吸光度(OD值),通過標準曲線計算樣品中人一氧化氮合成酶(NOS)濃度。
試劑及材料:
小鼠Raw-264.7細胞株;細胞消化液(胰酶0.25%;EDTA 0.02%);LPS(10ug/mL);10%的胎牛血清;1%雙抗(青黴素、鏈黴素)的DMEM(Gbico)培養基;測試化合物;地塞米松;96孔板;多功能酶標儀;細胞培養箱;柏奧萊博小鼠iNOS酶聯免疫分析(ELISA)檢測試劑盒。
實驗步驟:
(1)、取處於對數生長期的Raw-264.7細胞用細胞消化液進行消化、離心,重懸後按照每孔100μL,細胞數6×104接種於96孔板中,37℃、5%CO2的細胞培養箱中培養。留3孔作為沒有細胞的空白對照;
(2)、培養12~48h至細胞為80~90%滿後吸除原培養液,加入不含血清的DMEM培養基90μL,再加入LPS(10ug/mL)10μL,即最終濃度為1μg/mL,然後放入培養箱中37℃繼續培養24h;
(3)、用少量DMSO溶解的測試化合物、CDDO-Me、地塞米松樣品(儲存液濃度10mM/L)樣品加無血清培養基序列稀釋9個濃度梯度100、50、25、12.5、6.25、3.13、1.56、0.78、0.39μM/L,每孔100μL加入到前述培養液中繼續培養4~6h;
(4)、標準品的稀釋與加樣:在酶標包被板上設標準品孔10孔,每孔加樣量都為50μL,濃度分別為60U/L,40U/L,20U/L,10U/L,5U/L,2個復孔;
(5)、加樣:分別設空白對照孔(空白對照孔不加樣品及酶標試劑,其餘各步操作相同)、待測樣品孔。在酶標包被板上待測樣品孔中先加樣品稀釋液40μL,然後再加待測樣品液10μL(樣品最終稀釋度為5倍);
(6)、溫育:用封板膜封板後置37℃溫育30分鐘;
(7)、配液:將30(48T的20倍)倍濃縮洗滌液用蒸餾水30倍稀釋後製成洗滌液備用;
(8)、洗滌:小心揭掉封板膜,棄去液體,甩幹,每孔加滿洗滌液,靜置30秒後棄去,如此重複5次,拍幹;
(9)、加酶:每孔加入酶標試劑50μL,空白孔除外;
(10)、溫育:操作同(3);洗滌:操作同(5);
(11)、顯色:每孔先加入顯色劑A 50μL,再加入顯色劑B 50μL,輕輕震蕩混勻,37℃避光顯色15分鐘;
(12)、終止:每孔加終止液50μL,終止反應(此時藍色立轉黃色);
(13)、測定:以空白空調零,450nm波長依序測量各孔的吸光度(OD值)。測定應在加終止液後15min以內進行。
實施例16
測試齊墩果型醯胺類化合物和sofosbuvir(陽性對照物)的HCV-RNA聚合酶IC50,結果如下表2:
表2
測試原理:
RNA多聚化合成過程中,焦磷酸(PPi)被釋放出來:(RNA)n+NTP→(RNA)n+1+PPi。在焦磷酸酶的催化作用下,PPi被轉化成Pi。Pi和MESG酶促反應後產物在360nm處具有最大吸收峰。
試劑及材料:
HCV-RNA聚合酶NS5B(Prospec Cat#HCV-269);焦磷酸鹽活性檢測試劑盒(AnaSpec Cat#E-6645);sofosbuvir(Gilead Cat#HY-15005);測試化合物;CDDO-Me
實驗步驟:
(1)、加入20mL去離子水至MESG酶底物(Component A)中,製成1mM的儲存液,分裝後儲存於-20℃冰箱中;用前將分裝好凍存的MESG酶底物儲存液放入37℃快速溶解(不超過5min),渦旋震蕩,放於冰上。
(2)、加入0.2mL去離子水至無機焦磷酸酶(Component E)中,製成30U/mL的儲存液,4℃保存。
(3)、加入0.5mL去離子水至嘌呤核酸磷酸化酶(Component B)中,製成100U/mL的儲存液,4℃保存。
(4)、添加100μL RNA聚合反應緩衝液(20mM Hepes,pH 7.1,7.5mM DTT,60mMNacl,100μg/mL BSA,20U/mL RNAsin,50μg/mL Poly C,5μg/mL Oligo G12,10μM GTP)和HCV-RNA聚合酶NS5B(500μg/mL),30℃孵育1h。
(5)、添加23μL去離子水至新的96孔板中,然後依次加入5μL 20×反應緩衝液(Component C),20μL MESG酶底物儲存液,1μL嘌呤核酸磷酸化酶儲存液,1μL無機焦磷酸酶儲存液,22℃孵育10min。
(6)、吸取步驟4反應液50μL添加至步驟5的96孔板中,混合均勻後22℃孵育30~60min。
(7)、在酶標儀上讀取360nm吸光值。
實施例17
測試齊墩果型醯胺類化合物和ledipasvir(陽性對照)的HCV蛋白酶體的IC50,結果如下表3:
表3
測試原理:
HCV NS3-4A蛋白酶可以在多個位點如NS3-4A,NS4A-4B,NS4B-5A和NS5A-5B處切割病毒的非結構多肽產物,而這些切割對於C肝病毒蛋白的成熟是必不可少的。螢光能量共振轉移(FRET)肽序列含有NS4A-4B切割位點。在HCV NS3-4A蛋白酶作用下,FRET肽被切為EDANS/DABCYL兩段,致使被DABCYL淬火的EDANS螢光得以恢復(參見圖30)。通過檢測ex/em=340nm/490nm螢光強度的變化,可以檢測HCV NS3-4A蛋白酶活性。
試劑及材料:
HCV NS3-4A蛋白酶(AnaSpec Cat#61017);HCV蛋白酶活性檢測試劑盒(AnaSpec Cat#AS-72087);ledipasvir(Gilead Cat#HY-15602);測試化合物;CDDO-Me
實驗步驟:
(1)、製備分析緩衝液:添加5mL 2×分析緩衝液(Component C)和300μL DTT(Component E)至4.7mL去離子水,製成10mL 1×分析緩衝液。
(2)、添加100μL HCV NS3-4A蛋白酶底物(50×,ComponentA)至4.9mL1×分析緩衝液中,製成5mL HCV NS3-4A蛋白酶底物溶解液。
(3)、用DMSO溶解的測試化合物、CDDO-Me、ledipasvir(儲存液濃度10mM/L)加無血清培養基序列稀釋9個濃度梯度100、50、25、12.5、6.25、3.13、1.56、0.78、0.39uM/L,每孔40μL加入到96孔板,再加入10μL HCV NS3-4A蛋白酶至上述稀釋液中,使其終濃度為20ng/孔,37℃孵育10~15min;同時設置HCV NS3-4A蛋白酶陽性對照、HCV NS3-4A蛋白酶底物對照。
(4)、加入50μL HCV NS3-4A蛋白酶底物溶解液至前述稀釋液中,室溫下輕輕震蕩30~60min混勻。
(5)、避光加入50μL終止液(Component D)後,用螢光酶標儀檢測ex/em=340nm/490nm螢光強度的變化。
實施例18
測試齊墩果型醯胺類化合物和順鉑(陽性對照)對癌細胞IC50
肝癌(HepG-2/Huh7),肺癌(A549),喉癌(Hep2),食道癌(Eca-109/K450/510/TE-1)
表4
實驗原理:
MTT廣泛應用於細胞增殖和細胞毒性的檢測。MTT為黃色化合物,是一種接受氫離子的燃料,可以被線粒體內的一些脫氫酶還原成結晶狀的深紫色產物formazan,在特定溶劑存在的情況下,可以被完全溶解。該產物在570nm處具有最大吸收峰。細胞增殖越多越快,則吸光度越高;細胞毒性越大,則吸光度越低。
測試材料:
肝癌(HepG-2/Huh7),肺癌(A549),喉癌(Hep2),食道癌(Eca-109/K450/510/TE-1)等呼吸和消化系統癌為主的癌細胞細胞株;10%的胎牛血清;1%雙抗(青黴素、鏈黴素)的DMEM(Gbico)培養基;細胞消化液(胰酶0.25%;EDTA0.02%);1%雙抗(青黴素、鏈黴素)的DMEM(Gbico)培養基;測試化合物(A1/A4/OAH2-1/OAH2-1-C/OAH2-2/OAH2-2-C);CDDO-Me;ledipasvir(Gilead Cat#HY-15602);96孔板;多功能酶標儀;細胞培養箱。
實驗步驟:
(1)鋪板:培養瓶內生長良好的肝癌,肺癌,胃癌,食道癌等呼吸和消化系統癌為主的癌細胞細胞株長至80%左右時用細胞消化液消化,細胞以6000個/孔、100μL/孔鋪於96孔板,放置於37℃、5%CO2培養箱培養過夜至貼壁。
(2)加藥。用少量DMSO溶解的測試化合物/B類化合物、CDDO-Me、地塞米松樣品(儲存液濃度10mM/L)樣品加無血清培養基序列稀釋9個濃度梯度,加藥濃度分別為100、50、25、12.5、6.25、3.13、1.56、0.78、0.39uM/L,設置一組DMSO、細胞以及空白對照組,每組5個復孔。將96孔板原培養基棄去,加入不同濃度梯度的測試化合物,DMSO以及空白培養基。放置於培養箱培養過夜。
(3)加MTT。加藥24小時後,96孔板每孔加10μL MTT(5mg/mL)。後用錫箔紙包好放培養箱培養4小時。
(4)加DMSO。加MTT4小時後,將96孔板中培養基小心吸出棄去,後每孔加入100μL DMSO。加完DMSO後,將96孔板包好放於搖床搖10分鐘左右後於酶標儀570-630nm波長進行測板。
(5)空白組只含有培養基,對照組是正常培養的細胞組。抑制率=(實驗組A570nm-空白組A570nm)/(對照A570nm-空白組A570nm)。
實施例19
測試齊墩果型醯胺類化合物和Ledipasvir(陽性對照)對肝細胞株(LO-2/HL-7702)和腎細胞株(293T/HK-2)IC50。
表5
實驗原理:
MTT廣泛應用於細胞增殖和細胞毒性的檢測。MTT為黃色化合物,是一種接受氫離子的燃料,可以被線粒體內的一些脫氫酶還原成結晶狀的深紫色產物formazan,在特定溶劑存在的情況下,可以被完全溶解。該產物在570nm處具有最大吸收峰。細胞增殖越多越快,則吸光度越高;細胞毒性越大,則吸光度越低。
試劑及材料:
肝細胞(LO-2/HL-7702)和腎細胞株(293T/HK-2);10%的南美/胎牛血清;細胞消化液(胰酶0.25%;EDTA0.02%);1%雙抗(青黴素、鏈黴素)的1640/DMEM(Gbico)培養基;測試化合物;CDDO-Me;ledipasvir(Gilead Cat#HY-15602);96孔板;多功能酶標儀;細胞培養箱。
實驗步驟:
(1)鋪板:培養瓶內生長良好的肝或腎細胞長至80%左右時用細胞消化液消化,細胞以4000個/孔、200μL/孔鋪於96孔板,放置於37℃、5%CO2培養箱培養過夜至貼壁。
(2)加藥。用少量DMSO溶解的測試化合物、CDDO-Me、地塞米松樣品(儲存液濃度10mM/L)樣品加無血清培養基序列稀釋10個濃度梯度,加藥濃度分別為200、100、50、25、12.5、6.25、3.13、1.56、0.78、0.39μM/L,設置一組乙酸乙酯組(濃度為20μL/mL)以及空白對照組,每組四個復孔。將96孔板原培養基棄去,加入不同濃度梯度的測試化合物,乙酸乙酯以及空白培養基。放置於培養箱培養過夜。
(3)加MTT。加藥24小時後,96孔板每孔加10μL MTT。後用錫箔紙包好放培養箱培養4小時。
(4)加DMSO。加MTT 4小時後,將96孔板中培養基小心吸出棄去,後每孔加入100μL DMSO。加完DMSO後,將96孔板包好放於搖床搖10分鐘左右後於酶標儀570nm波長進行測板。
(5)空白組只含有培養基,對照組是正常培養的細胞組。抑制率=(實驗組A570nm-空白組A570nm)/(對照A570nm-空白組A570nm)
最後所應當說明的是,以上實施例僅用以說明本發明的技術方案而非對本發明保護範圍的限制,儘管參照較佳實施例對本發明作了詳細說明,本領域的普通技術人員應當理解,可以對本發明的技術方案進行修改或者等同替換,而不脫離本發明技術方案的實質和範圍。
