一種製備鋇長石微晶玻璃的方法和系統與流程
2023-07-27 04:04:31 1
本發明涉及微晶玻璃材料領域,具體地,涉及一種製備鋇長石微晶玻璃的方法和系統。
背景技術:
鋇長石微晶玻璃具有高耐熱溫度、高機械強度、較好的抗氧化抗鹼侵蝕性及高的化學穩定性等優點,其廣泛應用於反射鏡用基體材料,集成電路基板材料,液晶顯示器等領域,一般採用燒結法製備,需先將含bao、al2o3、sio2的原料加熱至1600℃-1800℃的高溫,才能使原料熔融,再水萃、燒結製備微晶玻璃,該熔融溫度容易造成組分的揮發,對發熱體及耐火材料要求極高,大幅提高了生產成本。
技術實現要素:
本發明旨在提供一種採用金屬al粉及kmno4促進原料熔融以製備鋇長石微晶玻璃的新方法,降低原料熔融時的溫度,解決現有技術存在的不足。
本發明提出的促進原料熔融以製備鋇長石微晶玻璃材料的方法,其中,包括如下步驟:
步驟1:將bao、sio2、al2o3、b2o3、zro2混合均勻,製得混合料;
步驟2:將所述混合料加熱至熔融,製得熔融料;
步驟3:將kmno4及al粉混合均勻後加入到所述熔融料中,並攪拌均勻;
步驟4:對步驟3得到的熔融原料進行水萃、燒結以製備鋇長石微晶玻璃;
所述al2o3的用量≤原料總重量的10%。
優選地,所述bao的用量為29-39重量份,所述sio2的用量為25-36重量份,所述al2o3的用量為3-7重量份,所述b2o3的用量為4-6重量份,所述zro2的用量為1-2重量份,所述kmno4的用量為15-25重量份,所述al粉的用量為5-10重量份。
優選地,步驟3中,將kmno4及al粉混合均勻後按每次0.5-1.5重量份的投入量分次加入到所述熔融料中。
優選地,步驟2中,在1430℃-1480℃的溫度下加熱至熔融。
本發明還提供了一種利用上述方法製備鋇長石微晶玻璃的系統,包括:
第一混料機,設有bao入口、sio2入口、al2o3入口、b2o3入口、zro2入口和第一混合料出口;
熔化池,設有第一混合料入口和熔融料出口,所述第一混合料入口與所述第一混料機的第一混合料出口相連;
第二混料機,設有kmno4入口、al粉入口和第二混合料出口;
均化池,設有熔融料入口、第二混合料入口和熔融原料出口,所述熔融料入口與所述熔化池的熔融料出口相連,所述第二混合料入口與所述第二混料機的第二混合料出口相連;
水萃池,設有熔融原料入口和水萃料出口,所述熔融原料入口與所述均化池的熔融原料出口相連;
梭式窯,設有水萃料入口和鋇長石微晶玻璃出口,所述水萃料入口與所述水萃池的水萃料出口相連。
本發明通過加入al粉及kmno4兩種物質,部分替代了傳統方法中的鋁源、助熔劑及澄清劑,能有效改善原料的熔融效果。
附圖說明
圖1為本發明實施例中的一種製備鋇長石微晶玻璃的工藝流程圖。
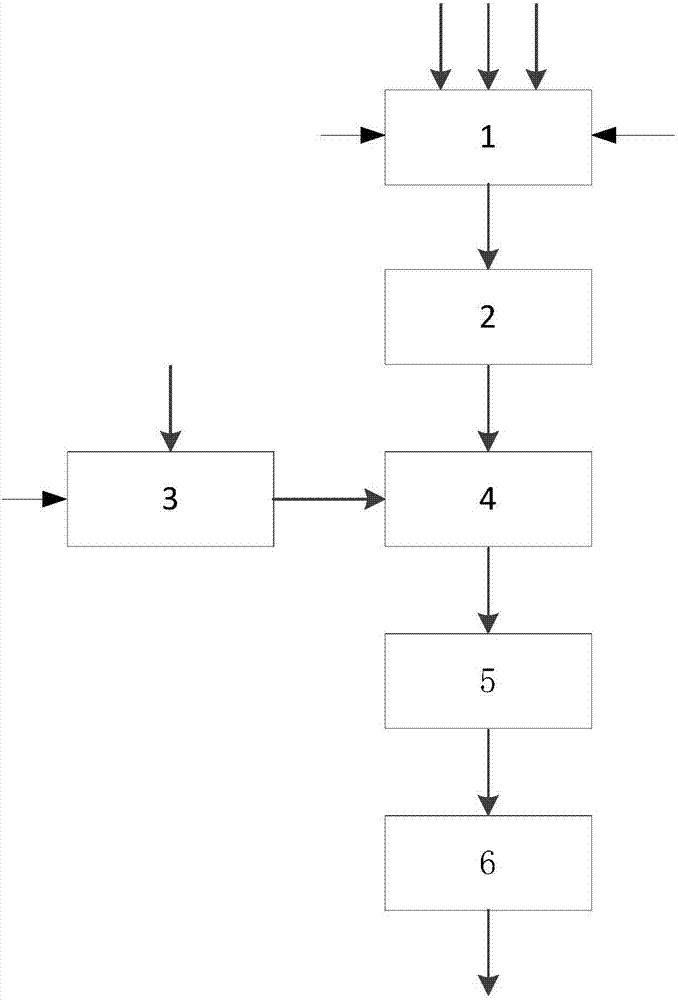
圖2為本發明實施例中的一種製備鋇長石微晶玻璃的系統的結構示意圖。
具體實施方式
以下結合附圖和實施例,對本發明的具體實施方式進行更加詳細的說明,以便能夠更好地理解本發明的方案以及其各個方面的優點。然而,以下描述的具體實施方式和實施例僅是說明的目的,而不是對本發明的限制。
根據bao-al2o3-sio2三元相圖,在bao/sio2的質量比為1.28左右(即鋇長石baal2si2o8中bao/sio2的理想質量比)時,發明人經過大量實驗,研究得出al2o3的含量在10wt%(質量百分含量)以下,則三元系的低共熔點溫度在1400℃以下,此時原料易熔融,而當al2o3含量從10wt%增加至20wt%左右時,三元系的低共熔點溫度快速增加至1600℃,可見al2o3的含量是影響鋇長石微晶玻璃原料熔融溫度的重要因素。因此,若能在熔融前期少配入al2o3,以降低熔融溫度,然後在熔融後期加入鋁源並使熔池自發升溫,則必能降低能耗成本並降低耐火材料對熔池的汙染。
根據上述研究工作,發明人提出了如下的促進原料熔融以製備鋇長石微晶玻璃材料的方法,包括如下步驟:
步驟1:將bao、sio2、al2o3、b2o3、zro2混合均勻,製得混合料;
步驟2:將混合料加熱至熔融,製得熔融料;
步驟3:將kmno4及al粉混合均勻後加入到熔融料中,並攪拌均勻;
步驟4:對步驟3得到的熔融原料進行水萃、燒結以製備鋇長石微晶玻璃。
上述步驟中,al2o3的用量≤原料總重量的10%。
原料熔融完成後,即可進行水萃、燒結等工序以製備鋇長石微晶玻璃。
在原料熔融前期,加入bao、sio2、助熔劑及晶核劑時,只配入少量al2o3(配入量不要高於10wt%),使原料在相對低溫段充分熔融。在本發明優選的實施例中,步驟2中,在1430℃-1480℃的溫度下即可將混合料加熱至熔融。
在原料熔融後期採用kmno4及金屬al粉混勻投入熔池,可起到補充剩餘al2o3、提供助熔劑、澄清劑及晶核劑的多重作用。kmno4為強氧化劑、金屬al為強還原劑、二者將發生一系列複雜的分解、氧化、還原反應,kmno4分解為k2mno4、mno2及o2,k2mno4分解為k2o、mno及o2,金屬al被o2氧化生成al2o3,金屬al被mno2氧化生成mn及al2o3,金屬mn被過量o2氧化生成mno等,最終生成物為al2o3、k2o、mno及o2,反應伴隨大量放熱。生成的al2o3將作為鋇長石微晶玻璃的鋁源;生成的k2o將作為原料的助熔劑;生成的mno將作為晶核劑;生成的o2起到使原料混合均勻,加速原料中微小氣泡上浮的作用;反應顯熱將使熔池溫度顯著提升,加速原料的熔融均化。
kmno4與al粉的反應很強烈,務必保證熔液面平靜後再開始下次投料,投料完畢後熔池溫度將上升100-150℃左右,之後對熔池進行攪拌。攪拌的時間越長,原料越均勻,在本發明優選的實施例中,攪拌時間為1-3小時。
bao、sio2、al2o3、b2o3、zro2、kmno4及al粉的用量直接影響最終製備的鋇長石微晶玻璃的質量,在本發明優選的實施例中,bao的用量為29-39重量份,sio2的用量為25-36重量份,al2o3的用量為3-7重量份,b2o3的用量為4-6重量份,zro2的用量為1-2重量份,kmno4的用量為15-25重量份,al粉的用量為5-10重量份。
如上所述,kmno4與al粉的反應很強烈,需要分批次投入,在本發明優選的實施例中,步驟3中,將kmno4及al粉混合均勻後按每次0.5-1.5重量份的投入量分次加入到熔融料中。
原料的粒徑越小,熔融過程越短,在本發明優選的實施例中,所有原料的粒徑均≤74微米。
如圖2所示,本發明提供的利用上述方法製備鋇長石微晶玻璃的系統包括:第一混料機1、熔化池2、第二混料機3、均化池4、水萃池5和梭式窯6。
第一混料機1,設有bao入口、sio2入口、al2o3入口、b2o3入口、zro2入口和第一混合料出口。bao、sio2、al2o3、b2o3、zro2在第一混料機1混合均勻後再進入熔化池2進行熔融。
熔化池2,設有第一混合料入口和熔融料出口,第一混合料入口與第一混料機1的第一混合料出口相連。
第二混料機3,設有kmno4入口、al粉入口和第二混合料出口。
均化池4,設有熔融料入口、第二混合料入口和熔融原料出口,熔融料入口與熔化池2的熔融料出口相連,第二混合料入口與第二混料機3的第二混合料出口相連。
熔融後的bao、sio2、al2o3、b2o3、zro2與kmno4及al粉的混合料混合均勻,即得熔融原料。熔融原料進行水萃、燒結後就可製得鋇長石微晶玻璃。
水萃池5,設有熔融原料入口和水萃料出口,熔融原料入口與均化池4的熔融原料出口相連。
梭式窯6,設有水萃料入口和鋇長石微晶玻璃出口,水萃料入口與水萃池5的水萃料出口相連。
下面參考具體實施例,對本發明進行說明。下述實施例中所取工藝條件數值均為示例性的,其可取數值範圍如前述發明內容中所示。下述實施例所用的檢測方法均為本行業常規的檢測方法。
實施例1
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,29重量份的bao、25重量份的sio2、3重量份的al2o3、4重量份的b2o3、1重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1450℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將7重量份的金屬al粉與15重量份的kmno4混合均勻,獲得23重量份的混合粉。在步驟s104,按每次1重量份的標準分批次將23重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為2小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1250℃,燒結時間3小時),即可製得鋇長石微晶玻璃。
實施例2
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,31重量份的bao、29重量份的sio2、5重量份的al2o3、5重量份的b2o3、1.5重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1460℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將8重量份的金屬al粉與18重量份的kmno4混合均勻,獲得26重量份的混合粉。在步驟s104,按每次1重量份的標準分批次將26重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為1小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1270℃,燒結時間3.5小時),即可製得鋇長石微晶玻璃。
實施例3
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,33重量份的bao、30重量份的sio2、5重量份的al2o3、6重量份的b2o3、2重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1470℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將9重量份的金屬al粉與18重量份的kmno4混合均勻,獲得27重量份的混合粉。在步驟s104,按每次1重量份的標準分批次將27重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為3小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1230℃,燒結時間2小時),即可製得鋇長石微晶玻璃。
實施例4
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,35重量份的bao、32重量份的sio2、5重量份的al2o3、6重量份的b2o3、2重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1470℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將10重量份的金屬al粉與24重量份的kmno4混合均勻,獲得34重量份的混合粉。在步驟s104,按每次0.5重量份的標準分批次將34重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為2.5小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1280℃,燒結時間3小時),即可製得鋇長石微晶玻璃。
實施例5
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,39重量份的bao、33重量份的sio2、6重量份的al2o3、5重量份的b2o3、2重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1480℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將10重量份的金屬al粉與25重量份的kmno4混合均勻,獲得35重量份的混合粉。在步驟s104,按每次1重量份的標準分批次將35重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為1.5小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1260℃,燒結時間2.5小時),即可製得鋇長石微晶玻璃。
實施例6
本實施例中,所有原料的粒徑均≤74微米。
參考圖1,在步驟s101中,35重量份的bao、36重量份的sio2、7重量份的al2o3、6重量份的b2o3、2重量份的zro2混合均勻,獲得混合料。隨後在步驟s102中,將上述混合料在1470℃下熔融2個小時,混合料被充分熔融,獲得熔融料。接著在步驟s103,將5重量份的金屬al粉與24重量份的kmno4混合均勻,獲得33重量份的混合粉。在步驟s104,按每次1.5重量份的標準分批次將33重量份的混合粉投入熔池內部。金屬al粉與kmno4粉末發生強烈的氧化還原反應,待投料完畢後,對熔池進行緩慢攪拌促進原料均化,攪拌時間為2.2小時。對步驟s104得到的成品進行依次步驟s200的水萃、步驟s300的燒結(燒結溫度1230℃,燒結時間3小時),即可製得鋇長石微晶玻璃。
綜上,本發明通過加入al粉及kmno4兩種物質,部分替代了傳統方法中的鋁源、助熔劑及澄清劑,能有效改善原料的熔融效果。
顯然,上述實施例僅僅是為清楚地說明本發明所作的舉例,而並非對實施方式的限定。對於所屬領域的普通技術人員來說,在上述說明的基礎上還可以做出其它不同形式的變化或變動。這裡無需也無法對所有的實施方式予以窮舉。而由此所引申出的顯而易見的變化或變動仍處於本發明的保護範圍之中。
