聚合方法和由其形成的聚合物與流程
2023-06-09 20:12:16 2
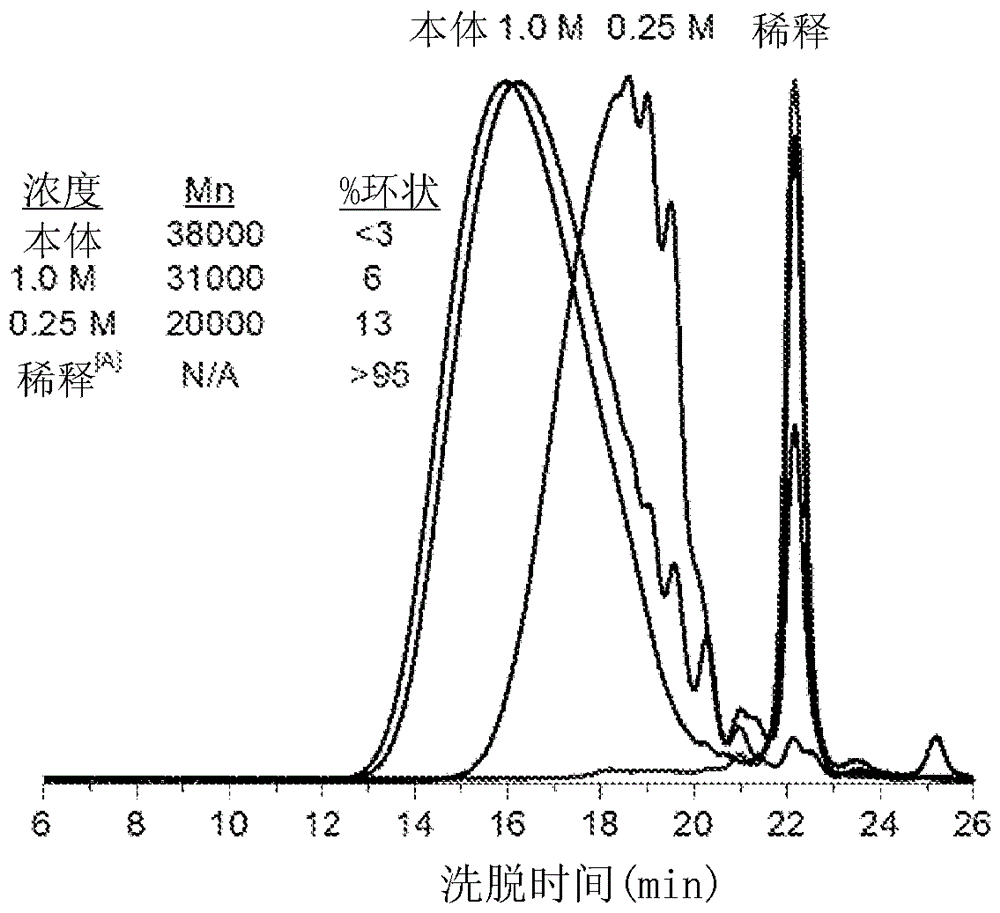
聚合方法和由其形成的聚合物對相關申請的交叉引用本申請要求2012年12月3日提交的美國臨時申請序號No.61/732,727的權益,其全文經此引用併入本文。政府資助在來自國家衛生研究院(NationalInstitutesofHealth),GrantNo.GM-087620和國家科學基金會(NationalScienceFoundation),GrantNo.CHE-0848982的政府資助下作出本發明。美國政府對本發明享有某些權利。發明領域本發明涉及聚合物和製造聚合物的方法。更具體而言,本發明涉及通過氟化和甲矽烷基化單體在鹼性催化劑存在下的縮合製造聚合物的方法,和可通過該方法獲得的聚合物。背景聚合材料在現代材料科學中起到重要作用。合成縮聚物(例如具有有機碸、有機硫酸酯、有機碳酸酯、有機氨基甲酸酯、有機脲或有機酯型聚合骨架的材料)用於各種產品和工業,包括例如包裝、高性能工程材料、醫療假體和植入物、光學器件和消費塑料製品。仍然需要製備聚合材料,特別是固體聚合物(例如塑料),包括用於高價值特種用途的材料(例如醫療假體和植入物、工程材料和光學器件)的新方法。本文描述的聚合方法和聚合物致力於解決這些需要。一些反應處於數百萬噸聚合物工業的中心。大部分商品聚合物由烯烴通過形成碳-碳骨架合成,而工程聚合物通常通過含活化羰基或其等同物的單體和合適的親核體的縮合反應,由此形成碳-雜原子鍵製備。以此方式製造聚酯、聚醯胺、聚氨酯和聚醯亞胺。儘管骨架結構多種多樣,但含有硫(VI)"–SO2–"連接體的聚合物在文獻中幾乎不存在並很少用於工業應用,在單體中已存在碸基團的聚碸除外(參見例如Garbassi,在Kirk-OthmerEncyclopediaofChemicalTechnology中;第五版;JohnWiley&Sons:2007;第10卷)。不出所料,合成含硫(VI)聚合物的大多數已報導的嘗試依賴於模仿羰基型縮合的反應,即磺醯氯與親核體的反應(參見例如(a)Goldberg等人,美國專利3,236,808;(b)Firth,美國專利3,895,045;(c)Thomson等人,J.Pol.Sci.,PartA1964,2:1051;(d)Worket等人,Polym.Sci.,PartA:Polym.Chem.1968,6:2022;(e)Schlott等人,在AdditionandCondensationPolymerizationProcesses中;AmericanChemicalSociety:1969;91:703-716)和在小得多的程度上,Friedel-Crafts磺醯化(參見例如Cudby等人,Polymer1965,6:589)。儘管通過這些方法獲得的聚合物的有吸引力的性質,如良好的熱和水解穩定性和機械彈性(參見Thompson等人,同上;Worket等人,同上;和Schlott等人,同上),易水解和參與簡易的氧化還原轉化,尤其是氯化的氯化硫(VI)的非選擇性反應性顯著限制這些方法和材料的效用。許多甲矽烷基化和氟化化合物的反應是有機合成以及聚合物化學中已知的。在1983年,Kricheldorf引入了用於合成聚芳基醚的「甲矽烷基法」,其利用Si–F鍵的強度和甲矽烷基氟化物副產物的無害性質(Kricheldorf等人,J.Pol.Sci.:Pol.Chem.Ed.1983,21:2283;Bier等人,美國專利4,474,932)。在2008年,Gembus證實磺醯氟(R-SO2F)與甲矽烷基醚在催化量的DBU存在下反應,以產生芳基磺酸酯(Gembus等人,Synlett.2008,1463)。氟化硫(VI),特別是硫醯氟(SO2F2)及其單氟化衍生物——磺醯(RSO2–F)氟、氨磺醯(R2NSO2–F)氟和氟代硫酸酯(ROSO2–F)(其中R是有機部分)與其它滷化硫(VI)形成鮮明對比。這些氧代氟化硫水解穩定得多、氧化還原惰性(redoxsilent)並且不充當滷化劑。但是,當在恰當的條件下存在適當的親核體時,可以顯現出它們的選擇性反應性。在70年代早期,Firth由BPA的氟代硫酸酯(獲自BPA和SO2F2)和雙酚的二鈉鹽製備聚(芳基硫酸酯)雙酚A(BPA)聚合物(參見例如Firth,J.Pol.Sci.,PartB1972,10:637;和Firth,美國專利3,733,304)。該聚合需要長時間加熱並產生相當大量的副產物(12至22%),Firth指出它們是環狀低聚物。副產物的脫除需要該聚合物從二甲基甲醯胺(DMF)中反覆沉澱到甲醇中。仍然需要通用並能在相對溫和和可規模化的條件下產生多種多樣的聚合物結構,包括在形式上被視為縮聚物的材料的新型聚合方法。還需要例如用於結構、包裝和纖維用途的新型聚合物,和來自容許帶有額外的非幹擾基團的單體的方法的聚合物,它們可以為特種用途官能化。本文描述的方法和聚合物致力於解決這些需要。除提供獲得具有有用性質的聚合物的實用途徑外,本文描述的有機硫酸酯的格外簡易的合成突出了硫酸酯連接體特別在有機化學中未受到重視的潛力,以及氧代氟化硫(VI)的獨特反應性特徵。本文描述的聚合物和方法應直接適用於不同學科。概述本文描述的聚合方法提供了通過活化的氟取代和甲矽烷基取代單體在溫和反應條件下的催化聚合的相對較高分子量的聚合物的直接合成。在化學計量、溫度和溶劑環境的意料不到的穩固條件下獲得具有驚人高的分子量的聚合物。氟代硫酸酯、氟代磺酸酯、羰基氟和某些雜環氟化物單體與甲矽烷基醚、甲矽烷基胺(特別是與C(=O)F單體)和甲矽烷基硫化物單體在溫和條件下反應,以形成多種多樣的聚合材料,包括例如聚硫酸酯、聚碳酸酯、聚磺酸酯和相關材料。通過含有在許多包裝和工程聚合物中存在的技術上有用的結構單元的聚合物和共聚物的成功形成證實本方法的選擇性。在一個優選實施方案中,由雙氟代硫酸芳基酯和芳基雙甲矽烷基醚在存在本體(即無溶劑)聚合的溫和反應條件下製備聚硫酸酯聚合物。該聚合物可以是基本線性的或在一些實施方案中可包括環狀聚合物鏈或由環狀聚合物鏈構成,其中單聚合物鏈的端基鍵合在一起以形成大環。含有氟取代和甲矽烷基取代單體的單體組合物在鹼性催化劑存在下縮合形成聚合物鏈和易與聚合物產物分離的甲矽烷基氟化物副產物。該單體組合物包含至少一種式F–X–F的化合物和至少一種式(R1)3Si–Z–Si(R1)3的化合物。各R1獨立地為烴基;X具有式–A(–R2–A)n–;各A獨立地為SO2、C(=O)或Het,優選SO2;R2包含第一有機部分;n是0或1;Het是在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環(優選1,3,5-三嗪),且當A是Het時,F取代基連接到其雜芳環的碳原子上;Z具有式–L–R3–L–;各L獨立地為O、S或N(R4),優選O;R3包含第二有機部分,且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;且各R4獨立地為H或第三有機部分。或者,除了或代替F–X–F和(R1)3Si–Z–Si(R1)3的組合,該單體組合物還可包含至少一種式F–X–Z–Si(R1)3的化合物。在聚合過程中,單體的各自的A和L基團一起形成X–Z聚合物鏈,且F和(R1)3Si取代基形成式(R1)3Si–F的甲矽烷基氟化物副產物,其容易與聚合物產物分離並可以再循環。在優選實施方案中,該聚合物包括相對穩定的氟取代端基,如果需要,其可以在選擇性反應條件下改性。該鹼性催化劑可以是脒、胍、磷腈、氮-雜環卡賓、叔醇鹽、氟化物鹽或上述兩種或更多種的組合。令人驚訝地,該雙-甲矽烷基和雙-氟單體的混合物在不存在鹼性催化劑的情況下甚至在升高的溫度下也是不反應的。該聚合方法特別可用於在溫和的高產率條件下製備芳基聚硫酸酯,如雙酚聚硫酸酯,以提供具有適合用於例如材料用途,如工程材料、包裝材料等的分子量和物理性質的聚合物。通過本文描述的方法製成的聚合物,包括芳基聚硫酸酯的一個優點在於,在許多情況下該聚合物的端基包括可以以通過現有方法不易實現的方式單獨反應以將聚合物鏈的末端官能化的氟基。在芳基聚硫酸酯的情況下,-OSO2F和-SO2F端基驚人地穩定,但在如本文所述的易控制條件下可選擇性地分別與酚式OH基團和氨基進行反應或水解成-OH和-SO3ˉ基團。甲矽烷基氟化物副產物可通過與酚式單體前體(例如雙酚A)的鹽(例如鈉或鉀鹽)反應形成有用的雙-甲矽烷基化單體(例如雙-甲矽烷基雙酚A)和氟化物鹽(例如氟化鈉)而再循環。該雙-甲矽烷基化單體可用於另一聚合反應。本文描述的聚合方法的一個實施方案涉及使雙氟化的第一單體與雙-甲矽烷基化的第二單體在鹼性催化劑存在下反應以形成聚合物鏈和甲矽烷基氟化物副產物。第一單體的氟取代基連接到缺電子基團,如磺醯基、羰基或雜芳基活化基團(優選磺醯基)上,且第二單體的甲矽烷基取代基經由氧、硫或氮原子(優選氧原子)連接到有機核心部分上。當第一和第二單體與催化劑合併時,第一單體的氟化物取代基與第二單體的甲矽烷基取代基反應以形成甲矽烷基氟化物,且第一單體的缺電子活化基團與第二單體的連接原子縮合以形成聚合物鏈。第一單體任選也可包括有機核心基團。在一些實施方案中,該方法包括使包含至少一種式F–X–F的化合物(優選FSO2F)的第一單體組合物與包含至少一種式(R1)3Si–Z–Si(R1)3的化合物的第二單體組合物在鹼性催化劑存在下反應,以形成交替的X–Z聚合物鏈和式(R1)3Si–F的甲矽烷基氟化物副產物的步驟。第一單體的X部分具有式–A(–R2–A)n–,其中各A獨立地為SO2、C(=O)或Het,優選SO2;R2包含第一有機部分;n是0或1;且Het是在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環(優選1,3,5-三嗪),其中各F連接到該雜芳環的碳原子上。第二單體的各R1獨立地為烴基(例如直鏈或支鏈烷基、苯基等);Z具有式–L–R3–L–,其中各L獨立地為O、S或N(R4),優選O;R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;且R4是H或第三有機部分。在聚合過程中,第一和第二單體的各自的F和(R1)3Si取代基形成甲矽烷基氟化物,而第一和第二單體的各自的A和L基團交替縮合以形成交替的X–Z聚合物鏈。當n為0時,第一單體的各F取代基連接到同一A基團上。本文描述的聚合方法中所用的鹼性催化劑包含選自脒、胍、磷腈、氮-雜環(N-雜環)卡賓、叔醇鹽和氟化物鹽的至少一種材料。例如,該鹼性催化劑可包含脒鹼(例如1,8-二氮雜雙環[5.4.0]十一-7-烯(DBU)等)、胍(例如1,1,3,3-四甲基胍(TMG)、1,5,7-三氮雜雙環[4.4.0]癸-5-烯(TBD)和7-甲基-1,5,7-三氮雜雙環-[4.4.0]癸-5-烯(MTBD)等)、磷腈鹼(例如2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜磷雜環己烯(diazaphosphorine)(BEMP)、1-叔丁基-4,4,4-三-(二甲基氨基)-2,2-雙[三(二甲基氨基)-亞正膦基(phosphoranyliden)氨基]-2λ5,4λ5-鏈二(磷腈)(P4-t-Bu)等)、氮-雜環卡賓(例如咪唑-2-亞基、1,2,4-三唑-5-亞基、噻唑-2-亞基、咪唑啉-2-亞基等)、叔醇鹽(例如叔丁醇鉀等)或含氟化物的鹽(例如CsF、CsFHF、KF、四丁基氟化銨(TBAF)、二氟三甲基矽酸三(二甲基氨基)鋶(TASF)等)或其中兩種或更多種的組合。該鹼優選包含脒、磷腈或兩者。如果需要,催化劑的組合可以作為混合物添加或相繼添加。優選地,第一和第二單體以大致等摩爾量或在第一(即氟化)單體過量(例如0.01至大約10摩爾%過量)下反應。第一和第二單體可以以純(無溶劑或本體)形式或在溶劑(例如滷代烴、乙腈、吡啶、N-甲基吡咯烷酮等)、溶劑的組合(例如一起或相繼添加)或無溶劑和溶劑條件的組合(例如相繼)中互相接觸。通常,該聚合在大約20℃至大約200℃的溫度下進行大約0.5至大約48小時。該聚合反應意外地容易,並通常表現出相對溫和的反應熱。另外,反應條件和單體意外地容許多種多樣的有機部分和取代基。這意味著"AA"和"BB"單體組分(包括已知幹擾正常酸-鹼反應的基團)的前所未有的選擇自由度和調節所得聚合物的官能度的能力到了非常高的程度。第一單體可以是符合式F–X–F的單一化合物或具有不同X基團的化合物的混合物。類似地,第二單體可以是符合式(R1)3Si–Z–Si(R1)3的單一化合物或具有不同的R1基團、Z基團或兩者的化合物的混合物。此類單體混合物可以以任何所需比例和用任何所需的X和Z基團配製以賦予所得聚合物所需性質,例如所需分子量、所需分子量分布、合意的物理或機械性質(例如玻璃化轉變溫度、水解穩定性、拉伸強度、抗衝擊性、延性、彈性、塑性等)或例如,生物可降解性。在一個實施方案中,第一單體具有式F-A-F。在這一實施方案中,第一單體可以是例如FSO2F、FC(O)F或F–Het–F(優選FSO2F)。如本文所述,Het是在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環,其中各F連接到該雜芳環的碳原子上。示例性的雜環是1,3,5-三嗪,且F取代基共價鍵合到位置2、4和6中的兩個或更多個位置處的碳原子上。當使用氣態單體如FSO2F時,如果需要,該反應可以在能在比1大氣壓高的壓力下運行的反應器中進行。在另一些實施方案中,第一單體是式F–A–R2–A–F的材料。R2是第一有機部分,其可包含或由有機核心材料構成,所述有機核心材料為如烴、雜環、碳水化合物、胺基酸、多肽、肽類似物等或其中兩種或更多種的任何組合,而A基團如上所述選自磺醯基、羰基或雜芳基(Het),優選SO2。在一些實施方案中,R2可以由式–L1–R5–L1–表示,其中各L1獨立地選自O、S和N(R4),優選O;各R5獨立地包含第一有機部分;且各R4獨立地包含H或第三有機部分。或者或另外,R2可以由式–L1–R5–表示,其中各L1和R5如上定義。通過本方法製成的聚合物包含可由式(I):(–A(–R2–A)n–L–R3–L)x–表示的聚合物鏈,其中各A獨立地為SO2、C(=O)或Het,優選SO2;各R2獨立地包含第一有機部分;各n獨立地為0或1;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環;各L獨立地為O、S或N(R4),優選O;各R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;各R4獨立地為H或第三有機部分;且x是該聚合物中的重複單元的平均數並具有至少10的值(例如10至100,000或更大)。該聚合物鏈包括至少一個衍生自第一單體的端基,即包括式E–A–的部分的端基,如E–A(–R2–A)n–,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。當A是Het時,各L基團連接到其雜芳環的碳原子上。或者或另外,該聚合物包括可由式(II):(–A–R2–A–L–R3–L)y–表示的聚合物鏈,其中各A獨立地為SO2、C(=O)或Het,優選SO2;各R2獨立地包含第一有機部分;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環(優選1,3,5-三嗪);各L獨立地為O、S或N(R4),優選O;各R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;各R4獨立地為H或第三有機部分;且y是該聚合物中的重複單元的平均數並具有至少10的值(例如10至100,000或更大)。該聚合物鏈包括至少一個衍生自第一單體的端基,即包括式E–A–的部分的端基,如E–A–R2–A–,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。當A是Het時,各L基團連接到其雜芳環的碳原子上。在另一些實施方案中,該聚合物包括可由式(III):(–A–L1–R5–L1–A–L–R3–L)z–表示的聚合物鏈,其中各A獨立地為SO2、C(=O)或Het,優選SO2;各R5獨立地包含第一有機部分;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環,優選1,3,5-三嗪;各L和L1獨立地為O、S或N(R4),優選O;各R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;各R4獨立地為H或第三有機部分;且z是該聚合物中的重複單元的平均數並具有至少10的值(例如10至100,000或更大)。該聚合物鏈包括至少一個衍生自第一單體的端基,即包括式E–A–的部分的端基,如E–A–L1–R5–L1–A–,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。當A是Het時,各L和L1基團連接到其雜芳環的碳原子上。在再一些實施方案中,該聚合物包括可由式(IV):(–A–L1–R5–A–L–R3–L)m–表示的聚合物鏈,其中各A獨立地為SO2、C(=O)或Het,優選SO2;各R5獨立地包含第一有機部分;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環;各L和L1獨立地為O、S或N(R4),優選O;各R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;各R4獨立地為H或第三有機部分;且m是該聚合物中的重複單元的平均數並具有至少10的值(例如10至100,000或更大)。該聚合物鏈包括至少一個衍生自第一單體的端基,即包括式E–A–的部分的端基,如E–A–L1–R5–A–,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。當A是Het(例如1,3,5-三嗪)時,各L和L1基團連接到其雜芳環的碳原子上。在另一些實施方案中,該聚合物包括可由式(V):(–A–L–R3–L)p–表示的聚合物鏈,其中各A獨立地為SO2、C(=O)或Het,優選SO2;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環;各L獨立地為O、S或N(R4),優選O;各R3包含第二有機部分且R3優選包含至少一個芳基或雜芳基部分;各L基團優選直接鍵合到R3的芳基或雜芳基部分上;各R4是H或另一有機部分;且p是該聚合物中的重複單元的平均數並具有至少10的值(例如10至100,000)。該聚合物鏈包括至少一個衍生自第一單體的端基,即包括式E–A–的部分的端基,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。當A是Het(例如1,3,5-三嗪)時,各L基團連接到其雜芳環的碳原子上。在再一些實施方案中,該聚合物可以由式(VI):(–A–R2–A–L–R3–L)a–(–A–L1–R5–L1–A–L–R3–L)b–(A–L1–R5–A–L–R3–L)c–(–A–L–R3–L)d–表示,其中a、b、c和d代表該聚合物中各自的重複單元的平均數,且a、b、c和d任一可以是0或更大,只要a、b、c和d之和具有至少10的值(例如10至100,000或更大),且該聚合物包括至少一個衍生自第一單體的端基,即式E–A–、E–A–L1–R5–A–、E–A–L1–R5–L1–A–、E–A–R2–A–或E–A(–R2–A)n–的端基,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。A、L、L1、R2、R3和R5各自獨立地如它們在本文所述的其它聚合物和單體實施方案中所定義。在一些實施方案中,至少一部分第一單體包括式F–X–F的支化單體,其中X包括在磺醯基、羰基或雜芳基活化基團上的附加F取代基,以使該附加F取代基也與第二單體的氧、硫或氮原子連接基上的甲矽烷基取代基反應以形成甲矽烷基氟化物,且第一單體的活化基團與第二單體的連接基縮合以在該聚合物中引入至少一個分支點。或者或另外,第二單體可包括支化單體,其中Z包括連接到氧、硫或氮原子連接基上的附加甲矽烷基取代基,以使該附加甲矽烷基取代基與第一單體的磺醯基、羰基或雜芳基活化基團上的氟取代基反應,以形成甲矽烷基氟化物,且第二單體的連接基與第一單體的活化基團縮合以向該聚合物中引入至少一個分支點。在本文描述的任何聚合方法和聚合物中,單體的各有機部分,例如R1、R2、R3、R4、R5和R8可以獨立地選自烴、雜環、碳水化合物、胺基酸、多肽、肽類似物,及其兩種或更多種的組合。在一些實施方案中,R2、R3、R4、R5和R8可包括一個或多個取代基,例如羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。本發明還提供通過本文描述的方法製成的聚合物。該聚合物包含具有選自下列的式的聚合鏈:式(I):(–A(–R2–A)n–L–R3–L)x–;式(II):(–A–R2–A–L–R3–L)y–;式(III):(–A–L1–R5–L1–A–L–R3–L)z–;式(IV):(–A–L1–R5–A–L–R3–L)m–;式(V):(–A–L–R3–L)p–;和式(VI):(–A–R2–A–L–R3–L)a–(–A–L1–R5–L1–A–L–R3–L)b–(A–L1–R5–A–L–R3–L)c–(–A–L–R3–L)d–,和至少一個衍生自如上所述的第一單體,即包括至少一個官能團"E–A–"的端基,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。在上式(I)、(II)、(III)、(IV)、(V)和(VI)中,各A獨立地為SO2、C(=O)或Het,優選SO2;各R2和R5獨立地包含第一有機部分;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少氮原子的芳族雜環(優選1,3,5-三嗪);各L和L1獨立地為O、S或N(R4),優選O;各R3和R5獨立地包含第二有機部分;各R4獨立地為第三有機部分;x、y、z、m、a、b、c和d是該聚合物鏈中各自的重複單元的平均數;x、y、z、m和p各自具有至少10的值(例如10至100,000或更大);且a、b、c和d各自可以是0或更大,只要a、b、c和d之和具有至少10的值(例如10至100,000或更大)。A、L、L1、R2、R3和R5各自獨立地如上文對單體式描述的那樣定義。在本文描述的任何聚合物中,各有機部分,例如R2、R3、R4、R5和R8可以獨立地選自烴、雜環、碳水化合物、胺基酸、多肽、肽類似物,及其兩種或更多種的組合。另外,R2、R3、R4、R5和R8可以被一個或多個官能團取代。此類官能團的非限制性實例包括例如羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸、多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。在一些實施方案中,優選的單體包括雙酚氟代硫酸酯(例如雙酚A氟代硫酸酯、雙酚A雙酚AF氟代硫酸酯、雙酚S氟代硫酸酯和具有連接在一起的兩個酚式基團的相關單體)和雙酚甲矽烷基醚(例如雙酚A甲矽烷基醚、雙酚A雙酚AF甲矽烷基醚、雙酚S甲矽烷基醚和具有連接在一起的兩個酚式基團的相關單體)。本文描述的聚合物通常是容易模製和熱成形成多種多樣的機械部件和結構組件的熱塑性材料。該聚(雙酚A硫酸酯)聚合物抗水解,具有相對較高的介電常數、良好的抗衝擊性以及與聚碳酸酯類似的拉伸強度、彈性模量和伸長。此類聚合物可製造成用於包裝材料、建築材料等的片材和膜,並可用於如汽車和飛機組件(例如擋風玻璃等)、醫療假體、安全護目鏡和容器(例如杯子、瓶子等)之類的用途。附圖簡述圖1圖解可用於本文描述的聚合方法的(A)氟化單體、(B)甲矽烷基化單體和(C)包含氟基和甲矽烷基的單體的非限制性實例。圖2在版塊(a)中示意性圖解所選雙酚A單體合成,在版塊(b)中示意性圖解由該單體合成聚(雙酚A硫酸酯)。圖3圖解(A)由前體材料製備氮-雜環卡賓型鹼性催化劑和(B)各種類型的氮-雜環卡賓的結構。圖4提供通過單體2a和2b的聚合在不同單體濃度下製成的聚(雙酚A硫酸酯)的標準化GPC跡線。圖5圖解溫度和催化劑載量對單體2a+2b(下方曲線)和單體2a+2c(上方曲線)的溶液聚合的影響。圖6提供與表2中的聚合物相關的所選GPC跡線。圖7提供代表性的聚(雙酚A硫酸酯)聚合物樣品的熱重分析(TGA)溫譜圖,其證實在不同條件下製成的並具有不同分子量特徵,即2.5kDa(最下方曲線)、40kDa和59kDa(兩個重疊的上方曲線)的MALSMn值的聚合物的一致的熱分解性質。圖8提供代表性的聚(雙酚A硫酸酯)聚合物樣品的差示掃描量熱法(DSC)二次加熱溫譜圖(插圖)和該聚合物的相應GPCMn相對於Tg的曲線圖。圖9提供與以類似方式壓縮模塑的商業LEXAN聚碳酸酯相比,壓縮模塑的聚(雙酚A硫酸酯)的拉伸應力-應變曲線。圖10示意性圖解通過本文描述的聚合方法製備聚(雙酚A碳酸酯)。圖11圖解由不同的單體組合合成的所選磺酸酯和硫酸酯聚合物的化學結構式,其證實本文描述的聚合方法的寬範圍。圖12圖解通過本文描述的聚合方法製成的聚(雙酚A硫酸酯)的氟代硫酸酯端基的改性以將染料(尼羅紅)連接到聚合物鏈的末端。圖13提供圖12中所示的尼羅紅染料封端的聚(雙酚A硫酸酯)的UV/可見光光譜。圖14提供用於測定聚(雙酚A硫酸酯)的dn/dc的折光指數相對於濃度的曲線圖;版塊(a)提供如本文中的實施例11中所述的流程#1的數據,且版塊(b)提供流程#2的數據。圖15提供(A)通過Firth的方法(US3,733,304)製成的聚(雙酚A硫酸酯)的GPC跡線;和(B)根據本文中的實施例1中描述的本體聚合方法製成的聚(雙酚A硫酸酯)的GPC跡線。圖16提供來自在相同目標條件下在不同反應規模下製成的各種批次的聚(雙酚A硫酸酯)以及在分離後已加熱或加工的樣品的GPC跡線。圖17圖解(A)由胺通過用乙烯磺醯基氟(ESF)處理合成磺醯基氟單體;(b)根據(A)中的圖式製成的所選單體;和(C)由磺醯基氟單體製成的所選共聚物。詳述本聚合方法可提供多種多樣的單體結構、官能取代基和單體-單體連接。在一些實施方案中,該聚合方法包括,基本由或由使至少一種雙氟化的第一單體F-X-F與至少一種雙-甲矽烷基化的第二單體(R1)3Si–Z–Si(R1)3在鹼性催化劑存在下接觸構成。第一單體的氟取代基連接到X的磺醯基、羰基或雜芳基部分上,且第二單體的甲矽烷基連接到Z的氧、硫或氮原子上。在鹼性催化劑存在下,第一單體的氟取代基與第二單體的甲矽烷基取代基反應以形成甲矽烷基氟化物。同時,第一單體的磺醯基、羰基或雜芳基與第二單體的氧、硫或氮原子(甲矽烷基與其連接)縮合,由此形成具有X-Z重複單元的線性交替聚合物鏈。如本文中詳細描述,第一單體可以由式F–A(–R2–A)n–F表示,其中各A獨立地為SO2、C(=O)或Het;R2包含第一有機部分;n是0或1;且Het是在其雜芳環中包含至少兩個碳原子(例如2至4)和至少一個(例如1至4)氮原子的芳族雜環。當A是Het時,各F連接到雜芳環的碳原子上。特別優選的A基團是SO2。當n為0時,第一單體可以由式F–A–F表示(即FSO2F、FC(O)F和F–Het–F)。當n為1時,第一單體可以由式F–A–R2–A–F表示。在一些實施方案中,第一有機部分R2可以由式–L1–R5–L1–表示,其中各L1獨立地選自O、S和N(R4);R5包含第一有機部分,且R4是H或第三有機部分。在另一些實施方案中,第一有機部分R2可以由式–L1–R5–表示,其中L1獨立地選自O、S和N(R4);R5包含第一有機部分,且R4是H或第三有機部分。第二單體(R1)3Si–Z–Si(R1)3可以由式(R1)3Si–L–R3–L–Si(R1)3表示,其中各L獨立地為O、S或N(R4);R3包含第二有機部分;且R4是H或第三有機部分。圖1圖解可用於本文描述的聚合方法的(A)氟化單體、(B)甲矽烷基化單體和(C)包含氟基和甲矽烷基的單體的非限制性實例。該聚合物鏈的X和Z部分通過如–SO2–L–、–C(=O)–L–、–Het–L–、–L1–SO2–L–、–L1–C(=O)–L–或–L1–Het–L–之類的鍵互相連接,其中各L和L1獨立地選自O、S和N(R4);且各R4獨立地包含H或有機部分。如本文所述,Z包含帶有氧、硫或氮原子的有機部分,且X可以是磺醯基、羰基或雜芳基活化基團,或X可包含帶有磺醯基、羰基或雜芳基活化基團的有機核心基團。在一些聚合物實施方案中,X的磺醯基、羰基和雜芳基活化基團直接連接到X中的第一有機部分(如果存在)的碳原子上。或者或另外,X的磺醯基、羰基和雜芳基可通過硫、氧或氮原子連接到其有機部分上。可與第一單體的氟取代基連接的雜芳基(在本文中也稱作雜芳族基團或「Het」)包括在芳環(例如5-元芳環或6-元芳環)中包含至少一個氮原子(例如1至4個氮原子)和至少兩個碳原子(例如2至4個碳原子)的任何雜環部分,且氟取代基連接到芳環中的碳原子上。包含6-元雜芳環的合適的雜芳基Het的非限制性實例包括氮雜苯雜環基團,如吡啶、二嗪(例如1.2-二嗪、1,3-二嗪或1,4-二嗪)和三嗪(例如1,3,5-三嗪);氮雜萘基團,如1-氮雜萘(也稱作喹啉)、2-氮雜萘(也稱作異喹啉)、1,2-二氮雜萘(也稱作噌啉)、2,3-二氮雜萘(也稱作酞嗪)、1,3-二氮雜萘(也稱作喹唑啉)、1,4-二氮雜萘(也稱作喹喔啉)、1,5-二氮雜萘、1,6-二氮雜萘、1,7-二氮雜萘、1,8-二氮雜萘、1,3,5-三氮雜萘、1,3,8-三氮雜萘和1,3,5,8-四氮雜萘(也稱作蝶啶)、氮雜菲咯啉基團,如1,10-二氮雜菲咯啉;等。包含5-元雜芳環的合適的雜芳基Het的非限制性實例包括吡咯、咪唑、噁唑、噻唑、吡唑、異噁唑、異噻唑以及稠合5-和6-元雜環,如吲哚、異吲哚、苯並噻唑、苯並噁唑、嘌呤等。如本文所述,第二單體的Z部分,和任選地,第一單體的X部分,可包含本文所述的式中的任何有機部分(例如R2、R3、R4和R5),因為單體對聚合的反應性主要受控於鹼性催化劑、和第一單體的磺醯基、羰基和雜芳基活化基團、第二單體中的氧、硫和氮原子的組合,和由第一和第二單體各自的氟基和甲矽烷基取代基形成熱力學穩定的甲矽烷基氟化物副產物。可用於本文描述的方法的雙-氟化和雙-甲矽烷基化的單體的非限制性實例在圖1中顯示。圖1的版塊A圖解所選氟化單體;圖1的版塊B圖解所選甲矽烷基單體;而圖1的版塊C圖解包括氟基和甲矽烷基取代基的所選單體。除非本文中另行指明或明顯與上下文相悖,在描述本發明的上下文中(尤其在下列權利要求的上下文中)使用的術語「一」和「該」和類似指示詞應被解釋為涵蓋單數和複數。除非另有說明,術語「包含」、「具有」、「包括」和「含有」應被解釋為開放式術語(即是指「包括,但不限於」)。除非本文中另行指明,本文中的數值範圍的記載僅旨在充當逐一提到落在該範圍內的各單獨數值的簡寫法,各單獨數值就像在本文中逐一記載那樣併入本說明書。通過測量獲得的所有數值(例如重量、濃度、物理尺寸、清除率、流速等)不應被解釋為絕對精確值,而應被視為包括在本領域中常用的測量技術的已知界限內的值。除非本文中另行指明或明顯與上下文相悖,本文描述的所有方法可以以任何合適的順序進行。除非另行要求,本文中提供的任何和所有實例或示例性措辭(例如「如」)的使用僅意在更好地闡明本發明的某些方面,而非限制本發明的範圍。說明書中的措辭都不應被解釋為指明任何未提出權利要求的要素對本發明的實施是必不可少的。關於基團或部分,本文所用的術語「有機」及其語法變型是指包含通常與至少一些氫結合的碳並任選包括一種或多種其它元素,如氧、硫、氮、磷、滷素或來自周期表第II-A族(例如B)、第IV-A族(例如Si)、第V-A族(例如As)、第VI-A族(例如Se)的另一非金屬或準金屬元素的材料。術語「有機」還是指傳統上被描述為有機金屬材料的材料(例如包含共價鍵合到碳原子上的一個或多個主族或過渡金屬原子)以及包括與有機部分絡合或成鹽的金屬元素的材料。有機部分或基團的非限制性實例包括烴、雜環(包括包含至少一個飽和、不飽和和/或芳族環的材料,所述環包含至少一個碳原子和一種或多種其它元素)、碳水化合物(包括糖和多糖)、胺基酸、多肽(包括蛋白質和含有至少兩個經肽鍵鍵合在一起的胺基酸基團的其它材料)、肽類似物(包括包含兩個或更多個通過非肽鍵的鍵,例如酯鍵連接的胺基酸的材料),及其兩種或更多種的組合。另外,有機部分R2、R3、R4、R5和R8可以被一個或多個官能團取代。此類官能團的非限制性實例包括例如羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸、多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。術語「烴」及其語法變型是本領域中公知的並且是指完全由氫和碳構成的有機化合物。烴可以是飽和的(不含多重鍵)、不飽和的(含有至少一個雙鍵或三鍵)或芳族的(含有芳環體系,如苯環或稠合芳環體系,如萘、蒽和類似體系)。烴可包括碳原子的直鏈、碳原子的支鏈、碳原子環或它們的任何組合。烴的非限制性實例包括鏈烷、烯、炔、環烷和基於炔的化合物。術語「烴基」及其語法變型是指通過從烴中除去氫原子形成的一價基團,例如乙基、苯基。術語「碳水化合物」及其語法變型是本領域中公知的並且是指例如在形式上具有經驗元素式(CH2O)x的多羥基化化合物,其中x>1。碳水化合物的非限制性實例包括糖(例如葡萄糖、麥芽糖)、多糖(例如澱粉、纖維素)以及糖和多糖的改性形式(例如代替或除了羥基外,包含一個或多個官能團,如氨基、醚、酯),以及脫氧糖和脫氧多糖(即其中OH已被H替代的糖和多糖)等。該碳水化合物可以是天然存在的材料、合成材料或其組合。術語「胺基酸」及其語法變型是本領域中公知的並且是指例如包含至少一個氨基和至少一個羧酸基的有機化合物。胺基酸的實例包括天然或合成α-胺基酸(例如常見的生產蛋白的胺基酸以及非生產蛋白的胺基酸,如鳥氨酸,根據結構,其可以是手性材料,例如左旋或右旋立體異構體或其混合物,或非手性材料),以及其中氨基和羧酸基被多於一個碳隔開的化合物。術語「多肽」及其語法變型是本領域中公知的並且是指例如包括兩個或更多個胺基酸(通常α-胺基酸)的材料,該兩個或更多個胺基酸通過一個胺基酸的羧酸基(通常α-羧酸基)和另一胺基酸的氨基(通常α-氨基)之間的肽(醯胺)鍵連接在一起。本文所用的術語多肽還包括蛋白質以及具有多肽核心結構以及附著到多肽骨架上的附加官能團或保護基的材料。術語「肽類似物」及其語法變型是指類似於多肽的材料,其中一個或多個肽鍵被非肽鍵,如酯、醚等替代。除非另行規定,本文所用的分子量值,如數均分子量(Mn)和重均分子量(Mw)以及多分散性指數值(「PDI」,即Mw/Mn)基於對照聚苯乙烯標樣的凝膠滲透色譜法(GPC),或如下文的實施例11中所述的與多角度光散射(MALS)聯用的GPC。沒有明確描述或語境暗示為是GPC或MALS值的分子量參數應被解釋為GPC衍生值。分子量值以克/摩爾(也被稱作道爾頓,"Da")或千克/摩爾(也被稱作kDa)為單位報導。令人驚訝地,本文描述的聚合方法可以在各種相對溫和的反應條件下進行。該反應通常可以在環境室溫(例如大約20至25℃)至大約200℃的溫度下進行。當該聚合不用溶劑(純)進行時,可能需要足以熔化單體的溫度。第一和第二單體優選以大致等摩爾量(基於所存在的F和甲矽烷基取代基的摩爾數)或在氟化的第一單體過量(例如0.01至大約10摩爾%過量)下反應。如本文所述,第一和第二單體可以以純形式或在溶劑中互相接觸。合適的溶劑的非限制性實例包括滷代烴(例如二氯甲烷、氯仿、四氯化碳、全氯乙烷、氯氟烴、碳氟化合物等)、醚(例如二乙醚、四氫呋喃、二甲氧基乙烷等)、酯(例如乙酸乙酯)、腈(例如乙腈等)、酮(例如丙酮、甲乙酮)、吡啶(例如吡啶、甲基吡啶等)、醯胺(例如N-甲基吡咯烷酮、乙醯胺、二甲基乙醯胺等)、亞碸(例如二甲亞碸等)和碸(例如環丁碸、二甲基碸等)。該溶劑優選是非水和非質子的。如果需要,可以使用混合溶劑體系,或該聚合反應可以相繼在不同溶劑中或在無溶劑和溶劑條件的組合中(例如在一種溶劑中(或無溶劑)開始並在另一溶劑中完成聚合)進行。該聚合的甲矽烷基氟化物副產物容易通過化學領域的普通技術人員公知的各種方法的任意一種與聚合物產物分離。例如,根據該甲矽烷基氟化物的沸點,可通過在環境大氣壓或減壓下蒸餾或蒸發除去甲矽烷基氟化物。或者或另外,可通過用溶解甲矽烷基氟化物但不溶解聚合物產物的溶劑(例如烴溶劑)洗滌從聚合物產物中除去傾向於相對非極性的甲矽烷基氟化物副產物。該甲矽烷基氟化物副產物也可通過與雙酚式單體前體(例如雙酚A)的鹽反應形成雙-甲矽烷基醚型單體而再循環。獲自本文描述的方法的聚合材料優選具有至少大約10,更優選大於10(例如10至大約100、200、300、400、500、1,000、10,000、100,000或更大)的聚合度(即單體單元的平均數)。在本文描述的方法中,第一和第二單體可各自包含單一的單體材料,或兩種或更多種單體材料的組合——作為混合物或相繼添加到聚合反應中。例如,第一單體F–X–F可包含兩種或更多種具有不同的X基團的單體材料的組合。類似地,第二單體(R1)3Si–Z–Si(R1)3可包含具有不同的R1基團、不同的Z基團或兩者的兩種或更多種單體材料的組合。單體的此類組合可以以如本文所述的任何所需比例配製,或可以分開添加到該聚合混合物中。根據各種單體的相對反應性,以及根據不同單體材料是一開始混合在一起還是以連續方式接觸,或是混合和連續添加的一些組合,由單體材料的此類組合產生的聚合物可包括無規分布的重複單元或可包括具有相同結構的重複單體單元的嵌段,或無規和嵌段化的鏈段。作為非限制性實例,第一單體的混合物可包括90摩爾%(mol%)的F–SO2–F和10摩爾%的F–SO2–CH2–Ph–SO2–F。第一單體的這種混合物與式Me3Si–O–Ph–CMe2–Ph–O–SiMe3的第二單體的反應隨之提供具有經驗式:–(SO2–O–Ph–CMe2–Ph–O–)e–(SO2–CH2–Ph–SO2–O–Ph–CMe2–Ph–O–)f–並具有大約9:1的e:f近似比的聚合物,其中SO2–O–Ph–CMe2–Ph–O和SO2–CH2–Ph–SO2–O–Ph–CMe2–Ph–O重複單元可能以無規方式分布在聚合物鏈中。或者,可如下形成嵌段共聚物:使一定量(例如9摩爾)的單一第一單體組合物F–SO2–F和更大摩爾量(例如10摩爾)的單一第二單體組合物Me3Si–O–Ph–CMe2–Ph–O–SiMe3接觸以形成第一均勻聚合物鏈段–(SO2–O–Ph–CMe2–Ph–O–)e,然後一定量(例如1摩爾)的不同的第一單體F–SO2–CH2–Ph–SO2–F,其足以與剩餘量的第二單體反應以形成第二聚合物鏈段(例如–(SO2–CH2–Ph–SO2–O–Ph–CMe2–Ph–O–)f),從而產生具有a:b的近似摩爾比例(即,在此實例中為大約9:1)的嵌段的嵌段共聚物。如聚合物領域中的普通技術人員所理解,第二單體也包含或者能包含多種具有不同Z基團的化合物,以產生具有重複單元的多種組合的聚合物,例如通式–(X1–Z1)g–(X1–Z2)h–(X2–Z1)i–(X2–Z2)k...–(X'–Z')w–的聚合物,其中g、h、i、k和w與該聚合反應混合物中存在的各不同的第一和第二單體的相對量成比例。在一些實施方案中,至少一部分第一單體包括式F–X–F的支化單體,其中X包括在選自如本文其它地方定義的SO2、C(=O)和Het的活化基團上的附加F取代基,以使所述附加F取代基也與第二單體的甲矽烷基取代基反應以形成甲矽烷基氟化物,且所述附加活化基團與第二單體的L基團縮合以在該聚合物中引入至少一個分支點。例如,第一單體可包含具有被三個活化氟取代基取代的有機核心基團如苯基的支化單體,如1,3,5-三-氟磺醯基苯或2,4,6-三氟-1,3,5-三嗪,其中該三嗪既是活化基團(Het),又是有機核心基團,或由該支化單體構成。另外或或者,第二單體可包括具有連接到氧、硫或氮原子上的附加甲矽烷基取代基的支化單體。如本文中所述,支化第二單體的反應也導致通過氧、硫或氮原子與第一單體的磺醯基、羰基或雜芳基活化基團的縮合向該聚合物中引入至少一個分支點,且氟基和甲矽烷基取代基的伴隨反應形成甲矽烷基氟化物。在本文描述的任何聚合方法實施方案中,有機部分,例如R2、R3、R4、R5和R8可選自烴、雜環、碳水化合物、胺基酸、多肽、肽類似物和其中兩種或更多種的組合。在一些實施方案中,R1、R2、R3、R4和R5可包括一個或多個取代基,例如羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸、多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。本文描述的聚合方法的一個有趣和有用的特徵在於所得產物包含至少一個鏈端且通常兩個鏈端都衍生自第一(氟化)單體的聚合物鏈,以使如此製成的聚合物包含氟取代的端基(例如SO2F、COF或HetF)。該氟取代的端基可用於在官能上改性該聚合物鏈的末端,例如通過用基於氧、氮或硫的親核體親核置換F取代基。這種端基改性可以在聚合過程結束時(例如當在溶液中進行聚合時)在聚合混合物中進行,或所得氟封端的聚合物可以在已分離出最初形成的聚合物後在分開的反應中與親核體反應。用於置換F取代基的適合的親核體的非限制性實例包括羥基取代的材料(例如醇和酚類化合物)、胺、疊氮化物、硫醇等。在一些實施方案中,通過本文描述的方法製備的聚合物包含具有選自下列的式的聚合鏈:式(I):(–A(–R2–A)n–L–R3–L)x–;式(II):(–A–R2–A–L–R3–L)y–;式(III):(–A–L1–R5–L1–A–L–R3–L)z–;式(IV):(–A–L1–R5–A–L–R3–L)m–;式(V):(–A–L–R3–L)p–;和式(VI):(–A–R2–A–L–R3–L)a–(–A–L1–R5–L1–A–L–R3–L)b–(A–L1–R5–A–L–R3–L)c–(–A–L–R3–L)d–。在上式(I)、(II)、(III)、(IV)、(V)和(VI)中,各A獨立地為SO2、C(=O)或Het,優選SO2;各R2和R5獨立地包含第一有機部分;各Het獨立地為在其雜芳環中包含至少兩個碳原子和1至4個氮原子的芳族雜環,其中各L連接到雜芳環的碳原子上;各L獨立地為O、S或N(R4),優選O;各R3獨立地包含第二有機部分;且各R4獨立地為H或第三有機部分。在式(I)、(II)、(III)、(IV)和(V)中,x、y、z、m和p各自是該聚合物中的重複單元的平均數並具有至少10的值(例如10至大約100、200、300、400、500、1,000、10,000、100,000或更大)。在式(VI)中,各a、b、c和d是各自的重複單元的平均數並可以獨立地為0或更大,只要a、b、c和d之和為至少10(例如10至大約100、200、300、400、500、1,000、10,000、100,000或更大)。式(I)、(II)、(III)、(IV)和(V)中的聚合物鏈包括至少一個衍生自第一單體的端基,優選兩個端基,即包括E–A–部分的端基,其中E優選是氟取代基(F),或E是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為如本文對R1、R2、R3、R4和R5所述的有機部分。可通過本文描述的方法製造的一類聚合物的實例是聚(有機硫酸酯),如本文的實施例中詳細描述的聚(雙酚硫酸酯)。在一個實施方案中,該聚(雙酚硫酸酯)由式(IV)表示,其中各A是SO2,且各L是O且各R3是式:–Ph–C(R7)2–Ph–的化合物,其中各Ph是1,4-亞苯基,且各R7是H、(C1-C4)烷基(例如甲基、乙基和丙基)或滷代(C1-C4)烷基(例如三氟甲基)。在本文描述的任何聚合物中,有機部分,例如R2、R3、R4、R5和R8可選自烴、雜環、碳水化合物、胺基酸、多肽和其中兩種或更多種的組合。另外,R2、R3、R4和R5可以被至少一個官能團取代。此類官能團的非限制性實例包括例如羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。在一個優選實施方案中,第一和第二單體可包含雙酚型化合物,其中兩個酚式基團(被氟磺醯基或甲矽烷基封端)通過連接鍵或連接基(例如氧、硫、氮、羰基或飽和或不飽和的亞烷基,其可以是取代或未取代的)連在一起,例如式VII的第一單體和式VIII的第二單體:其中各R1獨立地為烴基,且R9獨立地為共價鍵、C(CH3)2、C(CF3)2或SO2。一種優選聚合物是式IX的化合物:其中t是單體單元的平均數並且為至少10(例如10至大約100、200、300、400、500、1,000、10,000、100,000或更大),且E是F或是可通過從"A"部分中親核置換F而得的官能團,如疊氮基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、烷基硫基和類似基團。在一些實施方案中,E選自氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為如本文對R1、R2、R3、R4和R5所述的有機部分。下面例示本文描述的方法和材料的某些非限制性實施方案。實施方案A是一種聚合方法,其包括使液體單體組合物與鹼性催化劑接觸的步驟,其中所述單體組合物包含至少一種式F–X–F的化合物和至少一種式(R1)3Si–Z–Si(R1)3的化合物;其中:各R1獨立地為烴基;X具有式–A(–R2–A)n–;各A獨立地為SO2、C(=O)或Het;R2包含第一有機部分;n是0或1;Het是在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環,且當A是Het時,F取代基連接到其雜芳環的碳原子上;Z具有式–L–R3–L–;各L獨立地為O、S或N(R4);R3包含第二有機部分;各R4獨立地為H或第三有機部分;且其中在單體的各自的A和L基團縮合以形成X–Z聚合物鏈時,F和(R1)3Si取代基形成式(R1)3Si–F的甲矽烷基氟化物副產物;且其中所述鹼性催化劑包含選自脒、胍、磷腈、氮雜環卡賓、叔醇鹽和氟化物鹽的至少一種材料。實施方案B是實施方案A的方法,其中:各R1獨立地為烷基或芳基;X具有式–A(–R2–A)n–;各A是SO2;R2包含第一有機部分;n是0或1;Z具有式–L–R3–L–;各L獨立地為O;且R3包含含有至少一個直接鍵合到各L上的芳基或雜芳基的第二有機部分。實施方案C是實施方案A或B的方法,其中n是0。實施方案D是實施方案A至C任一項的方法,其中Het是1,3,5-三嗪。實施方案E是實施方案A至D任一項的方法,其中所述單體組合物包括一種化合物,其中X包括在磺醯基、羰基或雜芳基活化基團A上的附加F取代基,以使所述附加F取代基也與氧、硫或氮原子連接基L上的(R1)3Si取代基反應以形成甲矽烷基氟化物,且所述活化基團與所述連接基縮合以在所述聚合物中引入分支點。實施方案F是實施方案A至E任一項的方法,其中所述單體組合物包括一種化合物,其中Z包括在氧、硫或氮原子連接基L上的附加甲矽烷基取代基(R1)3Si,以使所述附加甲矽烷基取代基也與磺醯基、羰基或雜芳基活化基團A上的F取代基反應以形成甲矽烷基氟化物,且所述連接基與所述活化基團縮合以在所述聚合物中引入分支點。實施方案G是實施方案A至F任一項的方法,其中n是1;R2是–L1–R5–L1–;各L1獨立地選自O、S和N(R4);且各R4獨立地為H或第三有機部分,且R5包含有機部分。實施方案H是實施方案A至G任一項的方法,其中n是1;R2是–L1–R5–;L1選自O、S和N(R4);R4是H或第三有機部分;且R5是有機部分。實施方案I是實施方案A至H任一項的方法,其中所述鹼性催化劑包含1,8-二氮雜雙環[5.4.0]十一-7-烯(DBU)。實施方案J是實施方案A至I任一項的方法,其中所述鹼性催化劑包含選自如下的至少一種磷腈:2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜磷雜環己烯(BEMP)和1-叔丁基-4,4,4-三-(二甲基氨基)-2,2-雙[三(二甲基氨基)-亞正膦基氨基]-2λ5,4λ5-鏈二(磷腈)(P4-t-Bu)。實施方案K是實施方案A至J任一項的方法,其中所述鹼性催化劑包含選自CsF、CsFHF、KF、四丁基氟化銨(TBAF)和二氟三甲基矽酸三(二甲基氨基)鋶(TASF)的至少一種氟化物鹽。實施方案L是實施方案A至K任一項的方法,其中所述鹼性催化劑包含選自1,1,3,3-四甲基胍(TMG)、1,5,7-三氮雜雙環[4.4.0]癸-5-烯(TBD)和7-甲基-1,5,7-三氮雜雙環-[4.4.0]癸-5-烯(MTBD)的至少一種胍。實施方案M是實施方案A至L任一項的方法,其中所述鹼性催化劑包含選自咪唑-2-亞基、1,2,4-三唑-5-亞基、噻唑-2-亞基和咪唑啉-2-亞基的至少一種氮-雜環卡賓。實施方案N是實施方案A至M任一項的方法,其中各A是SO2。實施方案O是實施方案A至N任一項的方法,其中各R2包含直接鍵合到A基團上的芳基或雜芳基部分,或通過與所述芳基或雜芳基部分上連接的氧原子鍵合到A上的芳基或雜芳基部分。實施方案P是實施方案A至O任一項的方法,其中所述聚合物包含選自下列的式所示的聚合鏈:式(I):(–A(–R2–A)n–L–R3–L)x–;式(II):(–A–R2–A–L–R3–L)y–;式(III):(–A–L1–R5–L1–A–L–R3–L)z–;式(IV):(–A–L1–R5–A–L–R3–L)m–;式(V):(–A–L–R3–L)p–;和式(VI):(–A–R2–A–L–R3–L)a–(–A–L1–R5–L1–A–L–R3–L)b–(A–L1–R5–A–L–R3–L)c–(–A–L–R3–L)d–;其中:各A獨立地為SO2、C(=O)或Het;各L和L1獨立地為O、S或N(R4);各R2和R5獨立地包含第一有機部分;各R3包含第二有機部分;各R4獨立地為H或第三有機部分;各n獨立地為0或1;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環,且當A是Het時,F取代基連接到其雜芳環的碳原子上;x、y、z、m和p各自是該聚合物中的重複單元的平均數並具有至少10的值;且各a、b、c和d是各自的重複單元的平均數,並可以獨立地為0或更大,只要a、b、c和d之和為至少10。實施方案Q是實施方案A至P任一項的方法,其中R2、R3、R4和R5中的一個或多個包含選自如下的部分:烴、雜環、碳水化合物、胺基酸、多肽、肽類似物和其中兩種或更多種的組合。實施方案R是實施方案A至Q任一項的方法,其中R1、R2、R3、R4和R5中的一個或多個被選自如下的至少一個取代基取代:羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。實施方案S是實施方案A至R任一項的方法,其中所述單體組合物包含(a)兩種或更多種不同的式F–X–F的化合物,(b)兩種或更多種不同的式(R1)3Si–Z–Si(R1)3的化合物,或(c)(a)和(b)的c組合。實施方案T是實施方案S的方法,其中所述兩種或更多種不同的式(R1)3Si–Z–Si(R1)3的化合物因R1、Z或R1和Z的選擇而有差別。實施方案U是實施方案A至T任一項的方法,其中所述單體組合物包含至少一種式VII的化合物和至少一種式VIII的化合物:其中各R1獨立地為烷基或芳基,且各R9獨立地為共價鍵、C(CH3)2、C(CF3)2或SO2。實施方案V是實施方案A至U任一項的方法,其中所述液體單體混合物包含溶解在溶劑中的單體混合物。實施方案W是實施方案A至V任一項的方法,其中所述液體單體混合物包含熔融的單體混合物。實施方案X是實施方案A至W任一項的方法,其中所述F-X-F單體包含硫醯氟(FSO2F)。實施方案Y是實施方案A至W任一項的方法,其中所述F-X-F單體包含式F-SO2-CH2CH2-N(R11)-CH2CH2-SO2-F的雙氟磺醯基單體,其中R11包含有機部分。實施方案Z是實施方案Y的方法,其中R11包含選自如下的部分:烴、雜環、碳水化合物、胺基酸、多肽、肽類似物和其中兩種或更多種的組合。實施方案AA是實施方案Y或實施方案Z的方法,其中R11被選自如下的至少一個取代基取代:羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。實施方案AB是一種聚合物,其包含具有選自下列的式的聚合鏈:式(I):(–A(–R2–A)n–L–R3–L)x–;式(II):(–A–R2–A–L–R3–L)y–;式(III):(–A–L1–R5–L1–A–L–R3–L)z–;式(IV):(–A–L1–R5–A–L–R3–L)m–;式(V):(–A–L–R3–L)p–;和式(VI):(–A–R2–A–L–R3–L)a–(–A–L1–R5–L1–A–L–R3–L)b–(A–L1–R5–A–L–R3–L)c–(–A–L–R3–L)d–;其中:各A獨立地為SO2、C(=O)或Het;各L和L1獨立地為O、S或N(R4);各R2和R5獨立地包含第一有機部分;各R3包含第二有機部分;各R4獨立地為H或第三有機部分;各n獨立地為0或1;各Het獨立地為在其雜芳環中包含至少兩個碳原子和至少一個氮原子的芳族雜環,且當A是Het時,F取代基連接到其雜芳環的碳原子上;x、y、z、m和p各自是該聚合物中的重複單元的平均數並具有至少10的值;且各a、b、c和d是各自的重複單元的平均數,並可以獨立地為0或更大,只要a、b、c和d之和為至少10;且該聚合物在聚合物鏈的一端或兩端包括式E–A–的基團,其中各E獨立地為氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。實施方案AC是實施方案AB的聚合物,其中一個或多個有機部分R2、R3、R4、R5和R8選自烴、雜環、碳水化合物、胺基酸、多肽、肽類似物和其中兩種或更多種的組合。實施方案AD是實施方案AB或AC的聚合物,其中R2、R3、R4、R5和R8中的一個或多個被選自如下的至少一個取代基取代:羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。實施方案AE是實施方案AB的聚合物,其中所述聚合物包含式IX的化合物:其中t是單體單元的平均數並且為至少10,各E獨立地為氟、OR8、NHR8、N(R8)2、疊氮基、CN或SR8,且各R8獨立地為有機部分。實施方案AF是實施方案AB至AD任一項的聚合物,其中所述聚合物具有式(I):(–A(–R2–A)n–L–R3–L)x–,其中各A是SO2,且各R2獨立地為-CH2CH2-N(R11)-CH2CH2-,其中R11包含有機部分。實施方案AG是實施方案AF的聚合物,其中R11包含選自如下的部分:烴、雜環、碳水化合物、胺基酸、多肽、肽類似物和其中兩種或更多種的組合。實施方案AH是實施方案AF或AG的聚合物,其中R11被選自如下的至少一個取代基取代:羥基、滷素、硝基、–C(O)R6、–C(O)OR6、–C(O)N(R6)2、–CN、–SOvR6、–SOvN(R6)2、R6SOvN(R6)–、–N(R6)SOvR6、–SO3R6、–N(R6)2、–N(R6)OR6、–N(R6)C(O)R6、–N(R6)C(O)OR6、–N(R6)C(O)N(R6)2、–OC(O)N(R6)2、–OC(O)OR6、疊氮基、烷基、環烷基、鏈烯基、炔基、烷氧基、氟烷基、氟烷氧基、芳基、芳氧基、雜芳基、聚(乙烯氧基)、炔基封端的聚(乙烯氧基)、脂肪酸、碳水化合物、胺基酸和多肽;其中各R6獨立地為H、烷基或芳基,且v是0、1或2。實施方案AI是實施方案AB的聚合物,其中所述聚合物具有小於大約2.2的基於使用聚苯乙烯標樣的凝膠滲透色譜法的分子量多分散性指數(PDI),並包括少於大約5重量%的環狀低聚物。實施方案AJ是實施方案AI的聚合物,其中所述聚合物是聚(雙酚A硫酸酯)。實施方案AK是包含聚(雙酚A硫酸酯)的透明的基本無色膜或片材。實施方案AL是製備實施方案AK的膜或片材的方法,其包括將聚(雙酚A硫酸酯)制粒並在升高的壓力下在高於其玻璃化轉變溫度的溫度下壓縮所述顆粒。實施方案AM是實施方案AL的方法,其中所述升高的壓力為至少大約25,000磅/平方英寸(psi)且所述溫度為大約200至250℃。在本文描述的任一實施方案中,氟化單體F-X-F的一個或多個A基團(即SO2、C(=O)或Het)可以被式S(=O)(=NR12)的基團替代,即,以形成含有代替SO2F、C(=O)F或Het-F基團的-S(=O)(=NR12)F官能團的單體。在下列非限制性實施例中進一步例示本文描述的方法和聚合物的某些方面和特徵。實施例1.示例性聚(雙酚A硫酸酯)製備丙烷-2,2-二基雙(4,1-亞苯基)二氟代磺酸酯(2a)的大規模製備.在2升單頸圓底燒瓶中裝入雙酚A(114.9克,0.5摩爾)、CH2Cl2(DCM;1升)和三乙胺(Et3N;174毫升,1.25摩爾,2.5當量)。將該混合物在室溫下攪拌10分鐘(min)。然後將反應燒瓶用隔膜密封,在溫和真空下除去溶液上方的氣氛,並通過針從充滿氣體的氣球引入SO2F2氣體(硫醯氟,VIKANE)。對於像這樣的大規模反應,容易觀察到從氣球中耗盡硫醯氟,並在需要時用新的氣球引入更多試劑。對於小規模反應,過量使用SO2F2。容易通過薄層色譜法(TLC)追蹤這些反應。反應混合物在室溫下劇烈攪拌2-4小時,通過GC-MS和TLC監測。在完成後,通過旋轉蒸發除去溶劑,將殘留物溶解在乙酸乙酯(EtOAc;1升)中,該溶液用1NHCl(2x500毫升)和鹽水(2x500毫升)洗滌。有機相經無水Na2SO4乾燥並濃縮。所得固體在高真空下在60℃下乾燥整夜,從而以定量收率產生白色結晶固體形式的所需化合物(197.1克,100%收率)。熔點(mp)48-49℃。1HNMR(400MHz,CDCl3)δ7.34-7.32(m,2H),7.28-7.26(m,2H),1.72(s,3H);13CNMR(101MHz,CDCl3)δ150.4,148.2,128.7,120.5,42.9,28.4,30.7;19FNMR(376MHz,CDCl3)δ+37.0;GC-MS(tR):7.2min;EI-MS(m/z):392[M]+。(丙烷-2,2-二基雙(4,1-亞苯基))雙(氧基))雙(叔丁基二甲基)矽烷(2c)的大規模製備.在2升燒瓶中,將88.4克(2.6當量,1.3摩爾)咪唑添加到雙酚A(114.2克,0.5摩爾)在DCM(1000毫升)中的溶液中,這種溶液在室溫下攪拌10分鐘。接著將181克叔丁基二甲基甲矽烷基氯(TBSCl;2.4當量,1.2摩爾)溶解到200毫升DCM中,並通過加料漏鬥經30分鐘將所得TBSCl溶液添加到雙酚A中。該反應在室溫下攪拌24小時。通過TLC或GCMS監測該反應。然後通過旋轉蒸發除去DCM溶劑,加入1000毫升EtOAc以再溶解該殘留物,該EtOAc溶液用500毫升飽和碳酸氫鈉溶液洗滌兩次,用500毫升鹽水洗滌兩次,然後有機相經無水Na2SO4乾燥。通過旋轉蒸發除去溶劑。所得產物在高真空下在70℃下乾燥24小時。獲得白色固體形式的純雙-TBS雙酚A化合物(225.2克,98.5%收率),其在聚合反應之前不需要進一步提純。mp78-80℃;1HNMR:(400MHz,CDCl3,23℃):δ7.10-7.07(m,4H),6.76-6.73(m,4H),1.65(s,6H),1.01(s,18H),0.22(s,12H).13CNMR:(100MHz,CDCl3,23℃):δ153.2,143.7,127.7,119.2,41.7,31.1,25.7,18.2,-4.39。GCMS:8.38min,MSm/z456.3(M+)。大規模本體聚合–(0.5摩爾規模)的聚(雙酚A硫酸酯).在配有回流冷凝器、兩個橡膠隔膜(其中之一含有用於內部測量的溫度計)和Teflon塗布的磁攪拌棒的1,000毫升3頸圓底燒瓶中裝入2a(98.1克,0.25摩爾)和2c(114.5克,0.25摩爾)。將反應容器放入油浴中並達到135℃。一旦單體熔融(內部溫度120℃),加入1摩爾%在1M己烷溶液(5毫升,5毫摩爾)中的BEMP。在5分鐘內,觀察到叔丁基二甲基氟矽烷(TBSF)回流。在大約45分鐘後,該反應混合物凝固並停止攪拌。繼續在120℃下加熱另外45分鐘,此時將回流冷凝器換成蒸餾頭,並蒸餾出TBSF(分離出56克)。然後將DMF(300毫升)添加到固體粗製BPA-聚硫酸酯產物中,並在130℃下繼續加熱直至恢復攪拌且所有聚合物溶解。使所得清澈無色DMF溶液冷卻至大約60℃,然後以連續一致的速率緩慢倒入在環境溫度下的含3升劇烈攪拌的(頂置攪拌器)甲醇的燒杯中,以致形成長的纖維狀BPA-聚硫酸酯絲束。這種材料(144克,99.3%)在真空爐中在80℃下乾燥整夜,通過GPC分析。PDI=1.7;參照聚苯乙烯標樣的Mn=120,000Da;通過MALS測得的Mn=58,000;Tg=98℃;1HNMR(400MHz,DMSO-d6)δ7.31(apps,8H),1.61(2,6H);對(C15H14O4S)n的計算值:C,62.05;H,4.86;S,11.04.實測值:C,61.98;H,4.80;S,10.84;F,0.33。本文描述的聚合反應極其有效,當使用雙(芳基氟代硫酸酯)2a和雙(芳基甲矽烷基)醚2b-e時,製成高分子量聚合物(圖2)。通過有機鹼,如1,8-二氮雜雙環[5.4.0]十一-7-烯(DBU)或2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜-磷雜環己烯(BEMP),或氟化物鹽,如CsF催化該反應。其以基本定量收率進行,與許多官能團相容,並且不需要特殊設備或預防措施。氟代硫酸酯和甲矽烷基醚單體都容易由BPA獲得(圖2,版塊(a))。其在三乙胺存在下用SO2F2氣體處理以生成雙(氟代硫酸酯)2a,其根據不需要色譜提純的簡單後處理程序在摩爾規模下以高收率作為貯存穩定的白色結晶固體分離。雙(甲矽烷基醚)單體2b-e可購得(2b)或容易根據標準程序大規模製備(2c-e)。在不同溶劑(1M在單體中)中在20摩爾%DBU存在下單體2a和2b之間的反應的最初檢查確認N-甲基吡咯烷酮(NMP)和二甲基甲醯胺(DMF)是用於製備聚硫酸酯的最佳溶劑(圖2,版塊(b))。在從甲醇中沉澱後,BPA-聚硫酸酯(BPA-PS)以95%收率作為白色粉末回收(GPCMn=30,900g/mol,參考聚苯乙烯標樣)。當使用TBS單體(2c)時,結果類似(GPCMn=24,600g/mol);在後一情況中,生成液體叔丁基氟二甲基矽烷(3c,TBSF)副產物並通過蒸餾除去。實施例2.催化劑評估.使用在乙腈中的單官能氟代硫酸酯(PhOSO2F)和TBS保護的酚(PhOTBS)評估各種有機和無機鹼、親核體、路易斯酸和氟化物源。結果表明脒、胍和磷腈是特別有用的催化劑。另一些活性催化劑是經有機和無機源引入的氟化物以及非親核的叔丁醇鹽鹼(KOt-Bu)。然後將活性催化劑用於BPA-氟代硫酸酯單體(2a)以及TMS(2b)和TBS(2c)保護的BPA單體在室溫下的聚合(參見表1)。TMS單體體系(2a+2b)提供高達大約Mn30,000至35,000g/mol的BPA-聚硫酸酯(基於GPC),而TBS單體體系(2a+2c)表現出更寬範圍的所得Mn值。在脒催化劑,表1中的條目1-3中,DBU對生成聚合物最有效,而DBN和PMDBD主要提供低聚物。胍,條目4-6,與脒催化劑基本相當(即使不是更優異),其中MTBD與DBU相比以一半的催化劑載量提供具有兩倍Mn的BPA-聚硫酸酯(2a+2c體系)。如通過BEMP製成的55,400g/mol的聚硫酸酯所證實,磷腈,條目7-8表現出最高催化活性。最後,催化用的KOt-Bu(條目9)和氟化物(條目10-11)僅在TBS體系中才產生聚硫酸酯,而在TMS體系中產生低分子量(MW)低聚物。由這些和其它初始研究看出,與2b,TMS體系(其表現出大約35,000g/mol的明顯Mn上限)相比,在酚式羥基取代基上具有更穩定的TBS保護基的2c提供製備具有更高Mn的聚硫酸酯的潛力。這兩種體系之間的差異可能與TBS酚與TMS酚相比高得多的鹼性穩定性相關。表1.BPA-聚硫酸酯催化劑評估在表1中,聚合條件是:催化劑載量[a]20摩爾%或[b]10摩爾%;摩爾濃度NMP[c]大約1M或[d]大約0.5M;反應時間[e]24小時或[f]48小時。由甲醇沉澱分離材料並通過GPC分析。Mn參考聚苯乙烯標樣。縮寫:DBU=1,8-二氮雜雙環[5.4.0]十一碳-7-烯;DBN=1,5-二氮雜雙環[4.3.0]-壬-5-烯;PMDBD=1,2,3,4,4a,5,6,7-八氫-2,2,4a,7,7-五甲基萘啶;TMG=1,1,3,3-四甲基胍;TBD=1,5,7-三氮雜雙環[4.4.0]癸-5-烯;MTBD=7-甲基-1,5,7-三氮雜雙環-[4.4.0]癸-5-烯;BEMP=2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜磷雜環己烯;P4-t-Bu=1-叔丁基-4,4,4-三-(二甲基氨基)-2,2-雙[三(二甲基氨基)-亞正膦基氨基]-2λ5,4λ5-鏈二(磷腈);KOt-Bu,叔丁醇鉀;CsF=氟化銫;TASF=二氟三甲基矽酸三(二甲基氨基)鋶。氮-雜環卡賓也可用作本文描述的聚合方法中的催化劑。圖3圖解由鹽和兩性離子中間體製備氮-雜環卡賓(版塊A)以及一些雜環卡賓種類(版塊B,其圖解了咪唑-2-亞基、1,2,4-三唑-5-亞基、噻唑-2-亞基和咪唑啉-2-亞基)。代表性的卡賓是1,3-(二-(2,4,6-三甲基苯基)-2,3-二氫-1H-咪唑-2-亞基。Enders等人,Chem.Rev.2007,107:5606-5655詳細描述了這些卡賓鹼和它們的製備,其全文經此引用併入本文。單體2a和2c與1,3-(二-(2,4,6-三甲基苯基)-2,3-二氫-1H-咪唑-2-亞基的兩性離子羧酸鹽前體的反應(參見圖3)在加熱時釋放CO2並原位產生活性催化劑。在2毫摩爾規模下,所得聚合物的GPCMn為56,000Da(聚苯乙烯標樣)且PDI為1.4。尚未理解催化的機制。初步調查表明用F-/HF2-活化甲矽烷基醚和它們轉化成高價矽衍生物可能至少部分是導致觀察到的甲矽烷基醚與氟代硫酸酯的反應性的原因。DBU和類似催化劑與氟磺醯基的相互作用也可能在該反應中發揮作用。實施例3.濃度、溫度和催化劑載量的評估用TMS體系(2a+2b)研究濃度的影響。分子量在本體中(在大約150℃,遠高於大約90至98℃的Tg)最高並隨濃度降低而降低(參見圖4)。本體聚合還表現出最低量的據信為環狀低聚物副產物,在GPC中在大約23分鐘表現出洗脫。如通過GPC測得的窄PDI和低Mn表明這種副產物的環狀拓撲。該環狀低聚物在有機溶劑中的溶解度低於該聚合物。儘管尚未確認確切的結構,但該環狀副產物表現出對稱NMR且元素分析表明(C15H14O4S)n的分子式(62.32%C,1.89%H,11.03%S)。環狀副產物的量隨濃度降低而提高。環狀副產物形成量的這種增加預計歸因於在低濃度下提高的分子內反應趨勢。對BPA-聚碳酸酯觀察到類似效應。在通過將2a和2b逐滴添加到含DBU的稀乙腈溶液中實現的低濃度下,該產物是幾乎純的環狀低聚物。對於在上述本體聚合條件下的活性的其它催化劑篩選包括BEMP、CsF和叔丁醇鉀。類似於上述結果,BEMP和CsF都提供比DBU更高的Mn。有趣地是,叔丁醇鉀無效,儘管其在溶液中表現出活性。隨後研究溫度對NMP中的基於溶液的聚合的影響。催化劑載量保持恆定在20%DBU。TMS體系如圖5(下方曲線)中所示對加熱不響應,GPCMn為大約35,000g/mol。這種TMS體系的本體聚合預計提高Mn,但僅輕微提高,大約40,000g/mol。相反,TBS體系(圖5,上方曲線)在反應溫度從室溫提高到50℃時表現出顯著的Mn提高。溫度的進一步提高造成Mn輕微提高:在這些提高的溫度下,Mn為大約50,000g/mol。在150℃(所研究的最高溫度)下,可能由於降解,Mn降低。還研究改變催化劑載量的影響。在NMP中在室溫下,無論所用的DBU摩爾%如何,TMS體系(2a+2b)基本沒有表現出GPCMn的變化。在TBS體系中,提高DBU載量造成提高的Mn。類似於溫度從室溫(RT)到50℃的第一次升高,DBU載量從20%到50%的第一次升高使得Mn大幅提升。更多的DBU確實進一步提高Mn,但隨著Mn達到大約50,000至55,000g/mol,提高不那麼明顯。在本體中在150℃下,催化劑載量對Mn沒有明顯的影響,其徘徊在65,000至70,000g/mol的表觀平均值附近。TBS體系比TMS體系(其在提高GPCMn中表現出明顯的限制)更響應不同的條件。在本體中,TBS體系生成最高分子量的聚合物。本體聚合還提供最少的環狀副產物,並可爭辯地是更不浪費和更生態友好的方法。由於這些原因,進一步擴大本體聚合條件的範圍。進一步的研究表明,聚合物的分子量取決於催化劑的性質、其載量和甲矽烷基的性質(表2,圖6)。TBS單體2c始終產生最大的聚合物,在使用BEMP催化劑時GPCMn超過100,000g/mol(表2,條目4-6)。DBU通常產生小於70,000g/mol的聚合物並在低載量下無效(參見條目4和7)。與TBS相比,無論聚合條件如何,由TMS單體2b獲得的聚合物從未超過40,000g/mol。TBDPS(2d)和TIPS(2e)BPA醚在本體中也成功聚合併產生Mn可變的聚硫酸酯(條目11和13),儘管需要較高的BEMP催化劑載量(參見條目10vs.11)。因此,TBS醚2c以「金鳳花(goldilocks)」單體出現,在不同條件下以低催化劑載量提供大聚合物。最後,對若干樣品施以用於測定絕對分子量的多角度光散射(MALS)分析。如對BPA-聚碳酸酯報導,聚苯乙烯標準看起來明顯高估聚硫酸酯的分子量。這對較低分子量聚合物(表2中的條目1-3)尤其明顯,在較高分子量下誤差降至大約兩倍(參見條目4和9)。圖6提供在表2中標作A、B、C和D的聚合物的代表性GPC跡線(分別為條目1、3、8和4)。表2.本體聚合條件的比較對表2的注釋:聚合條件:無溶劑,150℃,2小時(h)。後處理:溶解在DMF中,隨後從甲醇中沉澱。MnMALS是指通過與GPC聯用的多角度光散射測得的Mn。MnPS是指通過參考聚苯乙烯標樣的GPC測得的Mn。n/d=未測定。實施例4.聚(雙酚A硫酸酯)物理性質表徵.評估本實施例中獲得的聚(雙酚A硫酸酯)聚合物的物理性質。對MALSMn為大約2,500、40,000和58,000g/mol的聚合物進行熱重分析(TGA)測量。特別地,使用TAQ5000IRTGA以10℃/min的加熱速率測量BPA-聚硫酸酯樣品的熱分解。使用TAQ2000差示掃描量熱(DSC)裝置測定各種聚合物樣品的玻璃化轉變溫度(Tg)。使用以10℃/min從0℃到220℃的熱/冷/熱程序。Tg取自二次加熱掃描。TGA結果表明聚硫酸酯表現出優異的熱穩定性,如圖7中所示,具有非常類似的降解曲線,其中2,500g/mol樣品的曲線為最低曲線,40,000和58,000g/mol樣品顯示在上方重疊曲線中。隨著Mn提高,熱分解溫度僅輕微提高,但各材料熱穩定:在350℃附近僅發生大約5%重量損失。幾個分開的聚(雙酚A硫酸酯)樣品的代表性DSC溫譜圖在圖8(插圖)中提供,其中從頂部曲線到底部曲線評估MALSMn值分別為2.5kDa、10.6kDa、20kDa、38kDa和58kDa的聚合物。該聚合物的Tg值為大約72至98℃,最低Mn聚合物具有最低Tg,最高Mn聚合物具有最高Tg。沒有識別出結晶熔融峰或結晶峰,表明該BPA聚硫酸酯是非晶的。還發現該芳族硫酸酯骨架水解穩定。圖8還提供Mn相對於Tg的曲線圖。圖8中的數據表明在MALSMn超過大約20kDa(大約60kDa的GPCMn)時大約95至大約100℃的Tg值平臺。這表明該聚(雙酚A硫酸酯)聚合物的大約20kDa的MALSMn(或大約60kDa的GPCMn)代表用於產生完全纏結聚合物的近似最小分子大小。沒有識別出結晶熔融峰或結晶峰,表明受試聚(雙酚A硫酸酯)聚合物是非晶的。還首先通過與多角度光散射(MALS)聯用的GPC和用於測定絕對分子量的差示折光指數(dRI)檢測器使用與下文在實施例11中所述略微不同的分析參數和條件分析該120,000g/molMn樣品(基於對照聚苯乙烯標樣的GPC)。結果(在DMF中的分析)表明該聚合物的分子量為Mn=84,740g/mol;Mw=111,500g/mol;PDI=1.31,這是略高於如下文在實施例11中所述測得的58,000g/mol的值的Mn。這些不同的結果表明聚合物分子量測定對用於分子量測定的具體條件和方法的公知敏感性。因此,對本文描述的聚合物測得的分子量參數可基於用於獲得測量結果的技術而改變。由於相對易於操作和設備的可得性、合適的標準和發展完善的方法,相對GPC分子量據信內部一致並適用於常規評估。實施例5.聚(雙酚A硫酸酯)機械性質評估.將2a和2c的本體聚合擴大至0.5摩爾規模。使用1摩爾%BEMP催化劑在120℃下進行該反應2小時。在反應過程中沒有觀察到內部溫度的顯著變化。以定量收率(145克)獲得Mn為58,000Da(MALS)的BPA-PS。該聚合物輕微可溶於多種多樣的有機溶劑,包括氯仿、二氯甲烷和丙酮,在DMSO和DMF中觀察到最佳溶解度(大約1克/2毫升DMF,在加熱下)。在80℃下用50/5010%NaOH/EtOH溶液處理聚硫酸酯16小時不造成可觀察到的Mn變化,表明與聚碳酸酯相比優異的水解穩定性。將大規模批次的聚(雙酚AA硫酸酯)制粒並壓縮模塑以進行各種物理和機械分析。LEXAN聚碳酸酯樣品在類似條件下壓縮模塑並用於比較。在壓薄時,獲得基本無色、透明和可彎曲但剛性的膜。原始的薄膜/片材用於透氣性測量。更厚的樣品,如用於拉伸強度測量的那些,表現出不透明的褐色。特別地,聚硫酸酯纖維和粉末在200℃下擠過熔體流動指數儀。將薄擠出物冷卻至室溫並用剪刀手動制粒。使用設定在230℃的Carver壓機將聚硫酸酯顆粒壓縮模塑成薄膜和其它樣品模型總共20分鐘(10分鐘無壓力,接著10分鐘在25,000psi下)。將樣品從壓機中取出並在水中淬火。在Carver壓機中在室溫下使用銳鋼「曲奇成型刀(cookiecutter)」模具從聚硫酸酯板上衝壓出拉伸狗骨形試樣。在相同條件下製備未指定等級的BPA-聚碳酸酯(LEXAN)以供比較。評估拉伸性質、透氧率和密度。聚硫酸酯和聚碳酸酯聚合物的工程應力-應變行為都描繪在圖9中。用配有2.5kN測力計的MTSINSIGHT10機電測試框架測量拉伸性質。在環境溫度下以10%/min應變率一式三份進行試驗。使用阿基米德法在室溫下用分析天平測定密度。經4次測量取平均質量並記錄至4個小數位。密度計算至3個小數位,為1.310g/cc。在MOCONOX-TRAN2/21儀器上使用ASTM(D3985)批准的連續流測試槽法(continuous-flowtestingcellmethod)測定該聚合物的透氧率。在兩個分開的BPA-聚硫酸酯膜樣品上都在23℃和0%相對溼度(RH)下進行測量。(a)Sekelik等人,JournalofPolymerSciencePartB:PolymerPhysics1999;37:847-857;和(b)Kwisnek等人,Macromolecules2009,42:7031-7041描述了關於這種方法關注的進一步細節。類似於聚碳酸酯,聚硫酸酯表現出屈服,接著形成燒結頸、穩定化並蔓延。初步看來,至少在所用的具體條件下,聚硫酸酯具有比聚碳酸酯高的模量和略低的屈服應力。聚硫酸酯的致斷應變達到50%以上,但受樣品缺陷限制。真實的伸長可能明顯更高。屈服和燒結頸通常對在環境條件下的熱塑性非晶聚合物而言是不典型的。聚碳酸酯和聚碸是常用的實例。這種觀察結果意味著聚硫酸酯在超過其屈服應力的應力下表現出韌脆轉變,清楚表明這種聚合物是延性但也相當剛性的。較大的模量可能與在環境溫度下聚硫酸酯中存在的較少自由體積有關。透氣率測量(表3)有助於測定自由體積。令人驚訝地發現聚硫酸酯的透氧率比聚碳酸酯低大約5倍,這使聚硫酸酯可用於例如氧敏感材料的包裝用途。降低的透氧率可歸因於較低的自由體積。在環境溫度下,聚硫酸酯具有源自較低Tg的較少過量的空穴自由體積。BPA-聚硫酸酯表現出大約1.310克/立方釐米(g/cc)或比聚碳酸酯緻密大約9%的密度。如含硫聚合物和網絡常見的那樣,重複單元中的重硫原子產生相當緻密的材料。切實而言,聚硫酸酯提供優於聚碳酸酯的其它潛在優點。聚硫酸酯的較低Tg可能易於加工。聚硫酸酯的鹼性穩定性也是優於聚碳酸酯(其已知水解)的顯著改進。表3.BPA-聚硫酸酯和用於比較的BPA-聚碳酸酯(LEXAN)的觀察到的性質實施例6.聚(雙酚A碳酸酯)的製備.圖10提供通過本文描述的方法製備雙酚A聚碳酸酯聚合物的示意性圖示。由雙-三氯甲基碳酸酯(「三光氣」)與氟化鉀和在乙腈中的1.5%18-冠醚-6根據Olofson,TetrahedronLetters,2002;34:4275-4279描述的方法生成氟光氣(COF2)。特別地,在通過冰-水浴冷卻的燒瓶中,將18-冠醚-6(200毫克)在乙腈(5毫升)中的溶液逐滴添加到三光氣(2克,6.8毫摩爾)和噴霧乾燥的KF(3.23克,55毫摩爾)在乙腈(30毫升)中的攪拌混合物中。該燒瓶配有乾冰/丙酮冷指形冷凝器,並將生成的COF2氣體送入含有雙-三甲基甲矽烷基-雙酚A(總共大約1克)在NMP中的1M溶液的反應容器中。通過注射器將大約0.1毫升DBU引入NMP溶液中。在添加DBU時該溶液立即變成深紫色。所得混合物在環境室溫(大約20至22℃)下攪拌大約12小時。該反應混合物形成粘性凝膠,將其在甲醇中稀釋,從而以大致定量收率(大約690毫克)形成灰色纖維狀聚(雙酚A碳酸酯)。通過GPC相對於聚苯乙烯標樣分析該聚碳酸酯,其表現出大約159860的Mw和大約70539的Mn(大約2.27的PDI)。實施例7.附加聚合實施例各種雙官能酚根據與圖2中所示類似的反應流程進行端基轉化和聚合。使用三氟甲基化的BPA單體形成具有良好品質和高分子量的均聚物和共聚物。檢查該聚合反應與不同官能團的相容性。根據與圖2中所示類似的程序製備單體4-13並包括雙酚AF(4a/b)、萘(5a/b)、醚(6a/c)、酯(9a/c和12c)、硫化物(8a/c)、酮(9a/c)、醯胺(10a/c和13c)和雙酚S(碸,11a/c)衍生物。該聚合反應在室溫下在1MNMP中用20摩爾%DBU進行24小時。如表4所示,獲得各種均聚物和BPA共聚物,證實該反應與不同官能團的相容性。如參考聚苯乙烯標樣的觀察到的分子量在相同的一般範圍內,這無法得出關於不同單體種類的相對反應性的結論。在結構類似的BPA-共聚物中,當在甲矽烷基醚單體中存在對位供電子(參見表4中的條目5vs.6,11vs.12)或吸電子(參見8vs.9,14vs.15)基團時,分子量降低。通過含有在其它工程聚合物中發現的技術上有用的嵌段的共聚硫酸酯的成功形成證實該反應的選擇性。也由雙-磺醯氟(條目23)獲得聚合物。由4,4』-聯苯基雙-磺醯氯通過使用在乙腈中的飽和KHF2水溶液在室溫下的便利轉化直接獲得磺醯氟單體14。表4.對表4的注釋:[a]在80℃下的聚合;[b]將溫度提高到100℃提供46,100的GPCMn和1.5的PDI;[c]低聚產物;[d]將溫度提高到100℃提供43,200的GPCMn和1.4的PDI。圖11提供通過本文描述的方法製成的磺醯基和硫酸酯聚合物結構的代表性取樣。除提供獲得具有有用性質和各種結構單元的聚合物的實用途徑外,本文描述的聚(有機硫酸酯)的格外簡易的合成突出了硫酸酯連接體在有機和材料化學中未受到重視的潛力以及氧代氟化硫(VI)的獨特反應性特徵。這種新型點擊反應直接適用於不同學科。實施例8.單體化學計量學的影響甲矽烷基醚-官能和氟代硫酸酯-官能的BPA單體的過量從0.0或無失配逐漸上升至1.0或100%化學計量不平衡以查驗雙-甲矽烷基醚或雙-氟代硫酸酯2a過量時的化學計量失配的影響。這些結果概括在表5中。過量的甲矽烷基醚,在這種情況中為雙-OTBSBPA單體2c導致基於GPC的Mn和PDI降低。Mn的這種降低預計歸因於傳統的逐步生長規則。在幾乎每種情況下獲得超過90%的收率,表明有限的單體完全耗盡。在1.0摩爾過量下,由於較低的低聚物在沉澱過程中的損失,收率明顯更低。在過量氟代硫酸酯單體的情況下,觀察到完全不同的影響。在雙-氟代硫酸酯的0.05摩爾過量下,Mn相當於或優於非失配的對照體系。隨著使用進一步過量的雙-氟代硫酸酯,Mn隨後從這種最大值降低。但是,在每種情況下,Mn高於雙-甲矽烷基醚的相同摩爾當量過量的情況。收率也奇怪地提高,在雙-氟代硫酸酯的最大過量下聚合時達到超過100%。因此對於這種聚合明顯看出,儘管"A-A"(雙-氟代硫酸酯)主要與"B-B"(雙-甲矽烷基醚)反應,A-A也可以與A-A反應。這一結果不僅是傳統的逐步生長聚合規則的一個驚人的例外,所得聚合物還看起來在線性聚合物鏈的兩端上都是氟代硫酸酯官能的。在傳統的逐步生長工程聚合物的情況下,端基通常是A或B官能團的統計混合物。這些基團隨後被單官能試劑封端,或簡單地降解或反應性太弱以致不可用。在沒有任何額外控制或繁瑣轉化的情況下確保逐步生長的聚合物的末端上的穩定易點擊官能團是工程聚合物的一個重要目標。表5.BPA-聚硫酸酯對化學計量不平衡的容許度實施例9.聚合物端基改性.將大約200毫克實施例8(來自表5的條目2)中製成的具有大約71,000g/mol的GPCMn的聚(雙酚A硫酸酯)與如圖12中所示的大約100毫克TBS-保護的尼羅紅染料和大約20微升DBU一起溶解在大約4毫升DMF中。將該混合物在大約40℃下攪拌大約1.5小時以提供包含連接在聚合物端基上的尼羅紅染料的聚合物。通過用大約20毫升甲醇稀釋而使染色的聚合物沉澱。所得沉澱的聚合物具有歸因於尼羅紅端基的特徵性品紅色。通過將染色的聚合物樣品再溶解在DMF中並使用在200至800納米的多種波長下的UV-Vis檢測進行GPC分離,證實染料與該聚合物的共價連接。GPC跡線表明,在567納米檢測器波長下的跡線表現出在與使用聚合物骨架波長(203納米)時相同的洗脫時間的峰。也通過甲矽烷基化尼羅紅染料與染色的聚合物和包含經由硫酸酯鍵連接到單一雙酚A化合物上的單一尼羅紅分子的單體材料的UV-可見光譜的比較證實染料與該聚合物的連接(參見圖13)。該聚合物和雙酚A-尼羅紅共軛化合物具有幾乎相同的UV/Vis光譜,而甲矽烷基化尼羅紅的光譜相對於染色的聚合物和染色的單體材料藍移(參見圖14)。因此,將染料共價連接到聚合物上的能力證實在該聚合物上存在氟代硫酸酯端基。實施例10.氟NMR端基分析.使用19FNMR端基分析獲得聚(雙酚AF硫酸酯)的聚合度(DP)和因此Mn的獨立的近似值。在作為溶劑的NMP中製備這些聚合物樣品,然後溶解在d7-DMF中以用於NMR分析。使用單體混合物的實驗證實,相對於聚合物鏈CF3信號量化OSO2F的端基信號的靈敏度為至少大約1:600(通過峰積分),假設所有聚合物為線性並包括兩個OSO2F端基,這相當於大約200的DP(n)。在NMP中大約1M的濃度下用雙(叔丁基二甲基甲矽烷基)雙酚AF和過量雙(氟代磺醯基)雙酚AF在DBU作為催化劑存在下在環境室溫下進行反應大約16小時。用5種不同量的雙(氟代磺醯基)雙酚AF(5摩爾%、10摩爾%、20摩爾%、50摩爾%和100摩爾%過量)運行實驗。獲自這些評估的DP值是上限,因為任何環狀聚合物/低聚物的存在會使結果偏向更高的表觀DP。5摩爾%過量的雙(氟代磺醯基)雙酚AF提供>200的DP(Mn>大約78000g/mol),即沒有可察覺的端基信號;10摩爾%過量提供大約90的DP(大約35100的Mn);20摩爾%過量提供大約26的DP(大約10140的Mn),50摩爾%過量提供大約13的DP(大約5070的Mn),且100摩爾%過量提供大約7的DP(大約2730的Mn)。本體製備的聚合物樣品(無溶劑)沒有表現出任何可察覺的OSO2F端基信號,表明DP>200和/或可能大環狀結構。實施例11.單體和聚合物合成的詳述Ex.11A.材料和方法除非另行說明,在AMX-400(Bruker)和INOVA-400(Varian)儀器上在295K下記錄1H和13CNMR譜。化學位移(δ)以相對於作為內標的殘留CHCl3、丙酮或DMSO的百萬分之份數表示。在400MHz下記錄質磁共振(1HNMR)譜。在100MHz下記錄碳核磁共振(13CNMR)譜。縮寫為:s,單重峰;d,雙重峰;t,三重峰;q,四重峰;p,五重峰;sex,六重峰;sept,七重峰;app,表觀。在AVATAR370傅立葉變換紅外光譜儀(ThermoNicolet)上記錄紅外光譜並以波數(cm-1)表示。使用熔點裝置(Thomas-Hoover)測定熔點(mp)並且是未校正的。在帶有以電子碰撞(EI+)模式運行的5975CInertMSD系統(Agilent)的7890AGC系統(Agilent)上記錄GCMS數據[To=50℃2.25分鐘;以60℃/min升至300℃;在300℃下保持4分鐘]。在帶有1100SL質譜儀(Agilent;電噴霧電離,ES)的1100LC/MSD(Agilent)上進行HPLC分析,用H2O中的0.1%三氟乙酸和CH3CN中的0.05%三氟乙酸洗脫。預塗布的F-254矽膠板(Merck)用於薄層分析色譜法(TLC)並用短波紫外線或用高錳酸鉀染色劑視覺化。使用EMD(Merck)SilicaGel60(40-63μm)進行柱色譜法。在配有二極體陣列和折光指數檢測器的LC20HPLC系統(Shimadzu)和串聯並置於柱溫箱中的STYRAGELHR-3和HR-4柱(Waters;5微米粒度,7.2毫米直徑)上進行GPC分析。用READYCAL聚苯乙烯標樣(Mn為500g/mol至600,000g/mol)校準該系統,用含有0.1%(wt.)LiBr作為改性劑的HPLC級DMF洗脫。以規則時間間隔驗證校準的準確度。MINIDAWNTREOS檢測器(Wyatt)用於多角度光散射(MALS)分析。除非另行說明,所有原材料和溶劑購自Aldrich,AcrosOrganics,Fisher,TCI,AlfaAesar或StremChemicals並按來樣使用。二甲基甲醯胺(DMF)和N-甲基-2-吡咯烷酮(NMP)作為"在分子篩上99.5%特級乾燥"獲自AcrosOrganics。1,8-二氮雜雙環[5.4.0]十一-7-烯(DBU)獲自AlfaAesar並按來樣使用。2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜-磷雜環己烯(BEMP)作為在己烷中的1M溶液獲自SigmaAldrich。硫醯氟氣體(SO2F2,可以以商品名VIKANE商業生產)是來自DowAgro的贈品。Ex.11B.一般聚合程序(a)小規模本體聚合–(參見表2).A-A(2a;1-5毫摩爾)和B-B(2b-e;1-5毫摩爾)單體在含有Teflon塗布的磁攪拌棒的16mL的厚玻璃壁螺旋蓋容器中合併,並用PTFE/矽酮隔膜密封。然後將這種反應器在攪拌下置於150℃油浴中,一旦單體熔化,引入催化劑以引發聚合。繼續加熱2小時,此時凝固的混合物冷卻並用每克聚合物大約1-2毫升DMF稀釋。通過用熱槍劇烈加熱或通過再引入150℃油浴中,輔助溶解。一旦完全溶解,將DMF溶液倒入每克聚合物大約100毫升甲醇中以使白色BPA-聚硫酸酯根據分子量以纖維或粉末形式沉澱。所得聚合物然後在真空爐中在65℃下乾燥並施以GPC分析。(b)聚合反應中的單體結構容許度–(參見表4).雙(氟代硫酸酯)(4-11a和14;1-3毫摩爾)和雙(甲矽烷基醚)單體(TMS2b,4b-5b和TBS2c,6-13c;1-3毫摩爾)對在配有Teflon塗布的磁攪拌棒的16mL的厚玻璃壁螺旋蓋容器中合併,並用PTFE/矽酮隔膜密封。將這些混合物溶解在1毫升NMP/1毫摩爾底物中(就各單體而言大約1M溶液)並用20摩爾%DBU處理。在室溫下繼續攪拌24小時。然後用熱槍加熱反應混合物以溶解任何沉澱的聚合物並將所得均勻溶液(在一些情況下需要額外的DMF以實現完全溶解)在環境溫度下直接添加到每克聚合物大約100毫升甲醇中以使聚硫酸酯共聚物沉澱。(c)分子量測定.使用GPC測定數均分子量(Mn)、重均分子量(Mw)和多分散性指數(PDI)。使用窄分子量聚苯乙烯標樣校準該系統。對於幾個樣品,使用MINIDAWNTREOS檢測器(Wyatt)測定多角度光散射。流動相是含有0.1%(wt.)LiBr改性劑的HPLC級DMF。對表6中的關鍵聚合物樣品提供代表性的GPC跡線和MALS分析報告。表6.(來自表2的字母名稱)對於MALS分析,通過對聚合物溶液的折光指數相對於改變的溶液濃度作圖,使用分批法測定差示折光指數(dn/dc)。用於溶解用於dn/dc測定和隨後的MALS分析的BPA-聚硫酸酯("樣品D",基於聚苯乙烯標樣,Mn=120,000Da)的流動相是含有0.1%LiBr(wt.)的HPLC級DMF。一式兩份獲得dn/dc。在實驗#1中,測得dn/dc為0.13009。在實驗#2中,測得dn/dc為0.12623(參見表7和圖14,版塊(a)–實驗#1和版塊(b)-實驗#2。表7.Ex.11C.單體製備.下面提供用於製備表4中所用的雙-氟代硫酸酯"AA"單體的示例性的一般程序(即化合物2a的製備)。4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基)二氟代磺酸酯(disulfofluoridate)(2a).在配有攪拌棒的500毫升圓底燒瓶中將雙酚A(1;20克,0.088摩爾)和三乙胺(30毫升,21.8克,0.216摩爾)溶解在CH2Cl2(200毫升)中。排空反應容器的頂空並填充經由與氣球相連的針引入的硫醯氟氣體。該反應在室溫下攪拌12小時,在此期間GC-MS分析表明完全轉化。然後將反應混合物在真空中濃縮,再溶解在300毫升EtOAc中,相繼用300毫升0.6MHCl(1x)、200毫升飽和NaHCO3(1x)、200毫升飽和NaCl(1x)洗滌並經Na2SO4乾燥。除去揮發物以產生黃色油形式的2a,其以白色固體結晶,隨後在真空下乾燥(33.3克,84.9毫摩爾,98%):mp49-52℃;IR(純)λmax1499,1441,1409,1368,1229,1186,1137,1083,1015,949,911,840,812,793,772,599,564,538,502,472cm-1;1HNMR(400MHz,CDCl3)δ7.32-7.25(m,8H),1.71(s,6H);13CNMR(100MHz,CDCl3)δ150.6,148.4,128.9,120.7,43.1,30.9;19FNMR(376MHz,CDCl3)δ37.2;GC-MS(EI)m/z=392.1[M]+。下面給出用於製備表4中所用的雙-甲矽烷基"BB"單體的示例性的一般程序(即化合物2c的製備)。注意將用於化合物2c的HCl洗滌換成用於製備三甲基甲矽烷基單體的附加NaHCO3洗滌。4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(叔丁基二甲基矽烷)(2c).在配有攪拌棒的3升圓底燒瓶中將雙酚A(1;50克,0.219摩爾)、咪唑(45克,0.662摩爾)和4-二甲基氨基吡啶(1.3克,0.11摩爾)溶解在500毫升CH2Cl2和40毫升二甲基甲醯胺的混合物中。將叔丁基二甲基甲矽烷基氯(69克,0.46摩爾)逐份添加到該反應中,其快速導致生成白色沉澱物。將反應混合物攪拌3小時,過濾以除去所有固體(咪唑-HCl)並在真空中濃縮。將所得油溶解在750毫升EtOAc中並相繼用700毫升1MHCl(1x)、400毫升飽和NaHCO3(1x)、500毫升飽和NaCl(1x)洗滌,然後經Na2SO4乾燥。除去揮發物以產生無色油形式的2c,其以無色固體結晶並隨後在真空下乾燥(96.3克,0.211毫摩爾,96%):mp84-87℃;IR(純)λmax2953,1501,1441,1230,1184,1137,1015,911,828,810,773,592,563,539cm-1;1HNMR(400MHz,CDCl3)δ7.07(d,J=8.8Hz,4H),6.72(d,J=8.8Hz,4H),1.62(s,6H),0.98(s,18H),0.19(s,12H);13CNMR(100MHz,CDCl3)δ153.4,143.8,127.8,119.3,41.9,31.2,25.8,18.3,-4.3;GC-MS(EI)m/z=456.4[M]+。(4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(三甲基矽烷)(2b)購自Gelest,Inc.並按來樣使用。由(4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(三甲基矽烷)根據用於製備雙-甲矽烷基"BB"單體的一般程序、用叔丁基二苯基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯,製備(4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(叔丁基二苯基矽烷)(2d)。通過快速色譜法提純(SiO2,0→5%EtOAc-己烷;在10%EtOAc-己烷下Rf=0.5)產生白色結晶固體形式的2d(大約27.8克,39.4毫摩爾,90%):mp94-98℃;IR(純)λmax1501,1442,1230,1164,1138,913,822,797,773,742,700,594,563,541,502cm-1;1HNMR(400MHz,CDCl3)δ7.86(dd,J=1.6,8.0Hz,8H),7.57-7.38(m,12H),7.01(d,J=8.9Hz,4H),6.79(d,J=8.8Hz,4H),1.63(s,6H),1.25(s,18H);13CNMR(100MHz,CDCl3)δ153.4,143.6,135.7,133.3,129.9,127.8,127.6,119.0,41.7,31.1,26.7,19.6;由(4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(三甲基矽烷)根據用於製備雙-甲矽烷基"BB"單體的一般程序、用三異丙基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯,製備(4,4'-(丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(三異丙基矽烷)(2e)。2e作為無色的粘稠油分離(23.1克,42.5毫摩爾,97%):IR(純)λmax2943,2864,1604,1504,1462,1257,1176,1106,1012,912,882,833,743,680,609,559,482cm-1;1HNMR(400MHz,CDCl3)δ7.07(d,J=8.7Hz,4H),6.79(d,J=8.7Hz,4H),1.64(s,6H),1.36-1.18(m,6H),1.13(d,J=7.2Hz,36H);13CNMR(100MHz,CDCl3)δ153.8,143.7,127.8,119.3,41.9,31.3,18.1,12.8;LRMS(EI)m/z=497.4[M–CH(CH3)2]+。雙酚AF(2,2-雙(4-羥基酚)六氟丙烷)獲自OakwoodChemicals並按來樣使用。由雙酚AF根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4,4'-(全氟丙烷-2,2-二基)雙(4,1-亞苯基)二氟代磺酸酯(4a)。4a作為白色結晶固體分離:mp128-130℃;IR(純)λmax1506,1450,1261,1240,1208,1163,1144,1019,968,911,840,805,768,737,697,645,575,536cm-1;1HNMR(400MHz,CDCl3)δ7.53(appd,J=9.0Hz,4H),7.42(dd,J=0.6,9.2Hz,4H);13CNMR(100MHz,CDCl3)δ150.4,133.6,132.6,123.7(q,J=E287.5Hz),121.3,64.2(appt,J=25.8Hz);19FNMR(376MHz,CDCl3)δ38.2,-64.1;LRMS(EI)m/z=500.0[M]+。由雙酚AF根據用於製備雙-甲矽烷基"BB"單體的一般程序、用三甲基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯並省略HCl洗滌,製備(4,4'-(全氟丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(三甲基矽烷)(4b)。4b作為米黃色固體分離:mp46-50℃;IR(純)λmax2959,1611,1513,1450,1242,1204,1168,1135,967,912,828,753,737,700,545,505cm-1;1HNMR(400MHz,CDCl3)δ7.25(d,J=9.2Hz,4H),6.81(d,J=9.1Hz,4H),0.29(s,4H);13CNMR(100MHz,CDCl3)δ155.9,131.7,126.4,124.6(q,J=287.8Hz),119.6,63.9(t,J=25.5Hz),-0.32;19FNMR(376MHz,CDCl3)δ-64.4;LRMS(EI)m/z=480.2[M]+。由雙酚AF根據用於製備雙-甲矽烷基"BB"單體的一般程序製備(4,4'-(全氟丙烷-2,2-二基)雙(4,1-亞苯基))雙(氧基)雙(叔丁基二甲基矽烷)4c。4c作為白色結晶固體分離:mp167-170℃;IR(純)λmax2952,2932,2859,1611,1513,1468,1275,1244,1202,1168,1134,968,911,830,804,777,727,701,667,556cm-1;1HNMR(400MHz,CDCl3)δ7.24(d,J=8.7,4H),6.80(d,J=9.0Hz,4H),0.99(s,18H),0.23(s,12H);13CNMR(100MHz,CDCl3)δ156.2,131.7,126.3,124.6(appd,J=285.1Hz),119.6,63.8(t,J=25.2Hz),25.8,18.3,-4.3;19FNMR(376MHz,CDCl3)δ-64.4;LRMS(EI)m/z=451.0[M–Si(Me)2t-Bu]+。萘-2,7-二醇購自AcrosOrganics並按來樣使用。由萘-2,7-二醇根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備萘-2,7-二基二氟代磺酸酯5a。5a作為白色粉末分離(12.3克,38毫摩爾,87%):mp122-124℃;IR(純)λmax1439,1365,1219,1187,1137,1115,960,922,896,839,801,637,582,530,470cm-1;1HNMR(400MHz,DMSO-d6)δ8.36(d,J=2.2Hz,2H),8.28(d,J=9.1Hz,2H),7.82(dd,J=2.4,9.1Hz,2H);13CNMR(100MHz,DMSO-d6)δ148.3,133.3,131.6,120.9,119.5;19FNMR(376MHz,DMSO-d6)δ38.1;LRMS(EI)m/z=324.0[M]+。由萘-2,7-二醇根據用於製備雙-甲矽烷基"BB"單體的一般程序、用三甲基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯,製備2,7-雙(三甲基甲矽烷氧基)萘5b。5b作為黃色油分離(13.1克,43.5毫摩爾,99%):IR(純)λmax2958,2856,1630,1604,1507,1460,1427,1365,1250,1211,1151,1110,909,833,743,697,612,489cm-1;1HNMR(400MHz,CDCl3)δ7.69(d,J=8.9Hz,2H),7.12(d,J=2.3Hz,2H),6.99(dd,J=2.3,8.8Hz,2H),0.37(s,18H);13CNMR(100MHz,CDCl3)δ153.6,136.2,129.3,125.4,120.0,114.0,-0.42;LRMS(EI)m/z=304.1[M]+。4,4'-氧基聯苯酚購自AKScientific並按來樣使用。由4,4'-氧基聯苯酚根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4,4'-氧基雙(4,1-亞苯基)二氟代磺酸酯6a。6a作為白色結晶固體分離(8.2克,22.5毫摩爾,75%):mp53-55℃;IR(純)λmax1499,1443,1230,1162,1132,1100,909,839,818,768,754,602,540,501cm-1;1HNMR(400MHz,CDCl3)δ7.36(dtd,J=0.9,3.7,10.6Hz,4H),7.11(dt,J=3.7,9.3Hz,4H);13CNMR(100MHz,CDCl3)δ156.4,145.8,122.9,120.6;19FNMR(376MHz,CDCl3)δ36.9;LRMS(EI)m/z=366.0[M]+。由4,4'-氧基聯苯酚根據用於製備雙-甲矽烷基"BB"單體的一般程序製備(4,4'-氧基雙(4,1-亞苯基)雙(氧基))雙(叔丁基二甲基矽烷)(6c)。6c作為清澈無色的粘稠油分離(11.9克,27.8毫摩爾,93%):IR(純)λmax2930,2857,1491,1451,1251,1213,1144,1096,908,871,835,778,691,504cm-1;1HNMR(400MHz,CDCl3)δ6.89-6.82(m,4H),6.80-6.77(m,4H),0.99(s,18H),0.19(s,12H);13CNMR(100MHz,CDCl3)δ152.1,151.3,120.9,119.6,25.8,18.3,-4.3;LRMS(EI)m/z=430.3[M]+。如Goldfinger等人在WO2009023759A2中所述通過氫醌與4-羥基苯甲酸的縮合製備4-羥基苯甲酸4-羥苯酯。由4-羥基苯甲酸4-羥苯酯根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4-(氟磺醯氧基)苯甲酸4-(氟磺醯氧基)苯酯(7a)。通過快速色譜法提純(SiO2,5→15%EtOAc-己烷;在20%EtOAc-己烷下Rf=0.52)產生白色粉末形式的7a(1.77克,4.5毫摩爾,45%):mp103-105℃;IR(純)λmax1740,1497,1443,1260,1230,1135,1068,1015,909,801,757,689,612,540,491cm-1;1HNMR(400MHz,CDCl3)δ8.34(d,J=9.0Hz,1H),7.52(dd,J=0.7,9.0,1H),7.47-7.40(m,1H),7.36(d,J=9.3Hz,1H);13CNMR(100MHz,CDCl3)δ163.2,153.6,150.3,147.5,132.9,129.5,123.7,122.5,121.5;19FNMR(376MHz,CDCl3)δ38.8,37.24;LRMS(EI)m/z=393.8[M]+。由4-羥基苯甲酸4-羥苯酯根據用於製備雙-甲矽烷基"BB"單體的一般程序製備4-(叔丁基二甲基甲矽烷氧基)苯甲酸4-(叔丁基二甲基甲矽烷氧基)苯基酯(7c)。通過快速色譜法提純(SiO2,2%EtOAc-己烷;在5%EtOAc-己烷下的Rf=0.56)產生白色粉末形式的7c(2.05克,4.4毫摩爾,45%):mp69-73℃;IR(純)λmax2956,2928,2857,1737,1601,1501,1442,1252,1232,1187,1160,1067,1010,904,822,782,692,540,501cm-1;1HNMR(400MHz,CDCl3)δ8.10(d,J=8.9Hz,2H),7.06(d,J=9.0Hz,2H),6.93(d,J=8.9Hz,2H),6.87(d,J=9.0Hz,2H),1.01(s,9H),1.00(s,9H),0.26(s,6H),0.22(s,6H);13CNMR(100MHz,CDCl3)δ165.3,160.7,153.3,145.2,132.3,122.8,122.6,120.7,120.2,25.8,25.8,18.4,18.3,-4.2,-4.3;LRMS(EI)m/z=458.2[M]+。4,4'-硫代二苯酚購自AlfaAesar並按來樣使用。由4,4'-硫代二苯酚根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4,4'-硫代雙(4,1-亞苯基)二氟代磺酸酯(8a)。8a作為灰白色結晶固體分離(17.1克,44.7毫摩爾,98%):mp54-56℃;IR(純)λmax1485,1442,1230,1177,1139,1101,1014,909,835,803,769,581,540,496cm-1;1HNMR(400MHz,CDCl3)δ7.44(d,J=9.0Hz,4H),7.32(dd,J=0.9,9.0Hz,4H);13CNMR(100MHz,CDCl3)δ149.3,136.2,133.0,122.2;19FNMR(376MHz,CDCl3)δ37.7;LRMS(EI)m/z=382.0[M]+。由4,4'-硫代二苯酚根據用於製備雙-甲矽烷基"BB"單體的一般程序製備(4,4'-硫代雙(4,1-亞苯基)雙(氧基))雙(叔丁基二甲基矽烷)(9c)。9c作為清澈無色的粘稠油分離(20.3克,46毫摩爾,99%):IR(純)λmax2929,2856,1586,1485,1444,1254,1231,1140,1072,1013,907,821,804,772,739,673,585,521,498cm-1;1HNMR(400MHz,CDCl3)δ7.20(d,J=8.7Hz,2H),6.77(d,J=8.7Hz,2H),0.98(s,9H),0.19(s,6H);13CNMR(100MHz,CDCl3)δ155.2,132.7,128.1,121.0,25.8,18.3,-4.3;LRMS(EI)m/z=446.3[M]+。雙(4-羥苯基)甲酮購自AKScientific並按來樣使用。由雙(4-羥苯基)甲酮根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4,4'-羰基雙(4,1-亞苯基)二氟代磺酸酯(9a)。9a作為白色結晶固體分離(11.1克,29.3毫摩爾,98%):mp91-94℃;IR(純)λmax1672,1591,1440,1409,1268,1231,1138,1015,907,808,761,667,632,540,494,466cm-1;1HNMR(400MHz,CDCl3)δ7.97-7.87(m,4H),7.60-7.45(m,4H);13CNMR(100MHz,CDCl3)δ192.8,152.7,137.0,132.3,121.3;19FNMR(376MHz,CDCl3)δ38.6;LRMS(EI)m/z=378.0[M]+。由雙(4-羥苯基)甲酮根據用於製備雙-甲矽烷基"BB"單體的一般程序製備雙(4-(叔丁基二甲基甲矽烷氧基)苯基)甲酮(9c)。9c作為無色低熔點固體分離(13.3克,30毫摩爾,99%):IR(純)λmax2960,2930,2857,1651,1596,1505,1466,1254,1160,1105,904,836,803,773,713,682,494cm-1;1HNMR(400MHz,CDCl3)δ7.73(appd,J=8.8Hz,4H),6.90(appd),J=8.8Hz,4H),1.00(s,18H),0.25(s,12H);13CNMR(100MHz,CDCl3)δ194.9,159.7,132.3,131.4,119.8,25.7,18.4,-4.2;LRMS(EI)m/z=442.3[M]+。由4-羥基苯甲酸和4-氨基酚如(a)C.H.C.Loch,J.-Y.Guan,G.Siegal,M.Overhand,ChemMedChem2007,2,1054-1070;(b)P.W.Elsinghorst,J.S.Cieslik,K.Mohr,C.M.Gütschow,JournalofMedicinalChemistry2007,50,5685-5695所述以四個步驟製備4-羥基-(4-羥苯基)苯甲醯胺。由4-羥基-(4-羥苯基)苯甲醯胺根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4-(氟磺醯氧基)-N-(4-(氟磺醯氧基)苯基)苯甲醯胺(10a)。通過快速色譜法提純產生白色粉末形式的10a(1.86克,4.7毫摩爾,50%):mp160-167℃;IR(純)λmax3417,1677,1600,1524,1503,1437,1405,1309,1258,1225,1176,1138,1104,1018,910,864,849,833,804,775,694,616,542,510,469cm-1;1HNMR(400MHz,CDCl3)δ10.70(s,1H),8.15(d,J=8.9Hz,2H),7.96(d,J=9.3Hz,2H),7.80(d,J=8.6Hz,2H),7.60(d,J=9.0Hz,2H);13CNMR(100MHz,CDCl3)δ164.5,151.5,145.2,139.5,135.4,130.6,121.9,121.4;19FNMR(376MHz,CDCl3)δ39.6,38.27;LRMS(EI)m/z=393.0[M]+。由4-羥基-(4-羥苯基)苯甲醯胺根據用於製備雙-甲矽烷基"BB"單體的一般程序製備4-(叔丁基二甲基甲矽烷氧基)-N-(4-(叔丁基二甲基甲矽烷氧基)苯基)苯甲醯胺(10c)。通過快速色譜法提純產生白色粉末形式的10c(2.26克,4.9毫摩爾,61%):mp209-210℃;IR(純)λmax3298,2952,2929,2889,2856,1640,1603,1505,1469,1406,1254,1168,1101,1009,909,833,777,733,690,505cm-1;1HNMR(400MHz,CDCl3)δ7.81(s,1H),7.75(d,J=8.7Hz,2H),7.46(d,J=8.8Hz,2H),6.88(d,J=8.6Hz,2H),6.81(d,J=8.8Hz,2H),0.99(s,9H),0.98(s,9H),0.22(s,6H),0.19(s,6H);13CNMR(100MHz,CDCl3)δ165.4,159.0,152.5,131.9,128.9,128.0,122.0,120.5,120.3,25.7,25.7,18.4,18.3,4.3,4.3;LRMS(EI)m/z=457.3[M]+。4,4'-磺醯基聯苯酚購自AlfaAesar並按來樣使用。由4,4'-磺醯基聯苯酚根據用於製備雙-氟代硫酸酯"AA"單體的一般程序製備4,4'-磺醯基雙(4,1-亞苯基)二氟代磺酸酯(11a)。11a作為白色粉末分離(7.5克,91%):mp118-122℃;IR(純)λmax1586,1486,1451,1405,1324,1291,1231,1178,1139,1103,1015,907,850,810,783,688,589,574,538,509,466cm-1;1HNMR(400MHz,CDCl3)δ8.10(d,J=9.1Hz,4H),7.53(d,J=8.3Hz,1H);13CNMR(100MHz,CDCl3)δ153.1,141.3,130.7,122.5;19FNMR(376MHz,CDCl3)δ39.2;LRMS(EI)m/z=413.9[M]+。由4,4'-磺醯基聯苯酚根據用於製備雙-甲矽烷基"BB"單體的一般程序、用三甲基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯,製備(4,4'-磺醯基雙(4,1-亞苯基)雙(氧基))雙(叔丁基二甲基矽烷)(11c)。11c作為白色粉末分離(8.8克,92%):mp135-137℃;IR(純)λmax2930,2857,1587,1492,1469,1314,1273,1151,1105,902,838,781,757,679,645,616,574,542cm-1;1HNMR(400MHz,CDCl3)δ7.79(d,J=8.8Hz,4H),6.88(d,J=8.8Hz,4H),0.96(s,18H),0.2(s,12H);13CNMR(100MHz,CDCl3)δ160.0,134.5,129.6,120.1,25.6,18.3,-4.3;LRMS(EI)m/z=478.2[M]+。由酚酞根據用於製備雙-甲矽烷基"BB"單體的一般程序、用三甲基甲矽烷基氯取代叔丁基二甲基甲矽烷基氯,製備4,4'-(3-氧代-1,3-二氫異苯並呋喃-1,1-二基)雙(4,1-亞苯基)二氟代磺酸酯(12a)。12a作為白色固體分離:mp93-98℃;IR(純)λmax1761,1500,1443,1410,1288,1229,1139,1081,1016,974,938,906,846,802,753,691,638,571,534,503,476cm-1;1HNMR(400MHz,CDCl3)δ8.00(ddd,J=0.8,1.1,7.7Hz,1H),7.79(td,J=1.2,7.5Hz,1H),7.65(td,J=0.9,7.5Hz,1H),7.57(dt,J=0.8,7.8Hz,1H),7.47(d,J=9.1Hz,4H),7.35(dd,J=0.8,9.1Hz,4H);13CNMR(100MHz,CDCl3)δ168.7,150.4,150.2,141.1,135.0,130.4,129.4,126.8,125.4,124.0,121.5,89.7;19FNMR(376MHz,CDCl3)δ37.9;LRMS(EI)m/z=489.1[M]+。通過3,5-二羥基苯甲酸的全面TBS保護、接著如M.E.El-Khouly,E.S.Kang,K.-Y.Kay,C.S.Choi,Y.Aaraki,O.Ito,Chem.Eur.J.2007,13,2854-2863所述選擇性釋放酸部分,製備3,5-雙(叔丁基二甲基甲矽烷氧基)苯甲酸。丁基-3,5-雙(叔丁基二甲基甲矽烷氧基)苯甲醯胺(13c).在配有攪拌棒和橡膠隔膜的50毫升圓底燒瓶中裝入3,5-雙(叔丁基二甲基甲矽烷氧基)苯甲酸(0.76克,2.0毫摩爾)並置於氬氣下。加入15毫升無水DCM,接著通過部分移除隔膜,依序添加羥基苯並三唑(HOBT;0.3克,2.2毫摩爾)和N,N'-二環己基碳二亞胺(DCC;0.45克,2.2毫摩爾)。將所得漿料在室溫下攪拌10分鐘。然後逐滴加入丁-1-胺(0.3毫升,0.22克,3.0毫摩爾)並將反應混合物攪拌整夜。所得不均勻溶液然後經Buchner漏鬥過濾,濾液用DCM進一步稀釋並用0.5MHCl洗滌。水層再次用DCM萃取,合併的有機物經Na2SO4乾燥。該粗製反應混合物隨後通過旋轉蒸發濃縮到矽膠上並施以快速色譜法(SiO2,10%EtOAc-己烷;在10%EtOAc-己烷下的Rf=0.3)以提供白色結晶固體形式的13c(0.76克,1.8毫摩爾):mp114-117℃;IR(純)λmax3294,2929,2857,1632,1583,1543,1438,1334,1253,1163,1027,1004,935,829,778,692,667,486cm-1;1HNMR(400MHz,CDCl3)δ6.81(d,J=2.1Hz,2H),6.43(t,J=2.1Hz,1H),6.02(apps,1H),3.41(q,J=7.1Hz,2H),1.58(p,J=7.7Hz,2H),1.39(sex,J=7.2Hz,2H),0.97(s,18H),0.95(t,J=7.3Hz,3H),0.19(s,12H);13CNMR(100MHz,CDCl3)δ167.3,156.8,137.1,114.9,112.1,39.9,31.8,25.8,20.3,18.3,13.9,-4.3;LRMS(EI)m/z=437.3[M]+。聯苯基-4,4'-二磺醯基二氟(14).在攪拌下將聯苯基-4,4'-二磺醯基氯(購自TCIchemicals;5.0克,0.014摩爾)溶解在40毫升乙腈和5毫升水中。向這種混合物中加入4當量飽和KHF2水溶液(1.2克)。使該反應進行3小時。該混合物用30毫升乙酸乙酯萃取兩次。合併有機餾分,用水、鹽水洗滌,然後經MgSO4乾燥。在真空下除去溶劑以提供黃色固體形式的14(4.1克,90%):mp194-197℃;IR(純)λmax1589,1405,1205,1095,816,771,750,709,569,535,493cm-1;1HNMR(400MHz,CDCl3)δ8.16(d,J=8.5Hz,4H),7.88(dd,J=0.7,8.7Hz,4H);13CNMR(100MHz,CDCl3)δ145.9,133.4(d,J=15.2Hz),129.4,128.9;19FNMR(376MHz,CDCl3)δ66.1;LRMS(EI)m/z=318.0[M]+。實施例12.通過苯基氟代硫酸酯(15)和叔丁基二甲基(對甲苯氧基)矽烷(16)的反應篩選催化劑實驗安排:以下列方式製備原料試劑的0.5M乙腈儲液:將苯基氟代硫酸酯(15)(2.667克,12.0毫摩爾)、叔丁基二甲基(對甲苯氧基)矽烷(16)(2.112克,12.0毫摩爾)和二苯基甲烷(標準,0.403克,2.4毫摩爾)溶解在足夠的無水乙腈中以獲得24毫升(總毫升數)儲液,其隨後置於氬氣氣氛下。將0.4毫升等分試樣分配到1毫升閃爍管中,由此提供60個單獨的0.2毫摩爾反應。然後將大約10或20摩爾%如表8中所示的催化劑添加到反應瓶中。用氬氣吹掃頂空並將反應混合物在室溫下搖振24小時。最後,將各反應混合物的15微升等分試樣用1毫升EtOAc稀釋並施以GC/MS終點分析以測定苯基甲苯基硫酸酯(17)和任何副產物4-甲基酚(18)的收率(如果有的話)。表8中所示的計算終點未通過分離證實,並被視為「粗製」。表8中所示的百分比可改變±5%並意在充當用於這一反應的有效催化劑的一般概況。表8.在表8中,測得催化劑量盡實際可能地接近10或20摩爾%。由衍生自化合物17的基於摩爾濃度的校準曲線計算粗製反應混合物中的產物百分比。收率可改變±5%。由參考二苯甲烷(內標)的初始反應混合物濃度推導出剩餘原材料百分比。15和16的實際收率可改變±5%。4-甲基酚18的百分比參考原材料16,即18的實際收率可改變±5%。在一些情況下,觀察到的產物是酚和哌啶的混合硫酸酯/氨磺醯基衍生物(化合物19)或二苯基硫酸酯20。實施例13.本聚合方法與Firth(US3,733,304)的用於製備聚(雙酚A硫酸酯)的方法的比較.通過Firth(US3,733,304)的方法,即通過二鈉雙酚A與雙酚A-雙氟代硫酸酯在氯苯中在大約150至165℃下的反應製備聚(雙酚A硫酸酯)。所得產物如Firth所述沉澱到水中,然後如本文所述通過GPC相對於聚苯乙烯標樣分析。GPC跡線顯示在圖15的版塊A中。當與在大約22分鐘洗脫時間的環狀低聚物峰結合時,根據Firth方法製成的聚合物的多分散性為大約6。為了比較,根據本發明製備的來自本文中的實施例1中的大規模製備的聚(雙酚A硫酸酯)的GPC顯示在圖15的版塊B中。由這兩個GPC跡線清楚看出,本方法提供具有窄得多的多分散性的更高分子量產物和明顯更少的環狀低聚副產物。實施例14.聚(雙酚A硫酸酯)在各種加工條件下的穩定性在本體無溶劑條件下(單體2a和2c的純熔體,無溶劑,使用1%BEMP催化劑,在120℃下)在2毫摩爾、20毫摩爾和250毫摩爾規模下製備聚(雙酚A硫酸酯)。將聚合物樣品溶解在DMF中並將這些材料的GPC跡線與來自實施例5的薄膜(由實施例1的大規模聚合物製成)的再溶解樣品進行比較。GPC跡線顯示在圖16中並清楚表明在各規模下都獲得具有基本相同的分子量狀況的聚合物。還顯示,將該聚合物加工成膜不會明顯影響分子量狀況。此外,用熱槍長時間加熱來自實施例1的大規模聚合物的樣品,加熱另一樣品並壓過0.45微米過濾器,它們都沒有明顯影響樣品的分子量狀況(參見圖16)。實施例15.由雙-甲矽烷基-雙酚A和硫醯氟製備聚(雙酚A硫酸酯)含有磨砂玻璃旋塞、配有攪拌棒和橡膠隔膜的100毫升Schlenk燒瓶在真空(7mmHg)下火焰乾燥。在冷卻至室溫後,將反應容器稱重(無內部氣氛),充入硫醯氟氣體(SO2F2)並最後再稱重以測定SO2F2的量(752毫克,7.37毫摩爾)。然後將溶解在7毫升無水DMF中的((丙烷-2,2-二基雙(4,1-亞苯基))雙(氧基))雙(叔丁基二甲基矽烷)(3.30克,7.22毫摩爾)和1M溶液形式的在己烷中的2-叔丁基亞氨基-2-二乙基氨基-1,3-二甲基全氫化-1,3,2-二氮雜磷雜環己烯(BEMP;368微升,101毫克,0.368毫摩爾)依序添加到反應容器中並作為封閉(對大氣封閉)系統將所得混合物在室溫下攪拌20分鐘。然後將反應容器置於150℃油浴中並在此後不久在反應容器的壁上可見到低沸點溶劑(可能是己烷和叔丁基氟二甲基矽烷(TBSF))的析出。該反應作為封閉系統在150℃下進行30分鐘,此時打開旋塞,由此釋放氣態己烷和TBSF,然後作為開放系統繼續加熱另外2小時。然後從油浴中取出粘稠淺黃色清澈液體形式的反應混合物,並使其冷卻至室溫。將反應混合物直接添加到200毫升MeOH中導致BPA-聚硫酸酯作為白色纖維狀固體沉澱。在真空下在80℃下乾燥3小時得到1.966克(94%),基於聚苯乙烯標樣的Mn為95,000Da。實施例16.由伯胺通過與乙烯磺醯基氟(ESF)反應製備的氟磺醯基單體圖17,版塊A圖解通過伯胺與ESF在DCM或乙酸中的反應便利地合成雙(2-氟磺醯基乙基)胺。圖17的版塊B圖解由此方式製備的此類單體的四個實例。圖17,版塊C圖解由這些單體和雙-甲矽烷基-雙酚A單體製成的聚合物的一些實例。ESF與伯胺和仲胺的反應的一般程序.將原料胺(1當量)溶解在DCM(在底物中大約0.1至0.5M)中並根據修改自Hyatt等人(J.Org.Chem.,1979,44:3847-3858)的程序用ESF(大約1至2.5當量)處理。將反應混合物在室溫下攪拌幾分鐘至1小時,通過LCMS監測轉化。在完成後,使用旋轉蒸發器除去DCM和過量ESF並乾燥,以提供基本不含任何雜質的產物。在某些情況中,可以使用柱色譜法獲得ESF加合物的分析純的樣品。2,2'-((2-(1H-吲哚-3-基)乙基)氮烷二基)二乙磺醯氟:根據上述一般程序,使用2當量ESF並將反應混合物在室溫下攪拌3小時,以提供通過快速柱色譜法(己烷/EtOAc–9/1至6/4)獲得的分析純的樣品。產物以黃色油形式以定量收率(1.9克)獲得。1HNMR(400MHz,CDCl3)δ(ppm):8.04(s,1H),7.57(d,J=7.8Hz,1H),7.37(d,J=7.9Hz,1H),7.23(t,J=7.5Hz,1H),7.16(t,J=7.4Hz,1H),7.01(brs,1H),3.48–3.39(m,4H),3.15–3.05(m,4H),2.96–2.89(m,2H),2.89–2.80(m,2H);13CNMR(101MHz,CDCl3)δ(ppm):136.3,127.1,122.3,122.2,122.1,119.6,118.5,113.0,111.5,54.2,49.4(d,J=13.2Hz),47.9,23.3;19FNMR(376MHz,CDCl3)δ(ppm):+57.9;Rf(己烷/EtOAc-7/3):0.27;ESI-MS(m/z):381[MH]+。2,2'-((呋喃-2-基甲基)氮烷二基)二乙磺醯氟:根據上述一般程序,在DCM(0.33M)中在2當量ESF存在下,以提供粗產物,其通過柱色譜法(己烷/EtOAc–95/5至7/3)提純。產物以黃色油形式以99%收率(1.6克)獲得。1HNMR(400MHz,CDCl3)δ(ppm):7.41(dd,J=1.9,0.8Hz,1H),6.37(dd,J=3.2,1.9Hz,1H),6.28(dd,J=3.2,0.7Hz,1H),3.81(s,2H),3.53(td,J=6.9,3.6Hz,4H),3.16(td,J=7.0,1.2Hz,4H);13CNMR(101MHz,CDCl3)δ(ppm):149.9,143.1,110.7,110.1,49.6,49.4(d,J=11.1Hz),47.9;19FNMR(376MHz,CDCl3)δ(ppm):+57.9;Rf(己烷/EtOAc–7/3):0.47;ESI-MS(m/z):340[MNa]+。2,2'-((3-乙炔基苯基)氮烷二基)二乙磺醯氟(修改自Hyatt等人J.Org.Chem.,1979,44:3847-3858):將ESF(1.8毫升;20毫摩爾)添加到在冰醋酸(3毫升)中的苯胺(1.17克;10毫摩爾)中並將反應混合物在50℃下攪拌24小時。在完成後,通過過濾分離粗產物,用己烷洗滌並從CCl4-DCM中重結晶。產物以淺棕色晶體形式以87%收率(2.94克)獲得。m.p.98-100℃.1HNMR(400MHz,CDCl3)δ(ppm):7.31(t,J=8.0Hz,1H),7.10–7.06(m,1H),6.85–6.82(m,1H),6.78–6.73(m,1H),4.01(t,J=6.4Hz,4H),3.67–3.59(m,4H),3.10(s,1H);13CNMR(101MHz,CDCl3)δ(ppm):144.0,130.5,124.3,124.2,117.6,115.0,83.3,78.0,48.3(d,J=14.4Hz),46.8;19FNMR(376MHz,CDCl3)δ(ppm):+57.2;ESI-MS(m/z):338[MH]+。用於ESF與磺醯胺和醇的反應的一般程序:將原材料(1當量)和三苯膦(0.1當量)溶解在DCM(在底物中0.33M)中並用ESF(大約1至2.5當量)處理。反應混合物在室溫下攪拌整夜,通過LCMS/GCMS/TLC監測轉化。在完成後,使用旋轉蒸發器除去DCM和過量ESF並通過短柱色譜法提純粗產物。根據用於ESF與磺醯胺的反應的一般程序,以白色固體形式以78%收率(251毫克)獲得2-(4-甲基-N-(丙-2-炔-1-基)苯基磺醯氨基)乙磺醯氟。Rf(己烷/EtOAc–5/1):0.25;m.p.125-126℃;1HNMR(400MHz,CDCl3)δ(ppm):7.74(d,J=8.3Hz,2H),7.35(d,J=8.5Hz,2H),4.15(d,J=2.5Hz,2H),3.87–3.80(m,2H),3.71–3.65(m,2H),2.45(s,3H),2.19(t,J=2.5Hz,1H);13CNMR(101MHz,CDCl3)δ(ppm):144.8,134.5,130.1,127.9,76.2,75.0,50.4(d,J=16.0Hz),41.9,38.8,21.8;19FNMR(376MHz,CDCl3)δ(ppm):55.9;ESI-MS(m/z):320[MH]+。根據用於ESF與磺醯胺的反應的一般程序,以白色固體形式以60%收率(175毫克)獲得2,2'-(((4-(3-苯基-5-(三氟甲基)-1H-吡唑-1-基)苯基)磺醯基)氮烷二基)-二乙磺醯氟。Rf(己烷/EtOAc–5/1):0.21;m.p.135-137℃;1HNMR(400MHz,CDCl3)δ(ppm):7.84(d,J=8.6Hz,2H),7.58(d,J=8.6Hz,2H),7.47–7.43(m,1H),7.43–7.39(m,1H),7.28–7.23(m,3H),6.80(s,1H),3.86–3.80(m,4H),3.71–3.66(m,4H);13CNMR(101MHz,CDCl3)δ(ppm):145.4,144.8(d,J=38.3Hz),143.9,135.7,130.0,129.4,129.0,128.8,128.6,117.4(d,J=336.3Hz),107.2,50.7,50.6(d,J=16.1Hz),45.6;19FNMR(376MHz,CDCl3)δ(ppm):+59.4,-62.8;ESI-MS(m/z):588[MH]+。本文中引用的所有參考資料,包括出版物、專利申請和專利經此引用併入本文,就像各參考資料被逐一和明確地指出經此引用併入本文並全文闡述在本文中。在本文中描述了本發明的優選實施方案,包括發明人已知的實施本發明的最佳方式。這些優選實施方案的變動是本領域普通技術人員在閱讀上文的描述時顯而易見的。發明人期望技術人員酌情利用這樣的變動,且發明人預計到以不同於本文中明確描述的方式實施本發明。因此,本發明包括所附權利要求書中列舉的主題的視適用法律允許的所有修改和等同物。此外,除非本文中另行規定或除非明顯與上下文相悖,本發明包括上述要素在其所有可能的變動下的任何組合。
