一種烏苯美司的製備方法與流程
2023-05-28 05:01:41 2
本發明涉及製藥領域,具體而言,涉及一種烏苯美司的製備方法。
背景技術:
烏苯美司(iubenimex;nn),也稱為bestatin,化學式為n-[(2s,3r)-3-氨基-2-羥基-4-苯基丁醯基]-l-亮氨酸,是一種競爭性的,可逆的蛋白酶抑制劑。它對精氨醯氨基肽酶(氨基肽酶b),白三烯a4水解酶(顯示環氧化物水解酶和氨基肽酶活性的鋅金屬蛋白酶),丙氨醯氨基肽酶(氨肽酶m/n),亮氨醯/胱氨醯氨基肽酶(催產素/血管加壓素酶)(白三烯d4水解酶)有抑制作用。正在研究用於治療急性骨髓性白血病。它源自橄欖鏈黴菌(streptomycesolivoreticuli)。已發現ubenimex抑制催產素,加壓素,腦啡肽和各種其它肽和化合物的酶促降解。
烏苯美司可增強免疫功能,用於抗癌化療、放療的輔助治療,老年性免疫功能缺陷等。可配合化療、放療及聯合應用於白血病、多發性骨髓瘤、骨髓增生異常綜合症及造血幹細胞移植後,以及其它實體瘤患者。
現有技術中,烏苯美司在合成過程中大多採用四氫呋喃、三乙胺作為溶劑或者催化劑等,這些試劑本身不環保,後續處理負擔比較大,會產生大量的廢水廢氣,而且三乙胺這種有機鹼容易殘留在產物中,造成有機溶劑殘留的問題。
有鑑於此,特提出本發明。
技術實現要素:
本發明的第一目的在於提供一種烏苯美司的製備方法,該製備方法中摒棄了以往採用的有機鹼、四氫呋喃、二氯甲烷、n、n二甲基甲醯胺等有機溶劑作為反應溶劑、乙酸乙酯作為萃取溶劑。直接採用乙酸乙酯作為反應和萃取溶劑,節約了成本同時避免了使用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺所帶來的安全環保隱患,採用弱酸強鹼無機鹽作為鹼催化劑,降低了成本,同時避免三乙胺殘留溶劑對成品質量的影響,整個製備方法過程中充分做到了避免使用有機溶劑,操作簡便,綠色環保,在提高了烏苯美司產品質量的同時,收率高。
為了實現本發明的上述目的,特採用以下技術方案:
本發明提供了一種烏苯美司的製備方法,包括如下步驟:
(a)dcc(二環己基碳二亞胺)催化條件下,溶劑為乙酸乙酯,將l-亮氨酸苄酯對甲苯磺酸鹽、hobt(1-羥基苯並三氮唑)縮合得到活化酯溶液;
(b)將(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸、弱酸強鹼無機鹽混合攪拌過程中,滴加所述活化酯溶液進行反應得到n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸;
(c)n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸在pd/c催化下,氫氣還原得到烏苯美司。
現有技術中,由於烏苯美司可增強免疫功能,用於抗癌化療、放療的輔助治療,老年性免疫功能缺陷等。可配合化療、放療及聯合應用於白血病、多發性骨髓瘤、骨髓增生異常綜合症及造血幹細胞移植後,以及其它實體瘤患者,因此鑑於其廣泛的應用,對其具體製備工藝的研究顯得非常具有實際意義。
但是,傳統的烏苯美司在合成過程中大多採用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺、三乙胺作為溶劑或者催化劑等,這些試劑本身不環保,後續處理負擔比較大,會產生大量的廢水廢氣,而且三乙胺這種有機鹼容易殘留在產物中,產生有機溶劑殘留的問題。
本發明為了解決上述技術問題,提供了一種烏苯美司的製備方法,該製備方法中,採用無機的弱酸強鹼鹽代替傳統的三乙胺這種有機鹼,無機鹽最好選擇碳酸氫鈉或碳酸氫鉀,更優選擇為碳酸氫鈉,由於溶於水時呈現弱鹼性從而促進反應的順利進行,但是需要注意的是,這裡一定不要選擇鹼性過強的鹽,因為如果鹼性過強,l-亮氨酸苄酯對甲苯磺酸鹽的苄酯會脫落,從而影響到反應的順利進行,因此在進行選擇時要選擇鹼性比較適宜的鹽。
另外,本發明在溶劑選擇上選擇的為乙酸乙酯,改進了傳統需要同時採用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺中一種為反應溶劑、乙酸乙酯為萃取溶劑。避免兩種溶劑同時使用。節約了成本的同時避免了使用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺等所帶來的安全隱患。傳統工藝之所以需要採用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺,是因為四氫呋喃、二氯甲烷、n、n二甲基甲醯胺本身溶解性好,原料(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸,還有hobt(1-羥基苯並三氮唑)能夠發生反應的關鍵在於,其具有良好溶解性的介質中充分分散以促進反應的正常進行,但是本發明利用了dcc催化以先形成活化酯溶液,做成活化酯後採用乙酸乙酯為溶劑,其溶解性已經可以滿足工藝要求,不需要採用四氫呋喃、二氯甲烷、n、n二甲基甲醯胺即保證反應的順利進行,並且通過採用弱酸強鹼無機鹽也一部分解決了溶解性的問題,提高了溶解性,可見本發明採用的弱酸強鹼無機鹽不僅起到了催化作用,也間接起到了作為溶解介質的作用。
本發明烏苯美司的製備工藝的總反應方程式為:
步驟(a)中,優選地,先添加l-亮氨酸苄酯對甲苯磺酸鹽、hobt,乙酸乙酯,並將溫度控制在0-5℃之間,然後添加含有dcc的乙酸乙酯溶液,將溫度升高至15-20℃之間,反應4-5h,一般在後續真正發生反應的時候將溫度升高以保證反應的正常進行,前期溫度在0-5℃之間是為了防止溫度太高副反應的發生。
優選地,含有dcc的乙酸乙酯溶液按照滴加的方式進行,通過逐漸滴加的方式可以保證反應平穩的進行,以控制反應進度,避免劇烈反應。
步驟(b)中,將碳酸氫鈉最好配製成10-20wt%的碳酸氫鈉溶液,因為碳酸氫鈉通過配製成溶液,可以提高反應原料的分散性,提高反應的催化性能。
另外,添加碳酸氫鈉溶液後,溫度一般控制在10-15℃之間,並通過快速攪拌的方式以加快各原料之間的互溶。
優選地,滴加活化酯溶液後,15-20℃之間反應4-5h,得到目的產物,但是還是需要後續分離的步驟以純化目的產物,一般採用tlc來跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm)。
優選地,反應後將產物n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸進行一系列的分離步驟得到純化後的產物,具體步驟最好按照如下操作進行:過濾分離有機相後,洗滌、乾燥以及濃縮操作,乾燥後得到濃縮物,向濃縮物中加入石油醚攪拌2-3h,過濾,乾燥以濃縮,石油醚的添加也是為了將目的產物更好的分散在有機相裡面。
優選地,向濃縮物中加入石油醚攪拌2-3h,過濾後,40-45℃的條件下乾燥,經過乾燥後得到分離純化後的產物,經過測定該步驟的收率可以達到94%以上。
步驟(c)中,溶劑採用的為冰醋酸,反應壓力控制在1.5-2mpa之間,反應溫度控制在20-30℃之間。該步驟通過將n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸催化還原,pd/c、氫氣的條件下脫掉cbz的保護基,得到最終的目的產物烏苯美司,但是此時得到的烏苯美司為粗品,後續通過酸溶鹼沉的方法結晶以獲得成品。因此最好將反應得到的烏苯美司粗品進行過濾、分離以進一步純化。
最後,後續的後處理步驟最好按照如下步驟進行:將烏苯美司粗品在70-80℃、壓力-0.05~-0.1mpa之間進行濃縮後,添加丙酮攪拌後,過濾,添加氨水析晶後,過濾即可。
優選地,添加氨水後,調節溶液的ph值在5-6之間,0-5℃析晶4-5h。
還有優選地,析晶後過濾加入丙酮攪拌2-3h,40-50℃之間乾燥得到烏苯美司成品。
現有技術的一鍋法在合成n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸的過程中使用的四氫呋喃、乙酸乙酯兩種溶劑,本發明的工藝僅使用乙酸乙酯作為溶劑,節約了成本的同時避免了使用四氫呋喃所帶來的安全隱患。還有,一鍋法在合成n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸的過程中使用的是三乙胺為鹼催化劑,本發明採用碳酸氫鈉為鹼催化劑,節約成本的同時,避免三乙胺殘留溶劑對成品質量的影響。另外,一鍋法在合成n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸的過程中需要進行濃縮四氫呋喃,而本發明的工藝反應結束直接萃取處理,更易操作,並不需要對四氫呋喃進行單獨處理,省時省力,也比較環保。最後,一鍋法合成的n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸收率無本發明的工藝高。
與現有技術相比,本發明的有益效果為:
(1)本發明的烏苯美司的製備方法,摒棄了以往採用的有機鹼、四氫呋喃等有機溶劑的添加,有機溶劑僅僅採用乙酸乙酯,節約了成本同時避免了使用四氫呋喃所帶來的安全隱患,採用弱酸強鹼無機鹽作為鹼催化劑,節約成本的同時,避免三乙胺殘留溶劑對成品質量的影響,整個製備方法過程中避免使用有機溶劑,操作過程簡便,容易操作,在提高了烏苯美司產品的同時,收率高;
(2)本發明的利用了dcc催化後先形成了活化酯溶液,做成活化酯後利用乙酸乙酯為溶劑,溶解性已經可以滿足工藝要求,不需要採用四氫呋喃即可滿足溶解性,並且通過採用弱酸強鹼無機鹽也一部分解決了溶解性的問題,提高了溶解性,可見本發明採用的弱酸強鹼無機鹽不僅起到了催化作用,也間接起到了溶解的作用,可見從工藝流程設計上也具有一定的創新性,先形成了活化酯降低了反應體系的溶解性要求。
附圖說明
為了更清楚地說明本發明發明具體實施方式或現有技術中的技術方案,下面將對具體實施方式或現有技術描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖是本發明發明的一些實施方式,對於本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他的附圖。
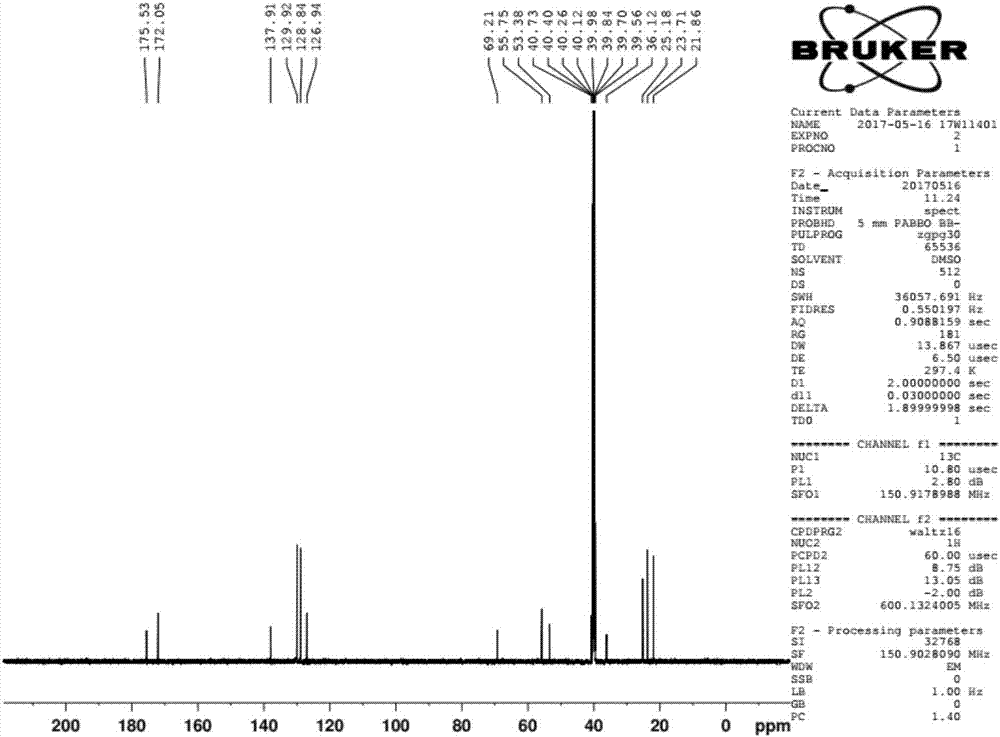
圖1-2為本發明實施例1中的烏苯美司產品的確認圖譜。
具體實施方式
下面將結合實施例對本發明的實施方案進行詳細描述,但是本領域技術人員將會理解,下列實施例僅用於說明本發明,而不應視為限制本發明的範圍。實施例中未註明具體條件者,按照常規條件或製造商建議的條件進行。所用試劑或儀器未註明生產廠商者,均為可以通過市售購買獲得的常規產品。
實施例1
烏苯美司的製備方法如下:
1)將l-亮氨酸苄酯對甲苯磺酸鹽、hobt、10倍(v/m)乙酸乙酯依次加入到反應釜中,投料完成不斷攪拌降溫,緩慢加入dcc的乙酸乙酯溶液,加入過程體系溫度0-5℃之間。投料完成後體系在15-20℃間反應4h,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm),得到l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液;
2)將(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸、10倍(v/m)10%的碳酸氫鈉溶液依次加入到反應釜中,攪拌至完全溶解,降溫至10-15℃,快速攪拌下滴加l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液,滴加完成後在15-20℃間反應4h左右,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm);
3)過濾分液,水相依次用7倍、2倍(v/m)乙酸乙酯萃取,合併乙酸乙酯相,乙酸乙酯相依次用6倍0.5wt%的鹽酸洗滌一次,6倍5wt%的飽和碳酸氫鈉洗滌一次,6倍純化水洗滌一次;乙酸乙酯溶液經無水硫酸鈉乾燥2h,過濾、濃縮至幹,向濃縮物中加入5倍(v/m)石油醚,攪拌2h分散,過濾、40-45℃下乾燥得n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸,收率94-98%;
4)在室溫下將n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸、pd/c(30%)溶解在15倍(v/m)的冰醋酸中,攪拌混合均勻後加入到反應釜中,氮氣氫氣依次置換三次,1.5-2mpa下攪拌反應至不吸氫為至;
5)過濾後的濾液在80℃、-0.1mpa下濃縮至幹,濃縮物中加入10倍(v/m)丙酮,攪拌分散4h,過濾、40-45℃下鼓風乾燥得烏苯美司醋酸鹽;
6)將烏苯美司醋酸鹽溶解在鹽酸溶液中,溶液降溫至0-5℃之間,用15wt%的氨水調節溶液ph值至5-6。0-5℃下析晶5h,過濾,固體用丙酮打漿3h,過濾,40℃下乾燥得到烏苯美司成品,收率為90.5%,具體確認圖譜見附圖1-2。
實施例2
烏苯美司的製備方法如下:
1)將l-亮氨酸苄酯對甲苯磺酸鹽、hobt、10倍(v/m)乙酸乙酯依次加入到反應釜中,投料完成不斷攪拌降溫,緩慢加入dcc的乙酸乙酯溶液,加入過程體系溫度0-5℃之間。投料完成後體系在15-20℃間反應5h,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm),得到l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液;
2)將(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸、10倍(v/m)20%的碳酸氫鈉溶液依次加入到反應釜中,攪拌至完全溶解,降溫至10-15℃,快速攪拌下滴加l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液,滴加完成後在15-20℃間反應5h左右,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm);
3)過濾分液,水相依次用7倍、2倍(v/m)乙酸乙酯萃取,合併乙酸乙酯相,乙酸乙酯相依次用6倍0.5wt%的鹽酸洗滌一次,6倍5wt%的飽和碳酸氫鈉洗滌一次,6倍純化水洗滌一次;乙酸乙酯溶液經無水硫酸鈉乾燥2h,過濾、濃縮至幹,向濃縮物中加入5倍(v/m)石油醚,攪拌3h分散,過濾、40-45℃下乾燥得n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸,收率94-98%;
4)在20-30℃條件下將n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸、pd/c(30%)溶解在15倍(v/m)的冰醋酸中,攪拌混合均勻後加入到反應釜中,氮氣氫氣依次置換三次,1.5-2mpa下攪拌反應至不吸氫為至;
5)過濾後的濾液在70℃、-0.05mpa下濃縮至幹,濃縮物中加入10倍(v/m)丙酮,攪拌分散5h,過濾、40-45℃下鼓風乾燥得烏苯美司醋酸鹽;
6)將烏苯美司醋酸鹽溶解在鹽酸溶液中,溶液降溫至0-5℃之間,用15wt%的氨水調節溶液ph值至5-6。0-5℃下析晶4h,過濾,固體用丙酮打漿3h,過濾,50℃下乾燥得到烏苯美司成品,收率為92.3%。
實施例3
烏苯美司的製備方法如下:
1)將l-亮氨酸苄酯對甲苯磺酸鹽、hobt、10倍(v/m)乙酸乙酯依次加入到反應釜中,投料完成不斷攪拌降溫,緩慢加入dcc的乙酸乙酯溶液,加入過程體系溫度0-5℃之間。投料完成後體系在15-20℃間反應4h,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm),得到l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液;
2)將(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸、10倍(v/m)20%的碳酸氫鈉溶液依次加入到反應釜中,攪拌至完全溶解,降溫至10-15℃,快速攪拌下滴加l-亮氨酸苄酯對甲苯磺酸鹽的活化酯溶液,滴加完成後在15-20℃間反應4h左右,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm);
3)過濾分液,水相依次用7倍、2倍(v/m)乙酸乙酯萃取,合併乙酸乙酯相,乙酸乙酯相依次用6倍0.5wt%的鹽酸洗滌一次,6倍5wt%的飽和碳酸氫鈉洗滌一次,6倍純化水洗滌一次;乙酸乙酯溶液經無水硫酸鈉乾燥2h,過濾、濃縮至幹,向濃縮物中加入5倍(v/m)石油醚,攪拌2h分散,過濾、40-45℃下乾燥得n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸,收率94-98%;
4)在20-30℃條件下將n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸、pd/c(30%)溶解在15倍(v/m)的冰醋酸中,攪拌混合均勻後加入到反應釜中,氮氣氫氣依次置換三次,1.5-2mpa下攪拌反應至不吸氫為至;
5)過濾後的濾液在75℃、-0.085mpa下濃縮至幹,濃縮物中加入10倍(v/m)丙酮,攪拌分散4h,過濾、40-45℃下鼓風乾燥得烏苯美司醋酸鹽;
6)將烏苯美司醋酸鹽溶解在鹽酸溶液中,溶液降溫至0-5℃之間,用20wt%的氨水調節溶液ph值至5-6。0-5℃下析晶5h,過濾,固體用丙酮打漿2h,過濾,45℃下乾燥得到烏苯美司成品,收率為91.4%。
比較例1
將(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁酸、l-亮氨酸苄酯對甲苯磺酸鹽、hobt、四氫呋喃溶依次加入到反應釜中,投料完成體系攪拌下降溫到0℃左右,依次緩慢加入三乙胺和dcc,加入過程體系溫度不超過10℃。投料完成後體系在15℃~20℃間反應,攪拌反應過夜,tlc跟蹤反應終點(乙酸乙酯:石油醚=2:1、紫外254nm)。
過濾,濾液在45℃、-0.085mpa下減壓濃縮至幹,得黃色油狀物濃縮物,加入15倍(v/m)乙酸乙酯溶解,溶液依次用4倍0.5n的鹽酸洗滌一次、4倍0.5n的飽和碳酸氫鈉洗滌一次、4倍純化水洗滌一次,乙酸乙酯溶液經無水硫酸鈉乾燥2小時。
過濾、濃縮至幹,向濃縮物中加入10倍(v/m)石油醚,攪拌2小時分散,過濾、40℃~45℃下乾燥得n-[(2s,3r)-3-苄氧甲醯胺基-2-羥基-4-苯基丁醯]-l-亮氨酸,收率80%-82%。
儘管已用具體實施例來說明和描述了本發明,然而應意識到,在不背離本發明的精神和範圍的情況下可以作出許多其它的更改和修改。因此,這意味著在所附權利要求中包括屬於本發明範圍內的所有這些變化和修改。
