一種氮化鈦的製備方法、氮化鈦及其應用與流程
2023-06-13 20:30:46 4
本發明涉及材料技術領域,特別涉及一種氮化鈦的製備方法、氮化鈦及其應用。
背景技術:
氮元素的化學性質非常穩定,但在一些特殊條件下,它可以與很多元素形成氮化物,在這些氮化物中,過渡金屬氮化物—氮化鈦成為了國內外研究的焦點。
現有技術中製備氮化鈦的合成工藝比較複雜,且製備出的樣品比表面積較小,沒有很好的微納米結構,現有技術中的半導體材料並沒有被很好地拓展成為具有能量儲存和轉換等應用的材料。傳統合成氮化鈦的方法有金屬鈦粉直接氮化法,利用氧化鈦碳熱還原法等,但金屬鈦粉直接氮化法容易在鈦表面形成薄膜阻礙反應的進行,而且工藝比較複雜,成本較大,純度不高,且利用二氧化為鈦原料經過碳熱還原往往需要很高的焙燒溫度增大了製備成本。
技術實現要素:
本發明提供一種氮化鈦的製備方法、氮化鈦及其應用,解決了現有技術中氮化鈦的製備工藝複雜、成本高、純度不高的技術問題,達到了氮化鈦的製備工藝簡單、成本低、純度高的技術效果。
為解決上述技術問題,本發明提供了一種氮化鈦的製備方法,所述製備方法包括:
獲取尿素前驅體;
取CH3CH2OH、TiCl4溶液和所述尿素前驅體,所述尿素前驅體與所述TiCl4的體積比為(3~8):1;
將所述TiCl4溶液緩慢滴加到所述CH3CH2OH中,直至所述CH3CH2OH與所述TiCl4溶液充分混合為黃色透明溶液;
量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置,使所述尿素前驅體與所述TiCl4溶液充分反應,並形成膠狀的混合溶液;
對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫;
停止加熱,並冷卻至室溫,研磨成粉。
優選的,所述CH3CH2OH具體為無水乙醇。
優選的,所述尿素前驅體與所述TiCl4的體積比為3:1。
優選的,所述CH3CH2OH與所述TiCl4溶液的體積比為(4~5):1。
優選的,所述CH3CH2OH與所述TiCl4溶液的體積比為5:1。
優選的,所述對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫,具體為:
在氮氣氣氛下,將膠體狀的混合溶液在高溫管式爐內加熱,使所述膠狀的混合溶液在4小時內加熱至800℃,並保溫3小時。
優選的,所述量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置,所述靜置具體為靜置7~8小時。
基於同樣的發明構思,本申請還提供一種氮化鈦,所述氮化鈦為如權利要求1至5任一所述的製備方法製備的氮化鈦。
基於同樣的發明構思,本申請還提供一種上述的氮化鈦的應用,,所述氮化鈦應用於光電陽極材料。
本申請有益效果如下:
本申請提供一種氮化鈦的製備方法、氮化鈦及其應用,所述氮化鈦為在低溫下製備得到的製備的具有特定形貌結構的具有微納米結構的氮化鈦應用於光電陽極材料,取消了中間存儲過程,相較於傳統陽極材料更加穩定,避免了電池出現過熱和起火的現象。
附圖說明
為了更清楚地說明本發明實施例或現有技術中的技術方案,下面將對實施例描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖僅僅是本發明的一些實施例。
圖1為本申請氮化鈦的製備方法製備得到的氮化鈦的SEM圖;
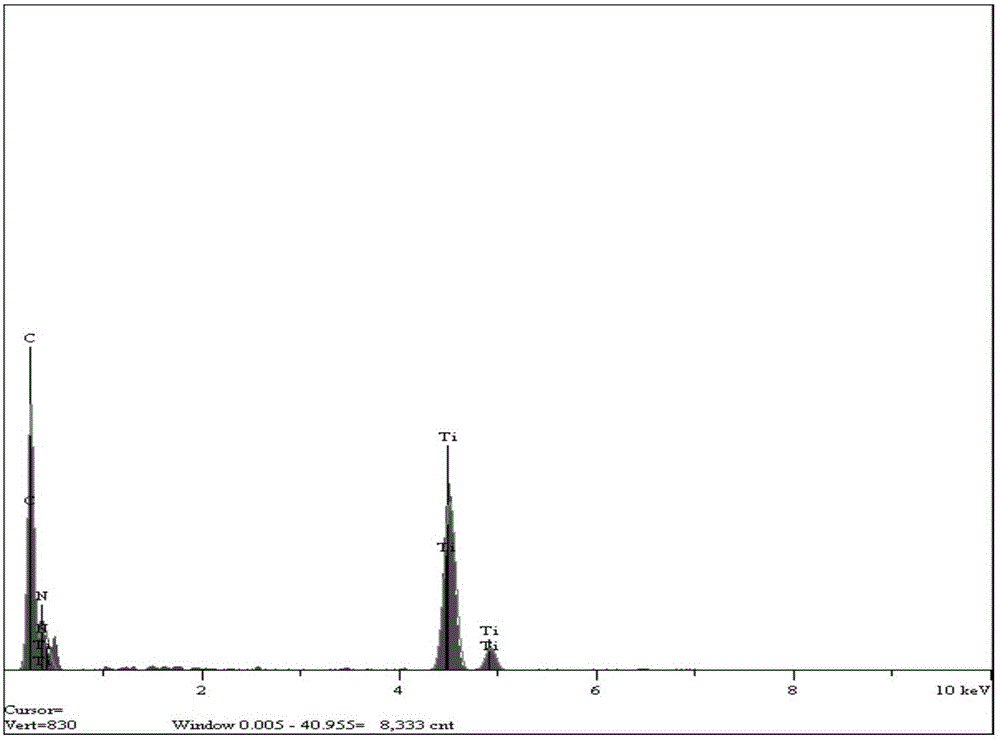
圖2為本申請氮化鈦的製備方法製備得到的氮化鈦的EDS圖;
圖3為本申請氮化鈦的製備方法製備得到的氮化鈦的XRD圖。
具體實施方式
本申請實施例通過提供一種氮化鈦的製備方法、氮化鈦及其應用,解決了現有技術中氮化鈦的製備工藝複雜、成本高、純度不高的技術問題,達到了氮化鈦的製備工藝簡單、成本低、純度高的技術效果。。
本申請實施例中的技術方案為解決上述技術問題,總體思路如下:
實施例一
本申請提供一種氮化鈦的製備方法,所述製備方法包括:
步驟S100,獲取尿素前驅體。
步驟S200,取CH3CH2OH、TiCl4溶液和所述尿素前驅體,所述尿素前驅體與所述TiCl4的體積比為(3~8):1;
具體的,所述CH3CH2OH具體為無水乙醇。所述尿素前驅體與所述TiCl4的體積比為3:1。所述CH3CH2OH與所述TiCl4溶液的體積比為(4~5):1。優選地,所述CH3CH2OH與所述TiCl4溶液的體積比為5:1。
步驟S300,將所述TiCl4溶液緩慢滴加到所述CH3CH2OH中,直至所述CH3CH2OH與所述TiCl4溶液充分混合為黃色透明溶液;
步驟S400,量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置,使所述尿素前驅體與所述TiCl4溶液充分反應,並形成膠狀的混合溶液。
具體的,所述量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置中,靜置7~8小時。
步驟S500,對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫;
具體的,所述對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫,具體為:
在氮氣氣氛下,將膠體狀的混合溶液在高溫管式爐內加熱,使所述膠狀的混合溶液在4小時內加熱至800℃,並保溫3小時。
步驟S600,停止加熱,並冷卻至室溫,研磨成粉。
本申請提供的氮化鈦的製備方法,在低溫下製備、操作簡單得到了微納米級的氮化鈦,且該氮化鈦具備特定形貌,請參見圖1至圖3。本申請提供的氮化鈦的製備方法,解決了現有技術中氮化鈦的製備工藝複雜、成本高、純度不高的技術問題,達到了氮化鈦的製備工藝簡單、成本低、純度高的技術效果。
實施例二
基於同樣的發明構思,本申請還提供一種氮化鈦,所述氮化鈦的製備方法包括:
步驟S100,獲取尿素前驅體。
步驟S200,取CH3CH2OH、TiCl4溶液和所述尿素前驅體,所述尿素前驅體與所述TiCl4的體積比為(3~8):1;
具體的,所述CH3CH2OH具體為無水乙醇。所述尿素前驅體與所述TiCl4的體積比為3:1。所述CH3CH2OH與所述TiCl4溶液的體積比為(4~5):1。優選地,所述CH3CH2OH與所述TiCl4溶液的體積比為5:1。
步驟S300,將所述TiCl4溶液緩慢滴加到所述CH3CH2OH中,直至所述CH3CH2OH與所述TiCl4溶液充分混合為黃色透明溶液;
步驟S400,量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置,使所述尿素前驅體與所述TiCl4溶液充分反應,並形成膠狀的混合溶液。
具體的,所述量取所述尿素前驅體並緩慢加入到所述混合後的所述CH3CH2OH與所述TiCl4溶液中,不斷攪拌,直至所述尿素前驅體完全溶解,靜置中,靜置7~8小時。
步驟S500,對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫;
具體的,所述對所述膠狀的混合溶液進行加熱至750℃~850℃,保溫,具體為:
在氮氣氣氛下,將膠體狀的混合溶液在高溫管式爐內加熱,使所述膠狀的混合溶液在4小時內加熱至800℃,並保溫3小時。
步驟S600,停止加熱,並冷卻至室溫,研磨成粉。
本申請提供的氮化鈦為在低溫下製備、操作簡單得到了微納米級的氮化鈦,且該氮化鈦具備特定形貌,請參見圖1至圖3。本申請提供的氮化鈦的製備方法,解決了現有技術中氮化鈦的製備工藝複雜、成本高、純度不高的技術問題,達到了氮化鈦的製備工藝簡單、成本低、純度高的技術效果。
實施例三
基於同樣的發明構思,本申請還提供一種氮化鈦的應用,所述氮化鈦為上述製備方法製備得到的氮化鈦,所述氮化鈦應用於光電陽極材料。
其中,請參閱圖1至圖3,上述在低溫下製備得到的製備的具有特定形貌結構的具有微納米結構的氮化鈦應用於光電陽極材料,取消了中間存儲過程,相較於傳統陽極材料更加穩定,避免了電池出現過熱和起火的現象。
本申請的有益效果如下:
本申請提供一種氮化鈦的製備方法、氮化鈦及其應用,所述氮化鈦為在低溫下製備得到的製備的具有特定形貌結構的具有微納米結構的氮化鈦應用於光電陽極材料,取消了中間存儲過程,相較於傳統陽極材料更加穩定,避免了電池出現過熱和起火的現象。
最後所應說明的是,以上具體實施方式僅用以說明本發明的技術方案而非限制,儘管參照實例對本發明進行了詳細說明,本領域的普通技術人員應當理解,可以對本發明的技術方案進行修改或者等同替換,而不脫離本發明技術方案的精神和範圍,其均應涵蓋在本發明的權利要求範圍當中。
