細胞調節納米組合物及使用方法與流程
2023-05-26 02:17:42 2
本申請要求2014年2月10日提交的美國臨時申請序號61/938,103的優先權,其全部內容通過引用併入本申請。
發明領域
本發明一般地涉及使用納米組合物來調節細胞行為。
發明背景
現代細胞療法通常涉及在體內或體外調節細胞行為,如刺激細胞增殖、誘導細胞分化和引導細胞遷移。然而,目前調節細胞行為的策略和方法是有限的。納米技術在生物醫學研究中的應用代表了基於納米級水平的修飾來創建有意義的和創新的工具的一個極具吸引力的嶄新方向。因此,需要開發使用納米粒子調節細胞行為的納米技術。
發明簡述
本公開提供了納米組合物以及此類納米組合物的方法或用途。所述納米組合物可以用於調節細胞行為,如細胞增殖、細胞分化、細胞活化和以濃度可控的方式獲得純的細胞群。
本公開的一個方面提供了一種用於細胞富集和調控的納米組合物。所述納米組合物包含納米結構和與所述納米結構可操作地連接的至少一種細胞調節劑。所述細胞調節劑能夠與細胞表面上的分子相互作用。
在一些實施方式中,在所述納米組合物中的納米結構包含磁性材料。在一些實施方式中,所述磁性材料是鐵磁性、亞鐵磁性、順磁性或超順磁性材料。在一些實施方式中,所述磁性材料是超順磁性氧化鐵(SPIO)。
在一些實施方式中,在所述納米組合物中的納米結構在所述納米結構的表面上具有矽烷化塗層。
在一些實施方式中,在所述納米組合物中的納米結構具有1nm至500nm的直徑。
在一些實施方式中,與所述納米結構可操作地連接的所述細胞調節劑包括特異性識別細胞表面上的分子的抗體。在一些實施方式中,所述細胞調節劑選自下組:抗CD3抗體、抗CD28抗體、抗CD81抗體及其任意組合。
在一些實施方式中,所述細胞調節劑是細胞表面上的受體的配體。在一些實施方式中,所述細胞調節劑包括選自由B7-1和B7-2組成的組的CD28天然配體的刺激性形式。
在一些實施方式中,所述細胞調節劑選自下組:CD137抗體、CD137配體蛋白、IL-15蛋白和IL-15受體抗體。
在一些實施方式中,所述細胞調節劑是疫苗。
在某些實施方式中,所述細胞調節劑與細胞相互作用,從而富集所述細胞的群或調節所述細胞的行為。在一些優選的實施方式中,所述細胞的行為是轉化、增殖、重編程、分化或遷移。
在某些實施方式中,可以將所述細胞用於治療。在一些優選的實施方式中,所述細胞能夠產生嵌合的抗原受體。
在一些實施方式中,行為被調節的所述細胞是T細胞。在一些實施方式中,所述細胞是NK細胞。
在一些實施方式中,行為被調節的所述細胞是幹細胞。在一些實施方式中,所述細胞是胚胎幹細胞。
在一些實施方式中,所述細胞的可用性是因為其純度。
在一些實施方式中,所述納米組合物還包含可檢測標記。在一些實施方式中,所述可檢測標記是螢光分子、化學發光分子、生物發光分子、放射性同位素、MRI造影劑、CT造影劑、酶底物標記或著色劑。
在另一個方面,本公開提供了一種通過如下方式調節細胞行為的方法:使所述細胞與可操作地與納米結構連接的至少一種細胞調節劑接觸。所述細胞調節劑與所述細胞表面上的分子接觸,並且所述細胞調節劑與所述分子之間的相互作用調節所述細胞的行為。在一些優選的實施方式中,所述方法還包括富集所述細胞群。
本發明的另一個方面涉及一種在對象中治療疾病的方法。所述方法包括使細胞與可操作地與納米結構連接的至少一種細胞調節劑接觸。所述細胞調節劑與所述細胞表面上的分子相互作用。所述細胞調節劑與所述分子之間的相互作用調節所述細胞的行為。然後將經調節的細胞施用至所述對象。
附圖簡述
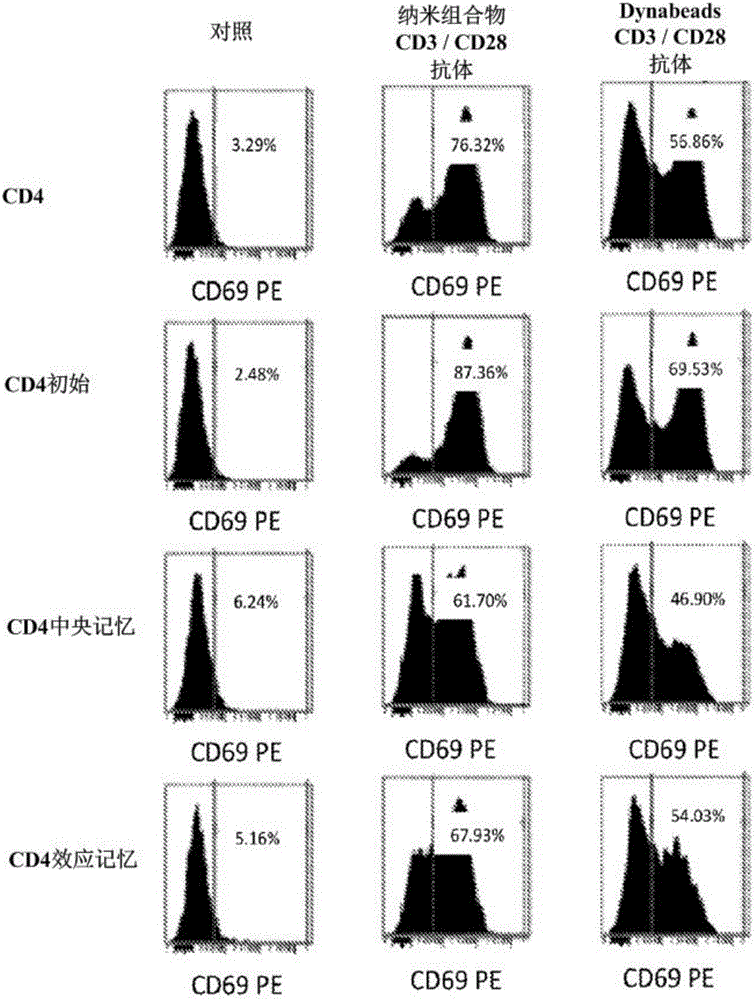
圖1:使用偶聯抗CD3/抗CD28抗體的納米組合物刺激CD4+T細胞。
圖2:使用納米組合物分離和鑑定循環腫瘤細胞。
發明詳述
在對本公開進行更加詳細的描述之前,應理解本公開不限於所描述的特定實施方式,並且因此當然是可以改變的。還應理解本申請所使用的術語僅僅是用於描述特定實施方式的目的,並且並非旨在為限制性的,因為本公開的範圍將僅由所附權利要求限定。當提供值的範圍時,應理解在該範圍上限和下限之間的每個中間值(除非上下文另有明確說明,否則到單位下限的十分之一)以及在該所示範圍中的任意其他所示的值或中間的值均應包括在本公開中。這些較小範圍的上限和下限可以獨立地包括在該較小範圍內,並且也包括在本公開中,同時滿足在所示範圍內的任意特異性排除的限值。當所示的範圍包括一個或全部兩個限值時,排除一個或全部兩個這些所包括的限值的範圍也包括在本公開中。
除非另有定義,本申請中使用的所有技術和科學術語均與本公開所屬領域普通技術人員的通常理解具有相同含義。儘管與本申請所描述的那些相似或等同的任意方法和材料也能夠用於實踐或檢測本公開,但是現對優選的方法和材料進行描述。
在本說明書中引用的所有出版物和專利均通過引用併入本申請,如同每個單獨的出版物或專利被特別地和單獨地指明通過引用併入並且其通過引用併入本申請以公開和描述與所引用的出版物相關的方法和/或材料。任何出版物的引用是為其在申請日之前公開的內容,並且不應被解釋為承認由於此前的公開而導致本公開沒有資格先於此類出版物。而且,所提供的出版日期可能不同於可能需要獨立確證的實際出版日期。
如對於閱讀本公開後的本領域技術人員而言顯而易見,本申請所描述和解釋的每個獨立的實施方式具有分別的組分和特徵,在不脫離本公開範圍和主旨的前提下,所述分別的組分和特徵可以容易地與任意其他若干實施方式的特徵分離或者可以容易地與任意其他若干實施方式的特徵組合。任何所述方法可以以所述事件的順序或以在邏輯上可能的任意其他順序實施。
除非另有說明,本公開的實施方式將使用在本領域範圍內的化學、固態化學、無機化學、有機化學、物理化學、分析化學、材料化學、生物化學、生物學、分子生物學、重組DNA技術、藥理學、成像等技術。在文獻中對這些技術進行了充分的解釋。
在對本公開的實施方式進行詳細描述前,應理解除非另有說明,本公開不限於特定的材料、試劑、反應材料、生產工藝等,因此是可以改變的。還應理解本申請所使用的術語僅用於描述特定實施方式的目的,並且其並非旨在為限制性的。在本公開中也可能的是,在邏輯上可行的情況下可以以不同順序執行步驟。
必須指出的是,如在本說明書和所附權利要求中所使用的,除非上下文另有明示,單數形式的「一個」、「一種」和「該」包括複數指示對象。因此,例如,提及「一種化合物」包括多種化合物。在本說明書和在隨後的權利要求中,將提及若干術語,除非相反的指示是明顯的,所述術語應該被定義為具有下述含義。
納米組合物
本公開的一個方面提供了一種用於細胞富集和調節的納米組合物,所述納米組合物包含納米結構和與所述納米結構可操作地連接的至少一種細胞調節劑,其中所述細胞調節劑能夠與細胞表面上的分子相互作用。
納米結構
如在本申請中所使用的,術語「納米結構」指具有範圍從約1nm至約1500nm(例如從1nm至1200nm、從1nm至1000nm、從1nm至800nm、從1nm至500nm、從1nm至400nm等)的直徑的粒子。在某些實施方式中,所述納米結構包含單一粒子或一簇粒子。在某些實施方式中,所述納米結構包含核納米粒子和塗層。所述核納米粒子可以是單一粒子或一簇粒子。所述塗層可以是本領域公知的任意塗層,例如聚合物塗層,如聚乙二醇、矽烷和多糖(例如葡聚糖及其衍生物)。
在一些實施方式中,本申請提供的納米結構含有磁性材料。適宜的磁性材料包括例如亞鐵磁性或鐵磁性材料(例如鐵、鎳、鈷、稀土金屬的一些合金以及一些天然存在的礦物(如磁石))、順磁性材料(如鉑、鋁)和超順磁性材料(例如超順磁性氧化鐵或SPIO)。
磁性材料具有磁性,所述磁性使得所述納米結構被磁體或在磁場中被拉引或吸引。磁性能夠便於使用磁性相互作用對納米結構進行操縱(例如分離、純化或富集)。當受到所施加的磁場(例如來自高場和/或高梯度磁體的磁場)時,所述磁性納米結構可被吸引至指定位點或被磁性引導至指定位點。例如,可以將磁體(例如磁柵)置於所述納米結構附近,以便吸引所述磁性納米結構。
可以使用本領域公知的具有磁性的任意納米結構。在某些實施方式中,本申請所提供的納米結構包含磁性納米粒子,所述磁性納米粒子含有磁性材料。例如,所述納米結構的磁性納米粒子是超順磁性氧化鐵(SPIO)納米粒子。所述SPIO納米粒子是氧化鐵納米粒子(磁赤鐵礦(γ-Fe2O3)或磁鐵礦(Fe3O4)),或者由這兩相組成的納米粒子。SPIO可以使用適宜的方法合成,並且作為膠體溶液分散在有機溶劑或水中。合成SPIO納米粒子的方法是本領域公知的(參見例如Morteza Mahmoudi等,Superparamagnetic Iron Oxide Nanoparticles:Synthesis,Surface Engineering,Cytotoxicity and Biomedical Applications,Nova Science Pub Inc出版,2011)。在一個實施方式中,可以通過溼化學合成方法製備SPIO納米粒子,所述方法涉及在存在鹼性介質的條件下將Fe和Fe鹽共沉澱。在合成過程中,可以引入氮氣以控制氧化,可以加入表面活性劑和適宜的聚合物以抑制附聚或控制粒徑,和/或可以使用乳液(如油包水微乳)來調節SPIO納米粒子的物理性質(參見例如Jonathan W.Gunn,The preparation and characterization of superparamagnetic nanoparticles for biomedical imaging and therapeutic application,ProQuest出版,2008)。在另一個實施方式中,可以任選地在存在一種或多種表面活性劑(例如月桂酸和油酸)和/或氧化劑(例如三甲基胺-N-氧化物)的條件下,在適宜溶劑(例如二辛基醚或十六烷)中通過單獨的五羰基鐵的熱分解或通過與過渡金屬羰基化合物的組合的五羰基鐵的熱分解而產生SPIO納米粒子(參見例如美國專利申請PG Pub 20060093555)。在另一個實施方式中,還可以通過氣相沉積法製備SPIO納米粒子,所述氣相沉積法涉及在含有不同濃度氧氣的氦氣氛中鐵的雷射汽化(參見Miller J.S.等,Magnetism:Nanosized magnetic materials,Wiley-VCH出版,2002)。在某些實施方式中,所述SPIO納米粒子是在美國專利申請PG Pub 20100008862中公開的那些。
在某些實施方式中,所述納米結構還可以包含非SPIO納米粒子。所述非SPIO納米粒子包括例如金屬納米粒子(例如金或銀納米粒子(參見例如Hiroki Hiramatsu,F.E.O.,Chemistry of Materials 16,2509-2511(2004)))、半導體納米粒子(例如具有單一或多個組分的量子點,如CdSe/ZnS(參見例如M.Bruchez等,Science 281,2013-2016(1998)))、摻雜的不含重金屬的量子點(參見例如Narayan Pradhan等,J.Am.Chem.Soc.129,3339-3347(2007))或其他半導體量子點);聚合物納米粒子(例如由PLGA(聚(乳酸-共-乙醇酸)(參見例如Minsoung Rhee等,Adv.Mater.23,H79-H83(2011))、PCL(聚己內酯)(參見例如Marianne Labet等,Chem.Soc.Rev.38,3484-3504(2009))、PEG(聚乙二醇)或其他聚合物中的一種或組合製備的粒子);含矽的納米粒子;和非SPIO磁性納米粒子(例如MnFe204(參見例如Jae-Hyun Lee等,Nature Medicine 13,95-99(2006))、合成的反鐵磁性納米粒子(SAF)(參見例如A.Fu等,Angew.Chem.Int.Ed.48,1620-1624(2009))和其他類型的磁性納米粒子)。在某些實施方式中,所述非SPIO納米粒子是有色納米粒子,例如半導體納米粒子,如量子點。
可以使用本領域公知的適宜方法製備或合成所述非SPIO納米粒子,例如溶膠-凝膠合成法、油包水微乳法、氣相沉積法等。例如,可以通過利用還原劑(如檸檬酸鹽或丙酮二羧酸酯)還原氯金酸鹽溶液(例如HAuCl4),從而製備金納米粒子。舉另一個例子,可以在二氧化矽粒子表面上由Cd(ClO4)2和Na2S製備CdS半導體納米粒子。舉另一個例子,可以基於在注射至熱配位溶劑中之後有機金屬試劑(如二甲基鎘和三辛基硒)的熱解來合成II-VI半導體納米粒子(參見例如Gunter Schmid,Nanoparticles:From Theory to Application,John Wiley&Sons出版,2011)。可以採用成核摻雜策略製備摻雜的無重金屬的量子點,例如摻雜Mn的ZnSe量子點,其中在高溫下形成小尺寸的MnSe納米簇作為核,並且ZnSe層包覆在核上。舉另一個例子,可以通過如下方式製備聚合物納米粒子:在兩相溶劑系統中乳化聚合物,通過超聲或均化誘導納米尺寸的聚合物液滴,並蒸發有機溶劑以獲得納米粒子。舉另一個例子,可以通過溶膠-凝膠合成來製備含矽納米粒子,其中在存在酸或鹼催化劑的條件下在水和乙醇的混合物中水解烷氧基矽前體(例如TMOS或TEOS),在劇烈攪拌下縮合經水解的單體,並且可以收集所得二氧化矽納米粒子。舉另一個例子,可以通過在高真空下使用離子束沉積,在非磁性間隔層(例如釕金屬)兩側的每一側上沉積鐵磁性層以及可化學蝕刻的銅剝離層和保護性鉭表面層,從而製備SAF(一種非SPIO磁性納米粒子),並且在除去保護層和進行選擇性銅蝕刻後釋放所述SAF納米粒子。
納米粒子的尺寸為1nm至100nm(優選尺寸為1-50nm、2-40nm、5-20nm、1nm、2nm、3nm、4nm、5nm、6nm、7nm、8nm、9nm、10nm、11nm、12nm、13nm、14nm、15nm、16nm、17nm、18nm、19nm、20nm)。可以通過選擇適宜的合成方法和/或系統來控制納米粒子的尺寸。例如,為控制納米粒子的尺寸,可以在極性溶劑中進行納米粒子的合成,所述極性溶劑提供了能夠吸附在納米粒子表面上的離子種類,從而提供了靜電作用和粒子-粒子斥力以幫助穩定納米粒子並抑制納米粒子的生長。舉另一個例子,可以在微量非均質系統中合成納米粒子,所述微量非均質系統能夠將納米粒子劃入受限的空腔或域中。此類微量非均質系統可以包括液晶、單層和多層、直接膠束、反膠束、微乳和囊泡。為獲得所需尺寸範圍內的納米粒子,可以適當控制或改變合成條件以提供例如所需的溶液濃度或所需的空腔範圍(詳細的綜述可以參見例如Vincenzo Liveri,Controlled synthesis of nanoparticles in microheterogeneous systems,Springer出版,2006)。
納米粒子的形狀可以是球形、立方體、棒狀(參見例如A.Fu等,Nano Letters,7,179-182(2007))、四角椎體形狀(參見例如Manna等,Nature Materials,2,382-385(2003))、椎體、多臂、納米管、納米線、納米纖維、納米板或任意其他適宜的形狀。在製備過程中控制納米粒子形狀的方法是本領域公知的(參見例如Waseda Y.等,Morphology control of materials and nanoparticles:advanced materials processing and characterization,Springer出版,2004)。例如,當採用自下而上的過程(即從分子至納米粒子)製備納米粒子時,可以加入強烈吸附於特定晶面上的形狀控制劑以控制粒子的生長速率。
單個納米結構可以包含單個納米粒子或者多個微型納米粒子或一簇微型納米粒子(A.Fu等,J.Am.chem.Soc.126,10832-10833(2004),J.Ge等,Angew.Chem.Int.Ed.46,4342-4345(2007),Zhenda Lu等,Nano Letters 11,3404-3412(2011))。所述微型納米粒子可以是均質的(例如由相同組合物/材料製得或具有相同尺寸)或者異質的(由不同組合物/材料製得或具有不同尺寸)。一簇均質微型納米粒子指具有基本上相同的特徵或特性或者由基本上相同的材料組成的一系列粒子。一簇異質微型納米粒子指具有不同特徵或特性或者由基本上不同的材料組成的一系列粒子。例如,異質微型納米粒子可以包含在中心的量子點和與所述量子點連接的若干離散的金(Au)納米晶。當納米粒子與塗層(如下文所述)締合時,在一系列異質納米粒子中不同的納米粒子不需要首先彼此之間締合,而是能夠單獨和分別地與塗層締合。
在某些實施方式中,所公開的納米結構包含多個納米粒子。例如,納米結構含有2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、50、60、70、80、90、100、100s或1000s個納米粒子。
在某些實施方式中,本申請所提供的納米結構還包含塗層。至少一個核納米粒子能夠嵌入塗層或使用塗層塗覆。可以使用本領域公知的任意適宜塗層,例如聚合物塗層和非聚合物塗層。塗層通過如下與核納米粒子相互作用1)分子內相互作用,如共價鍵(例如σ鍵、π鍵、δ鍵、雙鍵、三鍵、四重鍵、五重鍵、六重鍵、3c-2e、3c-4e、4c-2e、抓氫鍵、彎曲鍵、偶極鍵、π反向鍵、共軛、超共軛、芳香性、哈普託數和反鍵)、金屬鍵(例如與在核納米粒子中的金屬原子的螯合相互作用),或離子鍵(陽離子π鍵和鹽鍵),和2)分子間相互作用,如氫鍵(例如雙氫鍵、雙氫配合物、低壘氫鍵、對稱氫鍵)和非共價鍵(例如疏水性、親水性、電荷-電荷或π-堆疊相互作用、範德華力、倫敦色散力、機械鍵、滷素鍵、親金作用、嵌入、堆疊、熵力和化學極性)。
在某些實施方式中,塗層包含如美國臨時申請61/589,777和美國專利申請12/460,007(本公開中引用的所有參考文獻整體併入本申請)所公開的的低密度多孔性3D結構。
所述低密度多孔性3D結構指與現有介孔納米粒子(例如孔尺寸為2nm至50nm的介孔納米粒子)相比密度低得多(例如十幾倍、二十幾倍、三十幾倍、五十幾倍、七十幾倍、100s倍)的結構。(A.Vincent等,J.Phys.Chem.C,2007,111,8291-8298;J.E.Lee等,J.Am.Chem.Soc,2010,132,552-557;Y.-S.Lin等,J.Am.Chem.Soc,2011,133,20444-20457;Z.Lu,Angew.Chem.Int.Ed.,2010,49,1862-1866.)。
在某些實施方式中,所述低密度多孔性3D結構指密度<1.0g/cc(例如<100mg/cc、<10mg/cc、<5mg/cc、<1mg/cc、<0.5mg/cc、<0.4mg/cc、<0.3mg/cc、<0.2mg/cc或90%)。螢光顏色標識細胞類型,並表示細胞表面分子位置和功能。使用具有多功能螢光和磁性性質的納米組合物與兩種不同類型循環腫瘤細胞的相互作用並將其從全血樣品中分離。特異性相互作用來自於納米結構表面偶聯的抗體和細胞表面分子。紅色螢光納米結構(615nm發射)在表面上具有抗EpCAM抗體,其與H1650細胞(CFSE染色為綠色)相互作用。綠色螢光納米結構(535nm發射)在表面上具有抗CD19抗體,其與Oc1-Ly8(CMTMR染色為櫻紅色)相互作用。這些多功能納米組合物不僅與細胞相互作用,還通過螢光信號鑑定細胞類型或細胞表面標記物。
儘管本發明參照特定的實施方式(其中一些是優選的實施方式)進行了特別的顯示和描述,本領域技術人員應理解在不脫離如本申請所述的本發明的主旨和範圍的前提下可以對其形式和細節做出多種改變。
