胺基酸修飾的金屬富勒烯水溶性納米顆粒在製備腫瘤血管阻斷劑中的應用的製作方法
2023-06-16 23:55:14 3
本發明涉及胺基酸修飾的金屬富勒烯水溶性納米顆粒在製備腫瘤血管阻斷劑中的應用,屬於納米生物醫藥領域。
背景技術:
目前癌症已經成為繼心血管疾病之後,威脅人類生存健康的第二大殺手。腫瘤的生長和轉移都依賴血管網的存在,腫瘤血管是癌細胞的營養通道和轉移途徑。通過選擇性破壞已形成的腫瘤血管網快速切斷腫瘤血供,誘發腫瘤細胞發生缺血壞死,是一種切實有效的抑制腫瘤生長,阻止轉移的方法,這個概念由Juliana Denekamp於1982年提出,相應的藥物稱為血管阻斷劑(Vascular disrupting agents,VDAs)。其它任何直接攻擊腫瘤細胞的方法,在很大程度上只能暫時緩解病情,復發很難避免,這也是目前手術、放化療的局限所在。
現代醫學證明,正常血管需要一年時間才能夠長成,是由內膜、中膜和外膜構成的三層密實結構,而腫瘤血管只用4天即可形成,結構上為由內皮細胞構成的單層薄膜。而由於構成腫瘤血管的內皮細胞間隙較大、結構不完整,導致腫瘤血管通常包含有大量納米尺度的小孔,使小分子和一些納米顆粒能夠透孔而出。腫瘤血管阻斷劑正是利用了腫瘤血管和正常血管的差異,目前有抗體和小分子兩類。例如,3G4抗體Tarvacin通過結合腫瘤血管內皮細胞的磷脂醯絲氨酸殺傷胰腺癌細胞。小分子血管阻斷劑又分為微管解聚物和黃酮兩類藥物,微管解聚物通過結合血管內皮細胞微管蛋白β亞基的秋水仙鹼結合位點,導致微管解聚、肌動蛋白和微管蛋白分離,進而破壞血管內皮細胞骨架。秋水仙鹼和鬼臼毒素就是經典的微管解聚藥物。
由於腫瘤血管較正常組織血管有很大不同,腫瘤血管的內皮細胞間隙較大、結構不完整,導致腫瘤血管通常包含有大量納米尺度的小孔,由於腫瘤的高通透性和滯留效應(EPR效應),納米顆粒能嵌入這些小孔破壞腫瘤血管,從而導入腫瘤內部大量出血,切斷了腫瘤組織的營養供應,進而抑制了腫瘤的生長。血管阻斷劑已經成為目前腫瘤血管靶向治療領域的研究熱點之一,隨著科學研究的不斷發展,其必將進入臨床應用,成為腫瘤治療的突破性技術。
技術實現要素:
本發明的目的是提供胺基酸修飾的金屬富勒烯水溶性納米顆粒在製備腫瘤血管阻斷劑中的應用,本發明胺基酸修飾的金屬富勒烯水溶性納米顆粒應用於製備腫瘤血管阻斷劑中,其製備的腫瘤血管阻斷劑生物安全性更高,對正常生物組織無毒副作用,用於治療的效果好。
本發明提供的胺基酸修飾的金屬富勒烯水溶性納米顆粒在製備腫瘤血管阻斷劑中的應用;
所述胺基酸修飾的金屬富勒烯水溶性納米顆粒的結構通式為metallofullerene-(OH)x(Amino Acid)y;
其中,metallofullerene為金屬富勒烯;
0≤x<50;0≤y<20;
Amino Acid為水溶性胺基酸。
上述的應用中,所述金屬富勒烯包括;M@C2n、M2@C2n、MA@C2n、M3N@C2n、M2C2@C2n、M2S@C2n、M2O@C2n和MmA3-mN@C2n中的至少一種;其中,M、A均為金屬元素,所述M、A均選自Sc、Y和鑭系金屬元素中的至少一種,30≤n≤60,0≤m≤3,且n、m均為整數;
所述水溶性胺基酸為丙氨酸、甘氨酸、絲氨酸、精氨酸、賴氨酸和天門氨酸中的至少一種。
本發明中,鑭系金屬元素為鑭(La)、鈰(Ce)、鐠(Pr)、釹(Nd)、鉕(Pm)、釤(Sm)、銪(Eu)、釓(Gd)、鋱(Tb)、鏑(Dy)、鈥(Ho)、鉺(Er)、銩(Tm)、鐿(Yb)、鑥(Lu);
所述稀土金屬具體可為Gd,所述金屬富勒烯具體可為Gd@C82、Gd3N@C80。
上述的應用中,所述納米顆粒的水合直徑可為1~1000nm,具體可為100-150nm。
上述的應用中,製備所述胺基酸修飾的金屬富勒烯水溶性納米顆粒包括如下步驟:將所述水溶性胺基酸的鹼溶液與金屬富勒烯混合,進行親核加成反應,即得到所述胺基酸修飾的金屬富勒烯水溶性納米顆粒;
所述水溶性胺基酸的鹼溶液中鹼的質量分數可為10~50%,具體可為14%、10~14%、14~50%或11~25%;所述鹼具體可為氫氧化鈉;
所述水溶性胺基酸與所述金屬富勒烯的摩爾比可為1~100:1。
上述的應用中,所述親核加成反應的溫度可為50~100℃,具體可為50℃;所述親核加成反應的時間可為1~30h,具體可為1.5h、1~1.5h、1.5~7h或1~5h;
所述製備方法中,在所述親核加成反應之後還包括過濾除去雜質的步驟。
本發明還提供了一種腫瘤血管阻斷劑,該腫瘤血管阻斷劑的活性成分為所述胺基酸修飾的金屬富勒烯水溶性納米顆粒。
上述的腫瘤血管阻斷劑中,所述腫瘤血管阻斷劑的劑型為藥學可接受的劑型。
上述的腫瘤血管阻斷劑中,當所述腫瘤血管阻斷劑的劑型為注射劑時,其溶劑為水、生理鹽水、PBS緩衝液和Tris-HCl溶液中的至少一種;所述生理鹽水的濃度具體可為0.85~0.90%;PBS緩衝液的濃度具體可為0.01~0.1mol/L,PBS緩衝液組成的組分具體可為Na2HPO4、KH2PO4、NaCl和KCl;Tris-HCl溶液的濃度具體可為0.05mol/L;
所述水溶性胺基酸修飾的金屬富勒烯納米材料的濃度可為0.5~10mmol/L,具體可為1mmol/L、0.5~1mmol/L、1~10mmol/L或0.5~5mmol/L。
本發明進一步提供了一種高效阻斷腫瘤血管的腫瘤治療方法,包括如下步驟:1)向患腫瘤生物體給予有效劑量的所述腫瘤血管阻斷劑;
2)用與所述水溶性胺基酸富勒烯納米材料相匹配的輻射能量源對所述患腫瘤生物體的腫瘤部位進行射頻輻照。
上述的腫瘤治療方法中,所述腫瘤為肝癌、肺癌、結腸直腸癌、腎癌、胰腺癌、骨癌、乳腺癌、卵巢癌、前列腺癌、食管癌、胃癌、口腔癌、鼻癌、喉癌、膽管癌、宮頸癌、子宮癌、睪丸癌、腦膜瘤、皮膚癌、黑色素瘤和肉瘤中的至少一種;
所述腫瘤血管阻斷劑的給藥量可為1mg/kg~100mg/kg,具體可為2mg/kg;具體的所述患腫瘤生物體總給藥量按照所述荷瘤生物體的體重進行換算;
所述藥物的給藥方式採用靜脈注射、腹腔注射、口服和局部給藥中的至少一種;
所述射頻輻照的頻率可為1~1000MHz,具體可為200MHz、1~200MHz、200~1000MHz或50~500MHz,發射功率為1mW~10kW,具體可為5mW、1mW~5mW、5mW~10kW或1mW~100mW,所述輻照的時間可為10min~2h,具體可為30min、10min~30min、30min~2h或20min~1h;
所述患腫瘤生物體為哺乳動物;具體可為人、鼠、兔、豬、猴和狗中的至少一種。
本發明中,所述有效劑量是指當通過本發明的方法給予所述藥物時,足以有效傳遞用於治療腫瘤的活性成分的量。
本發明中,注射所述藥物在0~1h後進行所述輻照;具體可為10min~2h。
本發明在抗腫瘤治療中,通過將藥物注射入生物體後,通過血液循環到達腫瘤部位,隨後施加射頻輻照,使腫瘤部位的納米顆粒在血管中發揮作用,達到快速治療腫瘤的目的;由於腫瘤血管較正常組織血管有很大不同,腫瘤血管的內皮細胞間隙較大、結構不完整,導致腫瘤血管通常包含有大量納米尺度的小孔,由於腫瘤的高通透性和滯留效應(EPR效應),金屬富勒烯納米顆粒能嵌入這些小孔破壞腫瘤血管,阻斷血流,切斷了腫瘤組織的營養供應,進而抑制了腫瘤的生長。
本發明還提供了一種高效阻斷腫瘤血管的腫瘤的套裝,該套裝包括所述腫瘤血管阻斷劑和產生輻射能量源的設備。
上述的套裝中,所述產生輻射能量源的設備發射的頻率為所使用的射頻源輻照的頻率可為1~1000MHz,發射功率可為1mW-10kW,生物體吸收的輻照的功率可為1~1000mW,射頻輻照源可為脈衝模式。
本發明具有以下優點:
1、本發明藉助穿透性很強的射頻作用,不受腫瘤在生物體分布的限制,即可治療生物體表附近的腫瘤,也可治療生物體深部器官或組織的腫瘤。
2、本發明針對腫瘤血管和正常血管的差異,特異性阻斷腫瘤血管治療腫瘤,從而具有廣譜性。
3、本發明中胺基酸修飾的金屬富勒烯碳籠完整性更強,生物安全性更高,對正常生物組織無毒副作用。
4、與目前臨床普遍使用的環磷醯胺、紫杉醇等比較,本發明腫瘤血管阻斷劑給藥劑量小,毒性低,單次治療就能達到高抑瘤率;相比於同類金屬富勒醇藥物,本發明腫瘤血管阻斷劑在其基礎上更加降低了給藥劑量,以及給藥後射頻照射時間更短,治療速度更快,療效高。
附圖說明
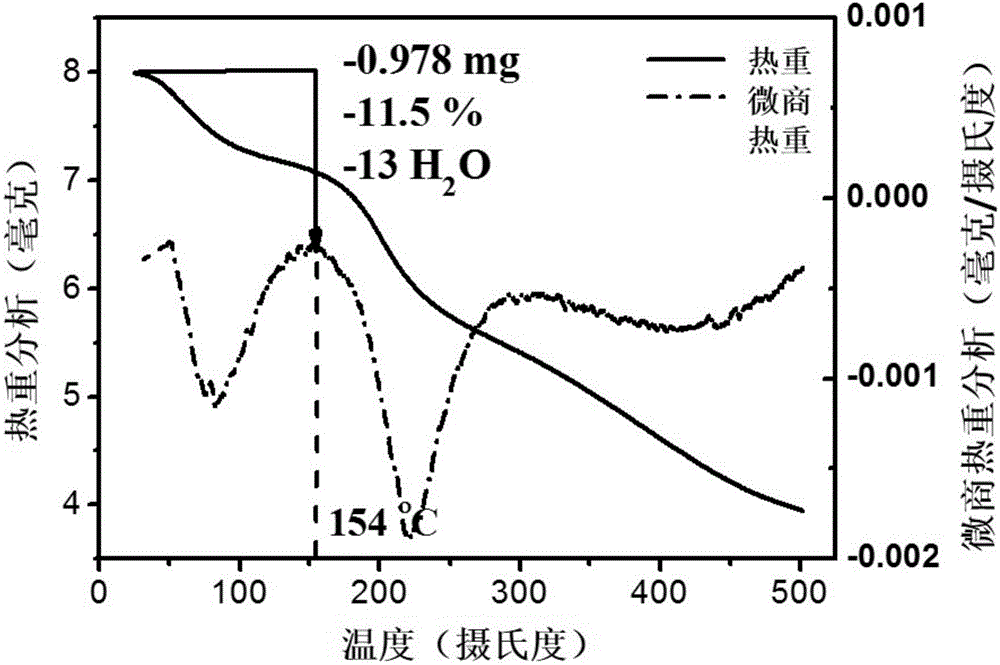
圖1、本發明實施例1中製備得到的Gd@C82(OH)13(NHCH2CH2COOH)6(簡寫為GF-Ala)熱重分析及微商熱重分析曲線。
圖2、本發明實施例2水溶性羥基修飾的Gd@C82納米顆粒(簡寫為GF-OH)的熱重分析及微商熱重分析曲線。
圖3、GF-Ala及GF-OH兩種藥物的磁化曲線及磁化強度-溫度曲線。
圖4、GF-Ala及GF-OH兩種藥物的高分辨原子力顯微鏡圖片。
圖5、GF-Ala及GF-OH兩種藥物的螢光猝滅擬合曲線,由此計算可得兩種藥物的蛋白結合率,其中F0是不加富勒烯時蛋白的螢光,F是加富勒烯後蛋白的螢光,Q是富勒烯濃度。
圖6、GF-Ala及GF-OH兩種藥物在pH=7時的平均水合半徑和Zeta電勢比較。
圖7、本發明實施例2中GF-Ala藥物在治療前、治療後及治療後24h的磁共振成像圖片。
圖8、本發明實施例2中兩種藥物的抑瘤率比較,在長期觀察12天期間,小鼠腫瘤在不同時間點的腫瘤狀態變化,以及12天後小鼠的腫瘤體積和重量對比。
圖9、本發明實施例2中兩種藥物在治療後24h後腫瘤血管的環境掃描照片(其中a為GF-Ala加射頻,b為a的局部放大圖,c為GF-OH加射頻,d為GF-Ala不加射頻,e為生理鹽水加射頻,f為只注射生理鹽水)。
具體實施方式
下述實施例中所使用的實驗方法如無特殊說明,均為常規方法。
下述實施例中所用的材料、試劑等,如無特殊說明,均可從商業途徑得到。
下述實施例中,水溶性羥基修飾的Gd@C82納米顆粒,結構簡式為Gd@C82(OH)26(簡寫為GF-OH),其製備方法參照文獻Carbon,2013,65,175。
實施例1、金屬富勒烯丙氨酸納米顆粒Gd@C82(OH)13(NHCH2CH2COOH)6的製備
把約10mg Gd@C82固體加入10ml單口瓶中,加入6ml NaOH質量分數為14%的β-丙氨酸鹼溶液(β-丙氨酸與NaOH的摩爾比為1:2),50℃下劇烈攪拌1.5h,黑色固體逐漸溶解生成棕黑色溶液。過濾除去未反應的少量固體粉末,濾液使用Mw=3500透析袋透析除去小分子雜質,使用220nm微孔濾膜過濾後得到的棕黑色溶液即為本發明的胺基酸修飾的金屬富勒烯水溶性納米顆粒Gd@C82(OH)13(NHCH2CH2COOH)6(又稱為β-丙氨酸修飾的金屬富勒烯納米顆粒,結構簡式為Gd@C82(OH)13(NHCH2CH2COOH)6,簡寫為GF-Ala)。
表1β-丙氨酸修飾的金屬富勒烯水溶性納米顆粒元素分析結果
對本發明β-丙氨酸修飾的金屬富勒烯水溶性納米顆粒進行元素分析所得碳、氮、氫元素比,如表1所示。由表1可知,根據熱重曲線分析可以得出原固體粉末中含11.5%的水,經過計算約為13個H2O分子,再結合元素分析,進一步推測得到該物質的平均分子式為Gd@C82(OH)13(NHCH2CH2COOH)6。
如圖1所示為Gd@C82(OH)13(NHCH2CH2COOH)6(簡寫為GF-Ala)熱重分析及微商熱重分析曲線,經計算固體中含11.5%的水份,結合元素分析中C、H、N含量可推測平均分子式為Gd@C82(OH)13(NHCH2CH2COOH)6。
由圖6和表2可知,本發明Gd@C82(OH)13(NHCH2CH2COOH)6在pH=7的水中平均粒徑為127.7nm,Zeta電勢為-44.7mV。
表2納米顆粒在pH=7的水中的平均粒徑及Z電勢
實施例2、β-丙氨酸修飾的金屬富勒烯納米顆粒在射頻作用下腫瘤治療及效果對比
1、建立荷瘤鼠動物模型:
選取5周周齡體重在16.0~20.0g的雌性BALB/c小鼠,皮下接種100μL濃度為5×107/ml的H22肝癌細胞。生長約5-7天後,腫瘤尺寸達到50-100mm3進行實驗。
2、腫瘤治療及不同藥物效果對比實驗
對比藥物:水溶性羥基修飾的Gd@C82納米顆粒,其表面修飾了大量的羥基基團,如圖2所示為其熱重分析TGA及DTG曲線,結合元素分析C、H、N含量(C 36.95%,H 2.36%,N<0.3%)推測其平均分子式為Gd@C82(OH)26。
通過尾靜脈注射β-丙氨酸衍生化GF-Ala和羥基化GF-OH這兩種藥物(濃度為1mmol/L,2mg/kg)於荷瘤鼠體內,隨後施加射頻(200MHz,5mW)治療30min。分別採集治療前、治療後和治療後24h的T2磁共振成像,並長期觀察兩種藥物的抑瘤效果。設置三個對照組,分別為只注射生理鹽水(Saline)、注射生理鹽水和施加射頻(Saline+RF),只注射β-丙氨酸修飾的金屬富勒烯藥物(GF-Ala)。
由圖3可知,經測試計算本發明金屬富勒烯胺基酸納米顆粒的有效磁矩為8.9μ,高於同類金屬富勒醇8.5μ;由圖4可知,同時改變碳籠表面修飾的官能團或分子,改善了納米顆粒的分散性和均一性,有利於藥物的穩定性;其次其與體內蛋白等的親和性也因表面修飾的不同而發生了變化,根據螢光猝滅機理,按照F0/(F0-F)=1/faKa[Q]+1/fa計算藥物與蛋白的結合常數,如圖5所示,得到本發明金屬富勒烯胺基酸納米顆粒與蛋白的結合常數為0.98×105L·mol-1,同類金屬富勒醇僅為0.13×105L·mol-1。由上述實驗證明,使用本發明所的胺基酸修飾的金屬富勒烯納米顆粒GF-Ala相比於同類金屬富勒醇GF-OH在腫瘤治療中的效果更為優異。具體表現為丙胺基酸修飾的金屬富勒烯納米顆粒GF-(Ala)是羥基修飾的金屬富勒烯納米顆粒GF-(OH)的使用劑量的1/5~1/10,可能的原因是改變了金屬富勒烯水溶化製備方法,反應條件更為溫和,碳籠表面修飾的官能團或小分子更少,碳籠的完整性更強,使得金屬富勒烯納米顆粒的磁性更強。
圖7所示為本發明GF-Ala藥物在治療前、治療後及治療後24h時腫瘤部位的T2磁共振成像狀況。從圖7中可以看出,治療後腫瘤中心區域出現大面積壞死情況,在成像上表現為變黑,治療後24h壞死比例大幅度提高。
圖8為本發明GF-Ala藥物與GF-OH藥物在同等劑量下長期抑瘤率的比較。本發明GF-Ala藥物治療後腫瘤組織呈現明顯的壞死變黑現象,經過12天的連續觀察,腫瘤部位幾乎結痂脫落;而GF-OH藥物相比於對照組表現出一定的治療效果,其治療後12天時腫瘤體積和重量約為本發明GF-Ala藥物的兩倍。
圖9為本發明GF-Ala藥物、GF-OH藥物及對照組在治療後24h時腫瘤血管的環境掃描照片。從圖中可以觀察到本發明GF-Ala藥物在射頻輔助治療後腫瘤血管內皮細胞出現大範圍的脫落,露出血管基膜,說明本發明GF-Ala藥物可以快速靶向摧毀腫瘤血管,切斷腫瘤部位的營養供應。而GF-OH藥物內皮細胞脫落較少,在同等劑量下對腫瘤血管的攻擊力不如本發明GF-Ala藥物。
