特異性靶向骨肉瘤細胞的適配子及其製備方法和應用與流程
2023-10-10 20:52:19 8
本發明涉及生物技術領域,具體涉及一種特異性靶向骨肉瘤細胞的適配子及其製備方法和應用。
背景技術:
骨肉瘤是骨惡性腫瘤中最多見的一種,是從間質細胞系發展而來,腫瘤迅速生長是由於腫瘤經軟骨階段直接或間接形成腫瘤骨樣組織和骨組織。骨肉瘤病理確診後需要即刻進行放化治療,截肢手術則作為傳統切除腫瘤組織的重要方法。該方式對病情起到了較好的控制效果,但對患者的身心傷害較大,嚴重影響術後生存質量。雖然通過新輔助化療結合手術治療,其預後有較大改善,5年生存率由20世紀70年代末的10%左右上升到如今的60%左右,但近30多年間,骨肉瘤經手術治療3年後有30-40%的復發率,儘管進行了多種努力,一直未能取得較大進展。
而腫瘤靶向治療由於其良好的靶向性以及抗腫瘤活性已成為當今腫瘤研究領域的熱點,其中靶向分子和毒性藥物偶聯物則是靶向藥物研究的前沿。
適配子出現十多年來,已應用於酶聯寡核苷酸實驗、流式細胞儀、適配子晶片(aptamer chip)、蛋白定量及蛋白純化等體外實驗,同時具有可在體內抑制生長因子和受體的相互作用或抑制酶活性等功能,還可進行體內成像等。適配子可以作為診斷和治療試劑,用於診斷時可識別與結合特定靶分子,用於治療疾病時可作為靶向輸送、功能阻斷物質或者直接阻斷疾病進程。
設計靶向藥物和毒性藥物偶聯物,首先要做的是選擇一個合適的靶向 分子。靶向腫瘤細胞表面特異性蛋白的核酸適配子具有良好的水溶性和顯著的腫瘤靶向性,相對於抗體而言,具有化學穩定性高、免疫原性和毒性低、分子量小易於進入細胞、易於合成和修飾等特點。
SELEX(systematic evolution of ligands by exponential enrichment)技術是九十年代發展起來的一種新的體外篩選技術,它運用大容量的隨機寡核苷酸文庫,並結合體外PCR擴增技術,以指數富集與靶分子特異結合的寡核苷酸,經過多輪篩選,獲得高親合力、特異性強的寡核苷酸適配子(aptamers),已成功運用於許多靶分子的篩選,包括金屬離子、有機染料、蛋白質、藥物、胺基酸以及各種細胞因子等,甚至可用於完整的細胞、病毒、孢子和朊病毒等。陳孜等人介紹了SELEX篩選骨肉瘤HER2適配體方法的建立(西安交通大學學報)2014年05期),該方法以HER2蛋白作為靶標進行了適配子篩選,但HER2蛋白不僅僅在骨肉瘤高表達,同時也在其他腫瘤細胞中高表達。
目前,尋找新的特異性靶向骨肉瘤細胞的適配子本領域技術人員研究的重點。
技術實現要素:
針對以上技術情況,本發明提供一種僅以骨肉瘤細胞作為靶標的,特異性針對骨肉瘤細胞的靶向適配子,從而在可以治療應用中實現更好治療效果。具體地,本發明提供一種能夠靶向骨肉瘤的適配子及其製備方法和應用,本發明適配子不僅可以用於診斷骨肉瘤疾病,還可以與已知具有治療骨肉瘤的藥物特異性地結合,將該藥物靶向骨肉瘤細胞從而實現對骨肉瘤疾病的靶向治療。
本發明所述適配子具有SEQ ID NO.1、SEQ ID NO.2或SEQ ID NO.3所示的核苷酸序列:
本發明通過以骨肉瘤細胞為靶的指數富集配體系統進化技術篩選得到的適配子是一種單鏈的寡核苷酸序列,可以特異性地與靶細胞結合。
本發明適配子作為靶向配體應用在藥物的細胞靶向遞送過程中,本發明適配子與抗骨肉瘤藥物結合後可以特異性靶向骨肉瘤細胞,為提高治療效果,並為降低肝臟毒性提供了解決途徑。
本發明提供一種特異性靶向骨肉瘤細胞的適配子的篩選、製備、分離方法,本發明所述方法包括:
1)適配子的篩選
準備上述隨機ssDNA文庫、FITC標記的正向引物和Biotin標記的反向引物;
選擇大鼠成骨細胞為靶細胞,大鼠肝細胞系和外周血單核細胞為非靶細胞,採用無酶的細胞消化液處理生長良好的細胞,接種於培養皿中,過夜培養,當細胞長至95%時即可用於文庫篩選;
將靶細胞消化,並與隨機文庫用孵育緩衝液孵育;
孵育結束後將細胞離心,加入雙蒸水,收集上清液,上清液中含有第一輪篩選與靶細胞結合的單鏈DNA,用於PCR擴增,製備下一輪篩選亞文庫;
PCR產物dsDNA經濃縮管濃縮後,與鏈親合素-磁珠進行孵育,加入鹼性溶液進行鹼變性,使得Biotin-ssDNA與鏈親合素結合後固定在磁珠上,游離的FITC-ssDNA亞文庫則被分離出來;然後取上清液,加入酸溶液進行中和;
將上述FITC-ssDNA亞文庫進行高解析度的瓊脂糖電泳,再次分離FITC-ssDNA及其中的汙染序列(dsDNA);
溴化乙錠染色10分鐘,紫外燈下切取FITC-ssDNA的目標條帶,通過小分子量DNA純化回收試劑盒進行回收;
2)適配子的富集
僅在第一輪篩選中對靶細胞進行孵育,從第二輪開始,正篩以後引入 非靶細胞負篩過程;最後離心收集上清液,棄去與非靶細胞結合的序列,重複上述過程5-20個循環;
3)適配子的測序:
將最後富集到的文庫PCR擴增成雙鏈DNA,使用克隆試劑盒進行克隆,經藍白斑篩選,挑選克隆進行測序;根據測序結果使用RNA structure軟體和DNAMAN軟體進行一級序列和二級結構的分析,即得。
作為本發明實施方案之一,所述方法步驟1)中的孵育緩衝液可以本領域常用的適於本發明的各種緩衝溶液,本發明優選為含有1.0mM MgCl2,0.1mg/ml酵母tRNA和0.1mg/ml鮭魚精DNA的磷酸緩衝溶液;
作為本發明實施方案之一,所述方法步驟1)中PCR的反應條件可以有本領域技術人員結合本發明和本領域技術人員進行確定,作為實施方案之一,本發明優選PCR反應條件為:94度預變性3min,94度變性30s,56度退火30s,72度延伸30s,最後72度延伸5min。
作為本發明實施方案之一,所述方法步驟1)中的鹼溶液可以選用本領域常用的鹼性溶液,本發明包括但不限於鹼溶液為200mM的NaOH溶液;
作為本發明實施方案之一,所述方法步驟1)中的酸溶液可以選用本領域常用的酸性溶液,本發明包括但不限於酸溶液為100mM鹽酸。
作為本發明實施方案之一,所述方法步驟1)中的電泳條件為:瓊脂糖電泳,電壓設定為180V,電泳時間為40分鐘。
作為本發明實施方案之一,所述特異性靶向骨肉瘤細胞的適配子的製備方法進一步包括:
1)適配子的篩選
準備上述隨機ssDNA文庫、FITC標記的正向引物和Biotin標記的反向引物;
選擇大鼠成骨細胞ROS17/2.8(ATCC)為靶細胞,大鼠肝細胞系BRL-3A(ATCC)和外周血單核細胞為非靶細胞,採用無酶的細胞消化液處理生長良好的細胞,按照5×106接種於培養皿中,過夜培養,當細胞長至95%時即可用於文庫篩選;
將靶細胞消化下來,與隨機文庫在37度條件下孵育1小時,孵育緩衝 液為含有1.0mM MgCl2,0.1mg/ml酵母tRNA和0.1mg/ml鮭魚精DNA的PBS;
孵育結束後將細胞離心下來,加入雙蒸水,100度水浴加熱10分鐘,收集上清液,上清液中含有第一輪篩選與靶細胞結合的單鏈DNA,用於PCR擴增,製備下一輪篩選亞文庫;
PCR反應條件為:94度預變性3min,94度變性30s,56度退火30s,72度延伸30s,最後72度延伸5min;
PCR產物dsDNA經濃縮管濃縮後,與鏈親合素-磁珠在37度孵育1小時,加入200mM NaOH溶液進行鹼變性7分鐘,打破dsDNA之間的氫鍵,使得Biotin-ssDNA與鏈親合素結合後固定在磁珠上,游離的FITC-ssDNA亞文庫則被分離出來;取上清液,加入適量100mM鹽酸溶液進行中和;
將上述FITC-ssDNA亞文庫進行高解析度的瓊脂糖電泳,電壓設定為180V,電泳時間為40分鐘,再次分離FITC-ssDNA及其中的汙染序列;
溴化乙錠染色10分鐘,紫外燈下切取FITC-ssDNA的目標條帶,通過小分子量DNA純化回收試劑盒進行回收;
2)適配子的富集
為了減少ssDNA文庫的損失,第一輪篩選中僅對靶細胞進行孵育;從第二輪開始,正篩以後引入非靶細胞負篩過程;正篩孵育過程與上述一致,負篩過程中,37度環境下孵育1小時以後,離心收集上清液,棄去與非靶細胞結合的序列;
重複上述過程5-20個循環,為了獲得較高親和力和特異性的適配子,隨著篩選輪數的增加,逐漸增加洗滌力度,洗滌次數也從3次增加到5次,洗滌時間從3分鐘增加到5分鐘。
篩選過程中每隔幾個循環使用流式細胞儀對富集情況進行分析;將靶細胞和非靶細胞消化下來,用富集文庫與其進行37度孵育1小時,PBS洗三次後,加入400ul PBS重懸細胞,流式細胞儀分析螢光強度;待螢光強度達到一定程度時,終止篩選;
3)適配子的測序:
將最後富集到的文庫PCR擴增成雙鏈DNA,使用克隆試劑盒進行克隆, 經藍白斑篩選,挑選多個克隆並進行測序,然後使用RNA structure軟體和DNAMAN軟體進行一級序列和二級結構的分析;根據分析結果進行截斷和鑑定,即得一級序列為:
作為實施方案之一,本發明提供一種所述適配子用於製備識別骨肉瘤細胞的生物探針的應用;
作為實施方案之一,本發明提供一種所述適配子作為特異性靶向骨肉瘤細胞的藥物的載體的應用,其中可以以本發明所述適配子作為特異性靶向骨肉瘤細胞的載體的藥物包括但不限於雷公藤甲素。
本發明所述適配子能夠特異性靶向骨肉瘤細胞並對肝細胞及外周血細胞不親和。
本發明實驗中,以SEQ ID NO.3(以下簡稱「LC6」)的適配子作為雷公藤甲素(以下簡稱「TP」)特異性靶向骨肉瘤細胞的載體的示例進行了相關的實驗,LC6適配子成功實現了TP特異性靶向骨肉瘤細胞,提高了抗骨肉瘤的活性,並降低了肝臟毒性。
附圖說明
圖1:骨肉瘤適配子的篩選;
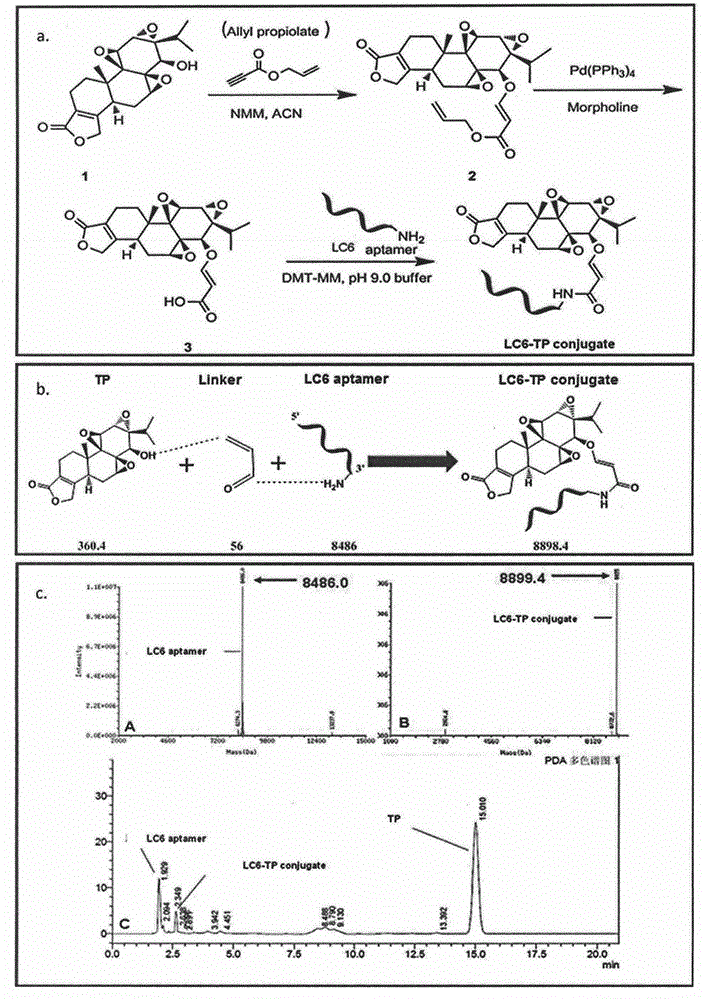
圖2a:LC6-TP偶聯物的化學合成流程圖;
圖2b:TP、Linker、LC6和LC6-TP偶聯物的理論分子量;
圖2c:LC6和LC6-TP偶聯物的質譜分析;
圖3a:LC6-TP偶聯物在血漿和不同pH的PBS中的穩定性;
圖3b:LC6-TP偶聯物與OS細胞、正常成骨細胞和肝臟細胞的結合能力;
圖3c:MTT測試不同濃度LC6-TP偶聯物和Dox對OS細胞的生存能力的影響。
具體實施方式
以下實施例僅用於進一步闡述本發明,但不以任何的方式限制本發明的有效範圍。
實施例1適配子的篩選、製備
1.實驗材料:
1.1 ssDNA文庫、FITC標記的正向引物和Biotin標記的反向引物:ssDNA文庫:
5』-ATCCAGAGTGACGCAGCA-55nt-TGGACACGGTGGCTTAGT-3』
5』引物:5』-FITC-ATCCAGAGTGACGCAGCA-3』;
3』引物:5』-biotin-ACTAAGCCACCGTGTCCA-3』;均由上海生工生物工程公司提供。
1.2大鼠成骨細胞:ROS17/2.8,購自中科院細胞庫,培養液為10%胎牛血清的DMEM培養基。
1.3大鼠肝細胞:BRL-3A,購自中科院細胞庫,培養液為10%胎牛血清的DMEM培養基。
大鼠外周血細胞:PBMCs,直接從大鼠外周血中分離。
1.4培養液:DMEM培養基和胎牛血清購自Gbico公司
1.5流式細胞儀:購自BD Immunocytometry Systems
1.6 CH倒置光學顯微鏡:購自日本奧林巴斯公司
1.7 PCR試劑盒(貨號:R011)、DNA Marker(20bp DNA ladder(Dye plus),貨號:3420A)和瓊脂糖凝膠(Agarose MS-6,貨號:D615)購自大連Takara公司
1.8小分子量DNA純化回收試劑盒(貨號:ZP205)購自Beijing Zoman Biotechnology,Co.,LTD
1.9鏈親合素的磁珠(貨號:Z5482)購自Promega公司
1.10噻唑藍(MTT,貨號:M2128)購自Sigma公司
1.11 PCR儀購自美國Perkin Elmer公司。
1.12紫外凝膠成像系統購自Rio-Rad公司。
1.13濃縮管(Amicon Ultra-15 centrifugal Filter-10k)購自Merck Milipore公司。
2.實驗方法:
2.1適配子的篩選
準備上述隨機ssDNA文庫、FITC標記的正向引物和Biotin標記的反向引物。
選擇大鼠成骨細胞ROS17/2.8(ATCC)為靶細胞,大鼠肝細胞系BRL-3A(ATCC)和外周血單核細胞為非靶細胞,採用無酶的細胞消化液處理生長良好的細胞,按照5×106接種於培養皿中,過夜培養,當細胞長至95%時即可用於文庫篩選。
將靶細胞消化下來,與隨機文庫在37度條件下孵育1小時,孵育緩衝液為含有1.0mM MgCl2,0.1mg/ml酵母tRNA和0.1mg/ml鮭魚精DNA的磷酸緩衝溶液(PBS)。
孵育結束後將細胞離心下來,加入雙蒸水,100度水浴加熱10分鐘,收集上清液,上清液中含有第一輪篩選與靶細胞結合的單鏈DNA,用於PCR擴增,製備下一輪篩選亞文庫。
PCR反應條件為:94度預變性3min,94度變性30s,56度退火30s,72度延伸30s,最後72度延伸5min。
PCR產物dsDNA經濃縮管(Amicon Ultra-15 centrifugal Filter-10k)濃縮後,與鏈親合素-磁珠(Z5482,Promega)在37度孵育1小時,加入200mM NaOH溶液進行鹼變性7分鐘,打破dsDNA之間的氫鍵,使得Biotin-ssDNA與鏈親合素結合後固定在磁珠上,游離的FITC-ssDNA亞文庫則被分離出來。取上清液,加入適量100mM鹽酸溶液進行中和。
將上述FITC-ssDNA亞文庫進行高解析度的瓊脂糖電泳(D615,Takara),電壓設定為180V,電泳時間為40分鐘,再次分離FITC-ssDNA及其中的汙染序列(dsDNA)。
溴化乙錠染色10分鐘,紫外燈下切取FITC-ssDNA的目標條帶,通過小分子量DNA純化回收試劑盒(ZP205,Beijing Zoman Biotechnology,Co.,LTD)進行回收。
2.2適配子的富集
為了減少ssDNA文庫的損失,第一輪篩選中僅對靶細胞進行孵育。從第二輪開始,正篩以後引入非靶細胞負篩過程。正篩孵育過程與上述一致,負篩過程中,37度環境下孵育1小時以後,離心收集上清液,棄去與非靶細胞結合的序列。
重複上述過程5-20個循環,為了獲得較高親和力和特異性的適配子,隨著篩選輪數的增加,逐漸增加洗滌力度,洗滌次數也從3次增加到5次,洗滌時間從3分鐘增加到5分鐘。
篩選過程中每隔幾個循環使用流式細胞儀對富集情況進行分析。將靶細胞和非靶細胞消化下來,用富集文庫與其進行37度孵育1小時。PBS洗三次後,加入400ul PBS重懸細胞,流式細胞儀分析螢光強度。待螢光強度達到一定程度時,終止篩選。
2.3適配子的測序:
將最後富集到的文庫PCR擴增成雙鏈DNA,使用克隆試劑盒(Invitrogen,cat.no.K4500-01)進行克隆,經藍白斑篩選,隨機挑選多個克隆進行測序。
根據測序結果使用RNA structure軟體和DNAMAN軟體進行一級序列和二級結構的分析。根據分析結果進行截斷和鑑定。最後挑選出三條候選適配子,一級序列為:
2.4 HPLC分析
將細胞裂解,取0.2mL細胞裂解液,加入50ul I.S.(2ug/ml),和1.2mL乙酸乙酯溶液,震蕩後離心5分鐘。取有機溶液1mL水浴乾燥,0.1mL甲醇復溶,4度離心10分鐘。取上清液(10ul)進樣分析。
色譜條件:Zorbax Extend-C18色譜柱(Agilent Technologies,U.S.A.),ODS預柱(Security Guard,U.S.A.),柱溫30度,流動相為甲醇/乙腈/水(15/20/65,v/v/v%),流速1.0ml/min,檢測波長218nm。
實驗例1適配子、雷公甲素-適配子耦合物的靶向骨肉瘤細胞的實驗
1.1適配子的靶向骨肉瘤細胞的實驗
1.1.1實驗方法
取本發明實施例1製備的適配子LC4、LC5、LC6,濃度為200nM,與骨肉瘤細胞、肝臟細胞和外周血單核細胞於37度環境下孵育1小時以後,流失細胞儀檢測螢光強度,細胞數為20,000。
1.1.2實驗結果
本發明所述LC4、LC5、LC6的適配子流失細胞儀數據顯示所述三條序列都可以特異性結合大鼠骨肉瘤細胞,同時與大鼠肝細胞和外周血單核細胞沒有明顯結合(圖1)。
1.2 LC6-雷公藤甲素(以下簡稱「LC6-TP」)靶向骨肉瘤實驗
1.2.1 LC6-雷公藤甲素(以下簡稱「LC6-TP」)的製備
LC6-TP製備方法按照圖2a所示的方法進行製備,且TP、Linker、LC6和LC6-TP偶聯物的理論分子量如圖2b所示;(c)LC6和LC6-TP偶聯物的質譜分析如圖2c所示。
1.2.2實驗方法及結果
LC6-TP偶聯物的pH敏感性:為了檢測LC6-TP偶聯物在體外的pH敏感性,LC6-TP偶聯物分別與血漿(pH 7.4)和不同pH值的磷酸緩衝溶液(PBS)孵育,HPLC分析不同時間點游離TP單體在血漿和PBS中的含量。 結果顯示,在孵育的過程中,血漿中沒有檢測到明顯的游離TP單體。然而,在不通pH的PBS中,隨著孵育時間的延長,越來越多的TP可以被檢測到。而且,在同一時間點,隨著pH值的降低,TP的含量逐漸增加(如圖3所示)
LC6-TP偶聯物的體外細胞選擇性實驗
為了研究LC6-TP偶聯物的體外細胞選擇性,Cy3螢光標記的LC6-TP偶聯物和陰性對照CRO-TP偶聯物(CRO為非特異核酸序列,作為LC6的對照)分別與骨肉瘤細胞、正常成骨細胞和肝臟細胞孵育,流式細胞儀分析螢光強度。結果顯示在骨肉瘤細胞中,LC6-TP的螢光強度明顯高於正常成骨細胞和肝臟細胞中的螢光強度。而CRO-TP偶聯物在三種細胞中均沒有明顯螢光(圖3)。
LC6-TP偶聯物的體外抗腫瘤活性實驗
為了檢驗LC6-TP偶聯物的體外抗腫瘤活性,化療藥物抵抗的骨肉瘤細胞分別與Dox和LC6-TP偶聯物孵育,MTT測試分析細胞生存能力。結果顯示,與Dox和LC6-TP偶聯物孵育的成骨細胞生存能力隨著濃度增加而下降。而且,在相同濃度,LC6-TP偶聯物可以更有效殺死骨肉瘤細胞。LC6-TP偶聯物的IC50比Dox低大約100倍。該結果表明LC6-TP偶聯物的抗腫瘤能力明顯強於Dox(圖3)。
1.2.3實驗結論
實驗結果顯示本發明適配子及其與雷公藤甲素耦聯物均能夠成功地靶向骨肉瘤細胞,而且LC6-TP偶聯物在生理pH條件下維持穩定而在骨肉瘤酸性環境下發生斷裂,從而釋放TP。在相同濃度下、LC6-TP偶聯物可以更有效殺死骨肉瘤細胞。
