包括含有活性成分的膜包衣層的複合製劑的製作方法
2023-12-03 17:21:06 5
本發明涉及一種包括含有活性成分的膜包衣層的複合製劑及其製備方法,更具體地,涉及一種包括含有活性成分的膜包衣層的複合製劑,其可以具有對通常外部衝擊的穩定形狀和耐久性以及活性成分的高溶出度,以及所述複合製劑的製備方法。
背景技術:
健康的年輕男子的前列腺為約核桃的大小,並隨著年齡逐漸增長。前列腺肥大為由於前列腺的嚴重擴大壓迫經過前列腺的尿道以導致各種症狀的疾病。
雖然尚未清楚地確定,但是已知前列腺肥大的原因為如在其它慢性疾病中的各種複雜因素。目前公認的前列腺肥大的原因為正常睪丸的衰老。前列腺為雄激素(男性性激素)依賴性器官,其需要連續供應用於正常生長和功能的雄激素。如果雄性激素由於閹割不再產生,前列腺可能收縮。
前列腺肥大的症狀包括下尿路症狀(LUTS),其包括由膀胱儲存障礙引起的症狀,例如每天八次或更多次的頻繁排尿、夜尿症、伴有強烈突然的排尿感覺以及強烈渴望排尿的緊急排尿、緊急尿失禁和疼痛排尿(排尿困難);和由膀胱排出障礙引起的症狀,例如延遲排尿(其中患者必須等待排尿開始)、中斷排尿(具有間歇尿流)、壓力排尿(其中患者必須施加壓力以開始排尿)、弱尿流、不完全排空的感覺和尿瀦留。
5-α-還原酶抑制劑為通常用於治療前列腺肥大的藥物,其可以單獨使用,並且還已知與坦索羅辛或5型磷酸二酯酶抑制劑(例如他達拉非、伐地那非、或烏地那非)一起使用以更有效地治療前列腺肥大。
5-α-還原酶抑制劑可以抑制睪酮轉化為二氫睪酮以進一步增強前列腺的擴大,並因此可以阻斷前列腺的擴大並從身體壓力中緩解尿道。
坦索羅辛為在泌尿生殖器官中選擇性地阻斷α-腎上腺素受體的藥物,並且已知通過鬆弛膀胱周圍的前列腺和平滑肌來改善排尿率,並緩解良性前列腺肥大的症狀。
作為5型磷酸二酯酶抑制劑的他達拉非(Cialis,Lilly ICOS)和伐地那非(Levitra,GSK)最初被開發為用於治療陽痿的藥物。然而,這些藥物越來越多地用於更多適應症,例如前列腺肥大和膀胱過動症(Euro Urol 2008;1236-44;J Uro 2007;1401-7)。
藥物聯用例如5-α-還原酶抑制劑和坦索羅辛的藥物聯用或5-α-還原酶抑制劑和5型磷酸二酯酶抑制劑的藥物聯用,由於聯用中施用的兩種活性成分的不同作用機制而在功效增強方面具有優勢(EP 1 501 517;BJU Int.2006Apr.97Suppl 2:39-43;discussion 44-5)。
然而,在製備包括兩種或更多種活性成分(例如上述藥物聯用)的複合製劑時,由於兩種或更多種不同活性成分之間的相互作用,可能出現與活性成分的穩定性有關的問題。為了確保這種複合製劑的穩定性,已經開發了一種複合製劑,其包括含有活性成分的芯和含有另一種活性成分的膜包衣層,其中兩種活性成分分離為不同的層(EP 1 830 820;US 6,682,759)。
在這種包括含有活性成分的膜包衣層的複合製劑中,如果膜包衣層具有不足的拉伸強度,則在產品的儲存期間通常的衝擊可能使膜包衣層分離或破裂,由於外觀和其它性質的變化,使得可能難以確保複合製劑的足夠功效以及保持可商售產品的質量,最終導致不能將製劑作為產品商業化。對於口服的該複合製劑,為了確保足夠的生物利用度和快速功效,需要膜包衣層中含有的活性成分的高溶出度。
技術實現要素:
技術問題
本發明提供了一種複合製劑,其包括含有活性成分的膜包衣層,其可以具有對通常外部衝擊的穩定形狀和耐久性以及活性成分的高溶出度。
本發明提供了一種製備包括含有活性成分的膜包衣層的複合製劑的方法。技術方案
根據本發明的一方面,提供了一種複合製劑,其包括:含有第一活性成分的芯;和含有第二活性成分的膜包衣層,其中所述膜包衣層包括聚乙烯醇-聚乙二醇接枝共聚物和聚乙烯醇。
根據本發明的另一方面,提供了一種製備上述複合製劑的方法,所述方法包括:製備含有第一活性成分的芯;製備含有第二活性成分的包衣溶液,其中將所述第二活性成分、聚乙烯醇-聚乙二醇接枝共聚物和聚乙烯醇溶解在溶劑中;和用所述含有第二活性成分的包衣溶液包覆所述芯。
有利效果
根據本發明的一個或多個實施方式,複合製劑可以包括含有活性成分的膜包衣層,其具有對通常的外部衝擊的強拉伸強度耐受性,並且確保該膜包衣層中含有的活性成分的高溶出度。因此,複合製劑因為在外部衝擊的情況下不發生外觀和性質的變化,因此可具有高的可銷售產品質量,並且可以確保足夠的生物利用度和快速作用而不喪失功效。含有兩種或更多種不同活性成分的複合製劑可用作具有良好的可銷售產品質量的有效複合製劑,並且可以改善患者對於藥物的聯合給藥的依從性。此外,由於複合製劑中包括膜包衣層,複合製劑可以具有顯著減小的體積,並因此與通過簡單地組合各自單一製劑的組合物製備的複合製劑相比,可以為顯著減小尺寸的片劑或膠囊的形式,增加了患者服給藥物時的方便性。
附圖說明
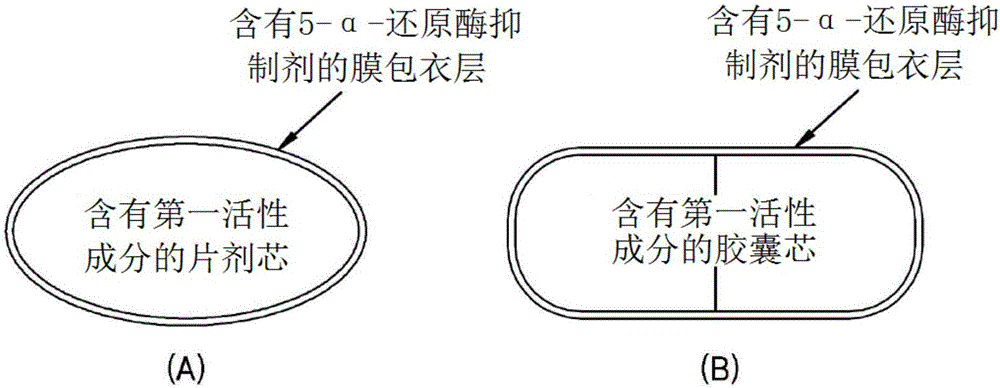
圖1為表示包括在含有第一活性成分的片劑芯的表面上包覆含有第二活性成分的膜包衣層的複合製劑(a)和包括在含有第一活性成分的硬膠囊芯的表面上包覆含有第二活性成分的膜包衣層的複合製劑(b)的示意圖;
圖2為複合製劑的照片圖像,其中一個評價為可接受的產品(a),而且另一個評價為有缺陷的產品(b);
圖3為表示比較例1至8的複合製劑在打開其PTP包裝時評價的缺陷率的圖;
圖4為表示實施例1至10的複合製劑在打開其PTP包裝時評價的缺陷率的圖;
圖5為表示關於比較例1至4的複合製劑的包衣材料在約60℃和相對溼度(RH)0%下保存1周後打開其PTP包裝時評價的缺陷率的圖;
圖6為表示從比較例1至4的複合製劑中非那雄胺的溶出度的圖;
圖7為表示從實施例2至5的複合製劑中非那雄胺的溶出度的圖;和
圖8為表示實施例3、11和12的複合製劑關於不同芯型在打開其PTP包裝時評價的缺陷率的圖。
具體實施方式
除非另有定義,本文使用的所有術語(包括技術和科學術語)具有與本發明所屬領域的普通技術人員通常理解的相同含義。雖然本文中列出了示例性方法或材料,但是其它類似或等同物也在本發明的範圍內。本文中作為參考文獻公開的所有出版物通過引用整體併入本文。
作為對包括含有活性成分的膜包衣層的複合製劑所用的包衣材料進行深入研究的結果,所述包衣材料確保含有活性成分的膜包衣層的足夠拉伸強度,以及膜包衣層中含有的活性成分的高溶出度,本發明的發明人發現,當使用聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的組合作為含有活性成分的膜包衣層的材料時,與使用其它膜包衣材料時相比,含有活性成分的膜包衣層可以具有足夠強的拉伸強度,以致在儲存期間不會因常規衝擊而分離或破裂,以及膜包衣層中含有的活性成分的高溶出度。
本發明的一方面提供了一種複合製劑,其包括:含有第一活性成分的芯;和含有第二活性成分的膜包衣層,其中所述膜包衣層包括聚乙烯醇-聚乙二醇接枝共聚物和聚乙烯醇。
含有第一活性成分的芯可以為通常用於藥物領域的任何藥物製劑。例如,芯可以為片劑、硬膠囊或軟膠囊的形式。然而,實施方式不限於此。硬膠囊或軟膠囊的填充劑部分可以為通常用於藥物領域的任何藥物製劑形式,例如顆粒、丸劑、粉劑、片劑、液劑或其任意組合。
芯可以為複合製劑總重量的約20wt%至99.5wt%。
含有第二活性成分的膜包衣層可以在芯的表面上。所述膜包衣層可以包括聚乙烯醇-聚乙二醇接枝共聚物和聚乙烯醇的組合作為包衣材料。
本發明的發明人通過用包括第二活性成分和不同包衣材料的膜包衣層包覆含有第一活性成分的片劑或膠囊芯而製備使用各種包衣材料的複合製劑,並對不同的包衣材料進行檢測測試和第二活性成分隨時間的溶出試驗。結果當單獨使用聚乙烯醇-聚乙二醇接枝共聚物、聚乙烯醇、聚維酮或羥丙甲纖維素作為包衣材料時,由於如從芯分離或斷裂的因素引起的複合製劑的膜包衣層的缺陷率高達20至40%,僅在使用聚乙烯醇時小於2%(參見試驗例1和3)。然而,當使用聚乙烯醇作為包衣材料時,使用韓國藥典的一般試驗的溶出試驗評價,複合製劑在15分鐘內具有小於75%的第二活性成分的低溶出度(參見試驗例4)。因此,難以獲得確保高拉伸強度和足夠高的溶出度的膜包衣層。另一方面,當使用聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的組合時,由於例如與芯分離或斷裂的因素引起的膜包衣層的缺陷率顯著降低至小於10%(參見試驗例2和6),並且第二活性成分在15分鐘內具有約75%或更高的足夠高的溶出度(參見試驗例5),表明顯著的結果顯示出實現了低的膜包衣缺陷率和高溶出度。
在一些實施方式中,聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇可以以約8:2至約4:6的重量比,並在一些實施方式中,以約7:3至約4:6的重量比,並在一些其它實施方式中,以約6:4使用。
聚乙烯醇-聚乙二醇接枝共聚物可以由約65%至約85%的聚乙烯醇單元和約15至35%的聚乙二醇單元組成,可以含有約0.01%至約0.5%的膠體二氧化矽,並且可以具有約35,000道爾頓至約55,000道爾頓的重均分子量。聚乙烯醇-聚乙二醇接枝共聚物可商購獲得,例如作為IR(可得自BASF),其由約75%的聚乙烯醇單元和約25%的聚乙二醇單元組成,含有約0.3%的膠體二氧化矽,並具有約45,000道爾頓的重均分子量。
作為水溶性聚合物的聚乙烯醇可以具有約20,000道爾頓至約200,000道爾頓的分子量,其中分子量變得越大,則粘度可能變得越高。
膜包衣層相對於100重量份的芯,可以為約0.5重量份至約80重量份。
在一些實施方式中,複合製劑的聚乙烯醇-聚乙二醇接枝共聚物可以包括約65%至約85%的聚乙烯醇單元和約15%至約35%的聚乙二醇單元,可以含有約0.01wt%至約0.5wt%的膠體二氧化矽,並且可以具有約35,000道爾頓至約55,000道爾頓的重均分子量;聚乙烯醇可具有約20,000道爾頓至約200,000道爾頓的分子量;並且聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的重量比可以為約7:3至約4:6。
圖1為表示根據實施方式的複合製劑的示意圖。
在圖1中,(a)為表示在包括第一活性成分的片劑芯的表面上包覆含有第二活性成分的膜包衣層的複合製劑的示意圖;且(b)為表示在含有第一活性成分的硬膠囊芯的表面上包覆含有第二活性成分的膜包衣層的複合製劑的示意圖。
在一些實施方式中,複合製劑還可以包括內包衣層,其將芯和膜包衣層彼此分離以更有效地防止活性成分之間的相互作用。相對於100重量份的芯,內包衣層可以為約0.01重量份至約60重量份。例如,可用於內包衣層的成膜材料(成膜劑和/或包覆劑)可以為羥丙基甲基纖維素、羥丙基纖維素、羥乙基纖維素、鄰苯二甲酸乙酸纖維素、乙基纖維素、甲基纖維素、聚甲基丙烯酸酯、聚乙二醇、滑石、二氧化鈦或其混合物。然而,實施方式不限於此。可以使用在藥物領域中通常用於形成用於口服或腸胃外施用的固體製劑的任何成膜材料。
在一些實施方式中,複合製劑還可以包括圍繞含有活性成分的膜包衣層的外包衣層,以進一步保護複合製劑免受外部環境的影響。外包衣層可以為不顯著影響含有活性成分的膜包衣層的高拉伸強度和第二活性成分的高溶出度的任何包衣層,這是複合製劑的預期目的。這種外包衣層可以通過防潮包衣或拋光包衣獲得。本領域普通技術人員可以根據包衣的類型基於本領域中已知的知識選擇合適的材料。
相對於100重量份的芯,外包衣層可以為約0.01重量份至約60重量份。
在一些實施方式中,除了上述成分之外,複合製劑可以在芯和含有活性成分的膜包衣層中還包括藥學上可接受的添加劑。添加劑可以選自稀釋劑、崩解劑、粘合劑、穩定劑、潤滑劑及其任意組合。
稀釋劑可以選自微晶纖維素、乳糖、Rudy press、甘露醇、磷酸二氫鈣、澱粉、低取代羥丙基纖維素及其任意組合。然而,實施方式不限於此。
崩解劑可以選自交聚維酮、澱粉乙醇酸鈉、交聯羧甲基纖維素鈉、低取代羥丙基纖維素、澱粉、藻酸、藻酸鈉及其任意組合。然而,實施方式不限於此。
粘合劑可以選自羥丙基纖維素、羥丙基甲基纖維素、聚乙烯基吡咯烷酮、共聚維酮、聚乙二醇、輕質無水矽酸、矽酸鹽衍生物(例如合成矽酸鋁、矽酸鈣和偏矽酸鋁酸鎂)、磷酸鹽(例如磷酸氫鈣)、碳酸鹽(例如碳酸鈣)及其任意組合。然而,實施方式不限於此。
穩定劑可以選自碳酸鎂、碳酸氫鈉、碳酸鈉、碳酸鈣及其任意組合。然而,實施方式不限於此。
潤滑劑可以選自硬脂酸、硬脂酸的金屬鹽(例如硬脂酸鈣或硬脂酸鎂)、滑石、膠體二氧化矽、蔗糖脂肪酸酯、氫化植物油、高熔點蠟、甘油脂肪酸酯、甘油二山萮酸酯及其任意組合。然而,實施方式不限於此。
本文中所用的術語「活性成分」不僅指用於治療目的的任何藥理學活性劑,而且還指為了診斷或預防目的可以施用到人體中的任何試劑或任何醫學試劑。在廣義上,「活性成分」可以為其加工形式的任何材料、成分或健康功能性食品,其可以用於保健目的,以進行影響身體結構和功能的營養調節功能或生理功能。
本文中所用的術語「第一活性成分」和「第二活性成分」用於將複合製劑的至少兩種活性成分彼此區分,其中為了便於描述,將在複合製劑的芯中含有的活性成分稱為第一活性成分,並且將在膜包衣層中含有的活性成分稱為第二活性成分。
第一活性成分和第二活性成分可以為需要聯合給藥的任何藥物,例如二甲雙胍和羅蘇伐他汀、非諾貝酸和羅蘇伐他汀、ω-3和羅蘇伐他汀、氨氯地平和氯沙坦、氯吡格雷和阿司匹林、二甲雙胍和格列本脲、納洛酮和羥考酮、非索非那定和孟魯司特、布林佐胺和噻嗎洛爾、樂卡地平和依那普利、坦索羅辛和5-α-還原酶抑制劑、5型磷酸二酯酶抑制劑和5-α-還原酶抑制劑、萘普生和埃索美拉唑、或二甲雙胍和格列本脲。如果需要,第一活性成分和第二活性成分中的每種可以包括單一成分或多種成分。
在一些實施方式中,複合製劑可以為口服劑型。
在一些實施方式中,第二活性成分可以為5-α-還原酶抑制劑,並且第一活性成分可以為需要與5-α-還原酶抑制劑聯合給藥的任何活性成分。例如,第一活性成分可以包括坦索羅辛或5型磷酸二酯酶抑制劑(例如他達拉非、伐地那非、烏地那非、或西地那非)。
也已知5-α-還原酶抑制劑和坦索羅辛的組合以及5-α-還原酶抑制劑和5型磷酸二酯酶抑制劑的組合在治療前列腺肥大上有效,並且也已知在功效提高方面是有利的,這是由於各個活性成分的不同機制(EP 1 501 517;BJU Int.2006Apr 97Suppl 2:39-43;Discussion 44-5)。因此,當包括坦索羅辛或5型磷酸二酯酶抑制劑作為第一活性成分並且包括5-α-還原酶抑制劑作為第二活性成分時,根據任一實施方式的複合製劑可以用作有效的前列腺治療製劑。
在一些實施方式中,第一活性成分可以為坦索羅辛或其藥學上可接受的鹽,並且第二活性成分可以為5-α-還原酶抑制劑。
5-α-還原酶抑制劑可以選自非那雄胺、度他雄胺、阿法烷二醇(alfatradiol)及其任意組合。使用根據韓國藥典的一般試驗的溶出試驗評價時,複合製劑中5-α-還原酶抑制劑的15分鐘內的溶出度可以為約75%或更高。
在一些實施方式中,考慮到已知的日劑量,按照游離鹼的量表示,複合製劑可以包括約0.1mg至約0.8mg,並在一些其它實施方式中,約0.2mg至約0.6mg的坦索羅辛或其藥學上可接受的鹽作為第一活性成分,以及約1mg至約10mg的非那雄胺作為第二活性成分。
在一些實施方式中,考慮到已知的日劑量,按照游離鹼的量表示,複合製劑可以包括約0.1mg至約0.8mg,並在一些其它實施方式中,約0.2mg至約0.6mg的坦索羅辛或其藥學上可接受的鹽作為第一活性成分,以及約0.2mg至約0.6mg的度他雄胺作為第二活性成分。
在一些實施方式中,第一活性成分可以為5型磷酸二酯酶抑制劑,並且第二活性成分可以為5-α-還原酶抑制劑。5型磷酸二酯酶抑制劑可以為他達拉非、伐地那非、烏地那非、西地那非、或其任意組合。例如,5型磷酸二酯酶抑制劑可以為他達拉非。他達拉非可以作為他達拉非游離鹼或其藥學上可接受的鹽例如氫溴酸鹽、磷酸鹽、硫酸鹽、鹽酸鹽、馬來酸鹽、富馬酸鹽、乳酸鹽、酒石酸鹽、檸檬酸鹽、苯磺酸鹽、樟腦磺酸鹽或葡糖酸鹽使用。例如,他達拉非可以為他達拉非游離鹼。然而,實施方式不限於此。
5-α-還原酶抑制劑可以選自非那雄胺、度他雄胺、阿法烷二醇及其任意組合。使用根據韓國藥典的一般試驗的溶出試驗評價時,複合製劑的5-α-還原酶抑制劑的15min內的溶出度可以為約75%或更大。
在一些實施方式中,考慮到已知的日劑量,按照游離鹼的量表示,複合製劑可以包括約5mg至約20mg,並在一些其它實施方式中,約5mg至約10mg的他達拉非或其藥學上可接受的鹽作為第一活性成分,以及約1mg至約10mg的非那雄胺作為第二活性成分。
在一些實施方式中,考慮到已知的日劑量,按照游離鹼的量表示,複合製劑可以包括約5mg至約20mg,並在一些其它實施方式中,約5mg至約10mg的他達拉非或其藥學上可接受的鹽作為第一活性成分,以及約0.2mg至約0.6mg的度他雄胺作為第二活性成分。
在一些實施方式中,複合製劑可以包括坦索羅辛或其藥學上可接受的鹽作為第一活性成分,和5-α-還原酶抑制劑作為第二活性成分;膜包衣層的聚乙烯醇-聚乙二醇接枝共聚物可以由約65%至約85%的聚乙烯醇單元和約15%至約35%的聚乙二醇單元組成,可包括約0.01wt%至約0.5wt%的膠體二氧化矽,並且可具有約35,000道爾頓至約55,000道爾頓的重均分子量;並且膜包衣層的聚乙烯醇可具有約20,000道爾頓至約200,000道爾頓的分子量,並且聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的重量比可以為約7:3至約4:6。
根據實施方式的複合製劑,其包括坦索羅辛、其藥學上可接受的鹽、或5型磷酸二酯酶抑制劑作為第一活性成分以及5-α-還原酶抑制劑作為第二活性成分,可以由於膜包衣層增強的拉伸強度而具有改善的形狀和耐久性,並且確保5-α-還原酶抑制劑的快速釋放。此外,由於在單一製劑中含有以不同機制有效治療前列腺肥大的兩種活性成分,因此複合製劑可以在治療和緩解前列腺肥大中提供協同效應,並且還可增加患者給藥依從性。
本發明的一個方面提供了製備根據任一上述實施方式的複合製劑的方法,所述方法包括:製備含有第一活性成分的芯;製備含有第二活性成分的包衣溶液,其中將所述第二活性成分、聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇溶解在溶劑中;和用包衣溶液包覆芯。
根據上述所有方面的複合製劑的上述細節可以應用於根據實施方式的其製備方法。
在芯的製備中,芯可以為能夠用作藥物領域中的芯的任何芯,例如片劑、硬膠囊或軟膠囊的形式。然而,實施方式不限於此。在芯的製備中,可以使用可以用作芯的任何市售製劑,或者可以直接製備用於本發明的芯。芯可以使用本領域普通技術人員根據芯的類型選擇的藥物領域中的已知技術製備。
在製備含有第二活性成分的包衣溶液中,溶劑可以為任何可溶解第二活性成分、聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的藥學上可用的溶劑。例如,溶劑可以為水、乙醇、甲醇、氯仿、二甲基亞碸(DMSO)或其任意組合溶液。在一些實施方式中,溶劑可以為水、乙醇或其任意組合溶液。然而,實施方式不限於此。
芯的包覆可以使用藥物領域中可用的任何膜包覆法進行,例如鍋包衣法、流化床包衣法或壓制包衣法。然而,實施方式不限於此。
當5-α-還原酶抑制劑(尤其是非那雄胺已知是致畸的)用作第二活性成分時,製藥公司需要單獨的獨立生產線以防止在製備含非那雄胺的製劑期間非那雄胺與其它醫藥產品混合。例如,在製備含有非那雄胺的固體製劑中,所有工藝,包括混合、制粒、壓片和包衣,必須在分離和專屬的區域中進行。然而,根據實施方式的複合製劑的製備方法包括將非那雄胺與含有非那雄胺的包衣溶液一起施用,使得可以僅通過附加引入含有非那雄胺的包衣的專用包衣設備來使用現有的藥物製備設備,並因此製備非那雄胺製劑可以相對方便。因此,當使用根據實施方式的複合製劑的製備方法時,含有5-α-還原酶抑制劑的複合製劑可以更經濟地製備。
實施例
現在將參考以下實施例詳細描述本發明的一個或多個實施方式。然而,這些實施例僅用於說明的目的,並且不旨在限制本發明的一個或多個實施方式的範圍。
實施例1-10:包括用含有5-α-還原酶抑制劑的膜包衣層包覆的坦索羅辛鹽酸鹽膠囊的複合製劑的製備(1)
通過將表1中所示的具有不同組成的包衣材料(實施例1-10)與乙醇-水混合溶液(乙醇:水=1:1(v/v))混合以製備包衣溶液,然後通過使用鍋包衣機(SFC-30,可從Sejong Co.,Ltd.獲得)包覆在含有坦索羅辛鹽酸鹽的膠囊(可從韓國的Hanmi Pharmaceutical Co.,Ltd.獲得)上。將製備的膠囊在約35℃下乾燥約30分鐘,從而製備包括用含有5-α-還原酶抑制劑的膜包衣層包覆的坦索羅辛膠囊芯的複合製劑。
比較例1至8:包括用含有5-α-還原酶抑制劑的膜包衣層包覆的坦索羅辛鹽酸鹽膠囊的複合製劑的製備(2)
以與實施例1至10相同的方式製備比較例1至8的包括用含有5-α-還原酶抑制劑的膜包衣層包覆的坦索羅辛膠囊芯的複合製劑,不同之處在於根據表1中所示的比較例1至8的組成製備包衣溶液。
[表1]
-IR(BASF)
-聚乙烯醇(KURARAY CO.LTD.)
-羥丙甲纖維素2910P603(SHIN ETSU CHEMICA CO.LTD.)
-聚維酮K-30(BASF)
實施例11和12:包括用含有5-α-還原酶抑制劑的膜包衣層包覆的坦索羅辛OD片劑芯的複合製劑的製備
通過將表2中所示的具有不同組成的包衣材料(實施例11和12)與乙醇-水混合溶液(乙醇:水=1:1(v/v))混合來製備包衣溶液,然後通過使用鍋包衣機(SFC-30,可由Sejong Co.,Ltd.獲得)在含有坦索羅辛鹽酸鹽的OD片劑(可從韓國的Hanmi Pharmaceutical Co.,Ltd.獲得)上包覆。將製備的複合片劑在約35℃下乾燥約30分鐘,從而製備包括用含有5-α-還原酶抑制劑的膜包衣層包覆的OD片劑芯的複合製劑。
[表2]
試驗例1:關於不同包衣材料的缺陷試驗
進行比較例1至8的複合製劑的缺陷試驗,以評價複合製劑的膜拉伸強度和缺陷率。
使用PTP包裝機(Lab-Blister machine,OMAR FANTASY PLUS)包裝每種複合製劑,其中用鋁膜密封包含每種複合製劑的鋁模具。隨機選擇10個普通人並要求打破100個PTP包裝,以便打開每個複合製劑的包裝,其中,如圖2中所示,複合製劑在其膜包衣層與其芯分離或破裂時被計為缺陷產品,或當膜包衣層與包裝前保持相同時作為可接受的產品,並且計算缺陷產品的百分比(以下稱為缺陷率)。計數為可接受產品(a)和缺陷產品(b)的複合製劑的實例的照片圖像示於圖2中。
將複合製劑的所得缺陷率示於表3和圖3中。
表3
考表3和圖3,僅使用IR、聚維酮或羥丙甲纖維素作為包衣材料的比較例1、3、4、5、7和8的複合製劑被發現具有約20%至約40%的高缺陷率的膜包衣層損傷,而僅使用聚乙烯醇作為包衣材料的比較例2和比較例6的複合製劑被發現具有約2%或更低的缺陷率。
試驗例2:包括聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的組合作為包衣材料的複合製劑的缺陷試驗
在與試驗例1中相同的條件下以相同的方式進行實施例1至10的複合製劑的缺陷試驗。將結果示於表4和圖4中。
[表4]
參考表3和4,與僅使用IR作為包衣材料的比較例1和5的複合製劑相比,使用IR與聚乙烯醇的組合作為包衣材料的實施例1-10的複合製劑被發現具有顯著降低的缺陷率。
特別地,與使用比例為約8:2的IR與聚乙烯醇的實施例1和6的複合製劑相比,使用比例為約7:3至約4:6的IR與聚乙烯醇的實施例2至5和實施例7至10的複合製劑被發現具有降低的缺陷率。
試驗例3:在應力條件下關於不同包衣材料的缺陷試驗
在約60℃和相對溼度(RH)為0%的恆溫室中保存1周後,以與試驗例1相同的方式進行比較例1至4的複合製劑的缺陷試驗,以評價每種複合製劑相對於儲存時間的穩定性。將試驗結果示於表5和圖5中。
[表5]
參考表5和圖5,單獨使用IR、聚維酮或羥丙甲纖維素作為包衣材料的比較例1、3和4的複合製劑都被發現具有約80%或更高的高缺陷率。然而,發現使用聚乙烯醇作為包衣材料的比較例2的複合製劑具有約17.4%的缺陷率,與比較例1、比較例3和比較例4的複合製劑相比顯示出改善的形狀和穩定性。
試驗例4:關於不同包衣材料的溶解試驗
如下進行溶解試驗以評價比較例1至4的複合製劑每個中的非那雄胺的溶出度。
使用根據韓國藥典(第10版)的一般試驗的溶出方法II(槳法)進行溶出試驗。根據韓國藥典(第10版),使用900mL蒸餾水(DW)作為試驗溶液,並且根據一般釋放製劑的操作方法以約50rpm的速度進行溶解試驗。在試驗開始後0分鐘、5分鐘、10分鐘、15分鐘、30分鐘、45分鐘和60分鐘取出測試溶液,並根據韓國藥典(第10版)的一般試驗通過液相色譜分析,由此通過與預先製備的標準溶液的比較獲得每個時間點的溶出度。將結果示於表6和圖6中。
[表6]
參考表6和圖6,與使用聚乙烯醇的比較例2的複合製劑相比,單獨使用IR、聚維酮或羥丙甲纖維素的比較例1、3和4的複合製劑被發現具有相對高的溶出度。
非那雄胺為需要高溶出度以實現高生物利用度的藥物。因此,與比較例1、3和4的複合製劑相比,使用聚乙烯醇的比較例2的複合製劑具有較低的生物利用度。
試驗例5:包括聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的組合作為包衣材料的複合製劑的溶解試驗
在與試驗例4相同的條件下進行實施例2至5的複合製劑的溶解試驗。將結果示於表7和圖7中。
[表7]
參考表7和圖7,發現使用重量比為約7:3至約4:6的IR和聚乙烯醇的實施例2至5的複合製劑在15min內具有約75%或更大的溶出度。
試驗例6:包括聚乙烯醇-聚乙二醇接枝共聚物與聚乙烯醇的組合作為包衣材料的複合製劑的關於芯型的缺陷試驗。
以與試驗例1相同的方式和相同的條件下進行實施例3、11和12的複合製劑的缺陷試驗。將結果示於表8和圖8中。
[表8]
作為缺陷試驗的結果,使用坦索羅辛片劑芯和與實施例3(使用坦索羅辛膠囊芯)的複合製劑相同的包衣材料的實施例11和12的複合製劑被發現具有改善的包衣形狀以及高溶出度和穩定性,也發現具有約1%或更低的低缺陷率。因此,發現根據任一實施方式的複合製劑的含有第二活性成分的膜包衣層適用於各種芯型,不僅適用於硬膠囊芯。
