一種普魯士藍/三氧化鎢複合光催化劑及其製備方法與應用與流程
2023-10-10 18:27:34 4
本發明屬於環境保護技術領域,涉及一種光催化劑的製備方法,具體涉及一種採用先簡單化學沉積而後溶劑熱製備PB/WO3複合光催化劑的方法。
背景技術:
隨著工業化進程的不斷加劇,水體汙染成為當今社會亟待解決的問題之一。異質光催化作為一種有效技術,可以利用太陽光輻照,在催化劑存在下,對有機物進行深度氧化,節約能源而且不汙染環境,因而具有很大的應用前景。
我國鎢資源蘊藏量豐富,居世界第一,因而WO3的來源相對廣泛。作為一種n型半導體,其帶隙能為2.4-2.8eV,能響應460-500 nm的可見光,是一種可見光響應型光催化劑。近年來在光化學、光催化劑、光致發光、氣敏性等應用領域引起了廣泛關注。大量對於WO3微納米結構的研究均表明該半導體在降解有機化合物方面展現了良好的光催化活性。但對於該單一體系,仍然存在下述幾個需要解決的問題:一是其吸收閾值僅約470 nm,對太陽能的利用率仍然較低;二是WO3的導帶位置約0.5~0.7V相對O2/O2-·的電勢(-0.046V)偏正,不利於氧氣的單電子還原,導致半導體中光生電子-空穴的複合速率很快,使光量子效率相對較低。這兩個問題的存在使WO3光催化活性的進一步提高受到限制。因此,拓寬WO3的可見光響應範圍,促進光生電子-空穴的有效分離與轉移,是目前該催化劑研究中需要解決的關鍵問題。
過氧化氫(H2O2)與二價鐵離子的混合溶液組成的芬頓試劑在氧化過程中產生強氧化劑 ·OH,可降解包括染料在內的多種有機物,因而被廣泛應用於有害有機物的處理。然而傳統芬頓技術只能在酸性條件下進行,當pH較高時Fe2+易生成沉澱,產生的鐵泥會造成二次汙染,增加處理成本,同時會抑制·OH生成,終止芬頓反應,限制其應用和推廣。因此,尋找有利於改善芬頓反應條件的鐵負載催化劑成為當前的研究熱點。普魯士藍的化學式組成為Fe4[Fe(CN)6]3,其組成中既有Fe2+又有Fe3+,其中,Fe3+/Fe2+的標準電極電勢為0.771V,比WO3導帶的電勢(0.5~0.7V)更正,因此Fe3+能夠捕獲WO3導帶上的電子,從而使WO3的光生電子和空穴得到有效分離;同時形成的Fe2+又能被加入的H2O2氧化成Fe3+ ,從而實現了離子之間的循環轉化,構成一個類芬頓反應。
基於上述思路,我們設計了WO3與普魯士複合光催化劑,並從節約能源、保護環境的角度出發,探索了一種操作簡單、成本低廉且高效的新型複合光催化劑,具有重要的理論和實際意義。
本發明本著簡化製備工藝、節約能源並提高性能的角度,通過簡單化學沉積而後溶劑熱的方法實現了PB和WO3半導體的複合,發現PB與WO3 的摩爾比在0.0005:1~0.1:1的範圍內光催化活性均明顯提高,其中摩爾比為0.03:1時的光催化活性最佳,其動力學常數為0.4546min-1,達到純WO3樣品的19.0倍。
技術實現要素:
為實現上述目的,本發明公開了一種普魯士藍PB/WO3複合光催化劑,其特徵在於它是由PB與WO3組成;其中PB與WO3 的摩爾比為0.001:1~0.05:1;所述複合光催化劑中PB指的是摩爾比為3:4的K4Fe(CN)6·3H2O和FeCl3反應得到的產物;WO3指的是三氧化鎢。其中最佳的PB與WO3 的摩爾比為0.03:1。
本發明進一步公開了普魯士藍PB/WO3複合光催化劑的製備方法,其特徵在於按如下步驟進行:
稱取一定量的Na2WO4·2H2O於25mL的聚四氟乙烯反應釜內襯中,加入5mL乙醇,磁力攪拌15min,將2mlNaCl溶液滴加於反應釜中,繼續磁力攪拌15min,然後將5mL 1.5×10-6~1.5×10-4mol/L的K4Fe(CN)6·3H2O和5ml 2.0×10-6~2.0×10-4mol/L的FeCl3水溶液緩慢滴入上述混合溶液中,攪拌10-15min加入3M HCl調溶液pH為0.5~2.0,繼續攪拌20~40 min後於60~200℃恆溫反應2~12h,待冷卻至室溫後,將沉澱離心分離、洗滌、60℃乾燥,收集所得粉末得到系列不同複合比例的 PB/WO3 複合光催化劑,所述的複合光催化劑中PB與WO3摩爾比在0.001:1~0.05:1。優選PB和WO3摩爾比在0.03:1。 本發明的製備方法中醇水體積比例為1:2.4,反應溫度為100-120℃。
本發明更進一步公開了普魯士藍PB/WO3複合光催化劑在降解有機染料方面的應用。其中的降解有機染料指的是降解印染和造紙車間排汙水中所含難降解性芳香類化合物方面的應用。該複合光催化劑在降解有機染料方面表現出良好的催化性能。所採用的製備方法為簡單化學沉積而後醇-水混合溶劑熱法,所得樣品具有優異的光催化性能,這些優勢預示著該光催化劑在工業廢水處理領域的良好應用前景。
附圖說明:
對所得部分光催化劑的結構、性能表徵結果如下:
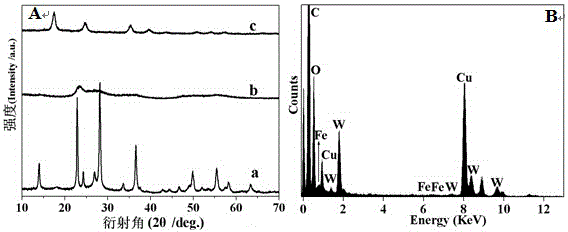
圖1為不同樣品的XRD、EDS圖譜;其中A為系列不同樣品的XRD圖譜:(a) WO3;(b) PB/WO3 -0.03;(c) PB;顯然相比於純WO3,複合光催化劑的衍射峰相當低,說明複合光催化劑的結晶度較差,不容易通過該表徵清楚地檢測WO3和PB的存在。因此進一步對樣品進行了電子能譜(EDX)的表徵,如圖1B所示,除了WO3中的W和O兩種元素外,從能譜圖中清楚檢測到了普魯士藍中Fe元素的存在,表明產物為普魯士藍與WO3形成的複合光催化劑;B為PB/WO3 -0.03複合光催化劑的EDS圖譜;
圖2為 WO3、PB及PB/WO3不同複合比例的紫外-可見漫反射光譜; WO3陡峭的吸收光譜形狀說明其來自本徵帶隙躍遷,雖然在可見光區也表現出一定的吸收,但由於其帶隙能約2.64eV,因此吸收帶邊僅約470 nm,對可見光區的吸收仍相對較少。而PB的吸收光譜範圍很寬,在200-800 nm的整個紫外-可見波段都有較強吸收。當將PB和WO3複合後,PB/WO3複合光催化劑的吸收帶邊明顯紅移。而且隨著PB複合比例的增加,材料在可見光區的吸收程度也有所增強。紫外-可見漫反射光譜表明PB的複合有效拓寬了WO3對可見光的吸收,從而能夠更加有效地利用太陽能;
圖3為在410nm紫外光激發下PB複合前後的WO3螢光光譜;螢光光譜常用來考察半導體中光生載流子的遷移和複合過程,螢光強度的減弱意味著載流子的複合機率降低。WO3在500-580 nm表現出較寬的黃綠色螢光發射帶,其中525 nm的最強螢光峰歸屬於激發電子從導帶的躍遷回價帶,從而引起光生電子-空穴複合而釋放出的能量。WO3經複合PB之後,螢光峰形與複合前基本一致,但螢光強度有所下降,尤其PB/WO3-0.03樣品的峰強度降低明顯,說明PB的複合可有效抑制電子-空穴的複合。但PB與WO3摩爾比過高(0.05:1)時,複合光催化劑的螢光強度反而又增強,這是由於過高的PB含量意味著在材料中引入了過多的相缺陷,而其又可成為光生載流子的複合中心。因此,在一定的複合比例內,PB的複合可有效抑制WO3中光生電子與空穴的結合機率,從而提高光量子效率。
圖4 為5 mg不同複合比例PB/WO3光催化劑在500W Xe燈輻照下,光催化降解10 ml 10-5 M的MO溶液的性能對比圖;其中(a)降解效率;(b)光催化反應速率常數;空白實驗表明MO在無光催化劑存在的情況下,經10min輻照後,僅有約1.2%的MO發生了降解,說明光照的影響可以忽略;WO3對染料分子的吸附很少,也不影響系列光催化劑的性能對比。在過氧化氫的協同下比較系列WO3基光催化劑的性能可以看出, 複合PB後WO3的光催化劑,活性均明顯提高,且表現出隨著PB元素複合比例的提高,催化降解效率先是大幅度提高,而後又稍有降低的趨勢,但均明顯優於未經複合的WO3。在純WO3存在下,光照10min後對MO的降解率為22.7%;PB/WO3-0.01的樣品在光照10min後對MO的降解率大幅增長至74.1%;而當PB/WO3摩爾比增大為0.03:1時,經過同樣的輻照時間,MO的吸光度幾乎降為零,表明染料已基本被降解完全。進一步增大PB與WO3的摩爾比為0.04:1時,同等時間內MO的降解率為83.3%。根據準一級反應動力學(圖4b),純WO3的降解反應速率常數為0.02386 min-1,而PB/WO3-0.03的速率常數為0.4546 min-1,是複合前樣品的19.0倍,顯示出最佳光催化活性。因此選定PB/WO3摩爾比為0.03:1為最佳複合比例。
具體實施方式:
為了進一步解釋本發明,提供下述製備方法實施實例。以下實施例的表述不限制本發明,本領域的專業人員可按照本發明的精神對其進行改進和變化,所述的這些改進和變化都應視為在本發明新型的範圍內。本發明所述的各種原料例如Na2WO4·2H2O、NaCl、HCl均有市售。
實施例1
稱取一定量的Na2WO4·2H2O於25ml的聚四氟乙烯反應釜內襯中,加入5mL乙醇,磁力攪拌10 min,將2ml NaCl溶液滴加於反應釜中,繼續磁力攪拌15min,然後將5ml 1.5×10-6mol/L的K4Fe(CN)6·3H2O和5ml 2.0×10-6mol/L的FeCl3溶液緩慢滴入上述混合溶液中,攪拌10min後,加入3MHCl調溶液的pH約為1,繼續攪拌20 min後於100℃恆溫反應4h,待冷卻至室溫後,將沉澱離心分離、洗滌、60℃乾燥,即可得到摩爾比為0.001:1的PB/WO3光催化劑。
實施例2
稱取一定量的Na2WO4·2H2O於25ml的聚四氟乙烯反應釜內襯中,加入5mL乙醇,磁力攪拌12min,將2mlNaCl溶液滴加於反應釜中,繼續磁力攪拌15min,然後將5ml 4.5×10-5 mol/L的K4Fe(CN)6·3H2O和5ml 6.0×10-5 mol/L的FeCl3溶液緩慢滴入上述混合溶液中,攪拌12min後,加入3MHCl調溶液的pH約為0.5,繼續攪拌30 min後於100℃恆溫反應4h,待冷卻至室溫後,將沉澱離心分離、洗滌、60℃乾燥,即可得到摩爾比為0.03:1的PB/WO3光催化劑。
實施例3
稱取一定量的Na2WO4·2H2O於25ml的聚四氟乙烯反應釜內襯中,加入5mL乙醇,磁力攪拌15min,將2mlNaCl溶液滴加於反應釜中,繼續磁力攪拌15min,然後將5ml 7.5×10-5 mol/L的K4Fe(CN)6·3H2O和5ml 1.0×10-4mol/L的FeCl3溶液緩慢滴入上述混合溶液中,攪拌15min後,加入3MHCl調溶液的pH約為1.5,繼續攪拌40 min後於100℃恆溫反應4h,待冷卻至室溫後,將沉澱離心分離、洗滌、60℃乾燥,即可得到摩爾比為0.05:1的PB/WO3光催化劑。
實施例4
印染車間所排汙水中含有的難降解性芳香類化合物的降解實例:
甲基橙是印染工業常用的難降解芳香類橙色染料,從印染車間取含有甲基橙染料3.27mg/L的廢水500mL,加入PB與WO3摩爾比為0.03:1的PB/WO3光催化劑250 mg,再滴入一定量的過氧化氫,在XPA-7型光化學反應儀暗箱中磁力攪拌達到吸-脫附平衡,經500W氙燈模擬日光輻照10 min後,立即過濾分離,測上清液吸光度計算MO的降解率為99.5%,而同等條件下純WO3的光催化降解效率僅為22.7%。
實施例3
選定性能最佳的PB/WO3 0.03:1樣品,對除甲基橙外的其它染料,包括橙黃和麗春紅也分別進行了相同條件下的光降解實驗,並和未經複合的WO3樣品進行了對比,所得數據列表如下:
從上表數據可以看出,PB/WO3-0.03不但對甲基橙的降解效率明顯高於未經複合的WO3,對染料橙黃和麗春紅的降解表現出同樣的優勢。說明該發明中的複合光催化劑在降解印染車間所排含難降解性芳香類化合物的汙水中確實具有良好的應用前景。
