快速減輕帕金森病中的運動波動的製作方法
2023-10-27 02:54:02 2
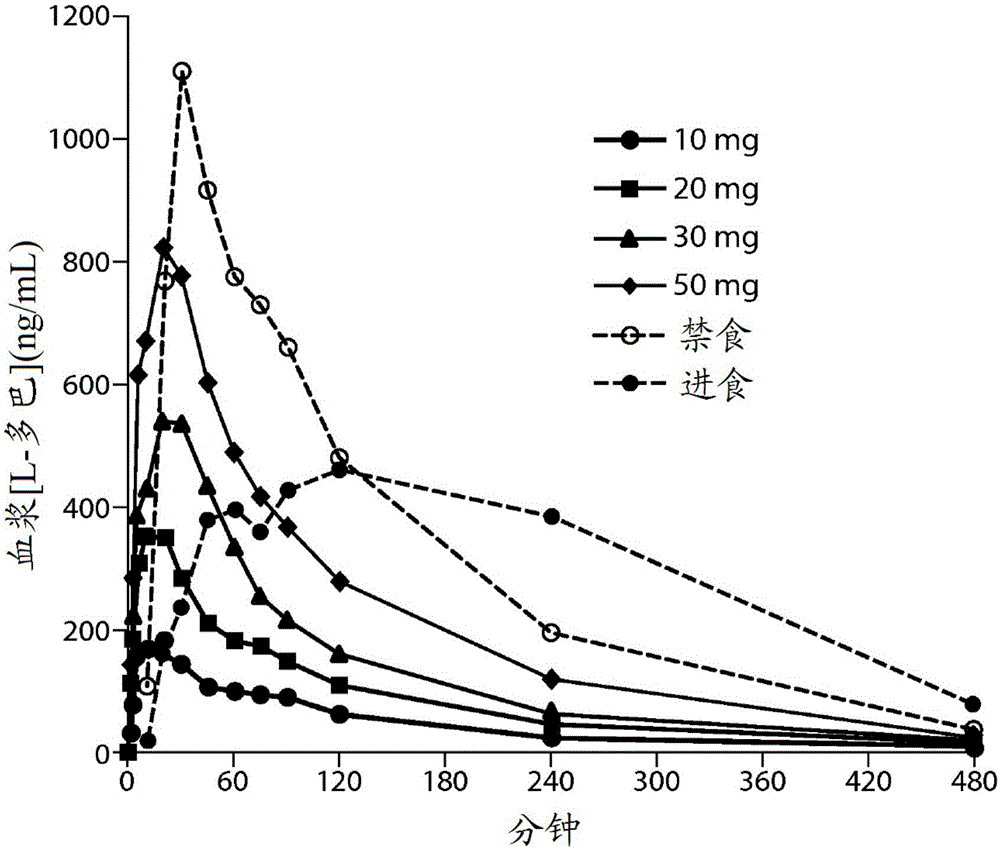
帕金森病(Parkinson’sdisease,在本文中也稱為「PD」)以神經病理學上基底神經節中多巴胺神經元的退化和神經學上虛弱性震顫、運動緩慢和平衡問題為特徵。據估計有超過一百萬人患有帕金森病。幾乎所有患者都接受多巴胺前體左旋多巴或「L-多巴」,其通常與多巴脫羧酶抑制劑卡比多巴結合。在疾病的早期階段,L-多巴足以控制帕金森病的症狀。但是,在一段時間以後,其傾向於不太有效,所述一段時間可以為疾病進程的數月到數年不等。L-多巴有效性降低的一個實例是進行治療的受試者中運動波動(motorfluctuations)的出現。「運動波動」意指受試者開始對多巴胺替代療法表現出可變的響應,使得在一些時間段內治療劑表現出良好效力並且充分控制帕金森病的症狀(在本文中也稱為「ON」時間/發作(episode)或「ON」),而在另一些時間段藥劑表現為幾乎沒有效果並且帕金森病的症狀惡化,其在本文中也稱為「OFF」時間/發作或「OFF」。運動波動可表現為效力「減退」,L-多巴的效力不再像開始觀察的那樣長,並且接著發生『on-off』症候群,其中患者經歷運動性的失能波動。逐漸地,經過一段時間,L-多巴的效力(on時間)可降低到多巴胺能治療的有用性嚴重受限的程度。認為帕金森病患者中L-多巴變化的效力至少部分地與L-多巴的血漿半衰期有關,即使在與卡比多巴共施用時,所述半衰期也傾向於非常短,在1至3小時的範圍。在疾病的早期階段,該因素被靶紋狀體神經元的多巴胺儲存能力減輕。L-多巴被所述神經元攝取和儲存並且隨時間釋放。但是,隨著疾病進展,多巴胺能神經元退化,導致多巴胺儲存能力降低。因此,L-多巴的積極效果變得與L-多巴的血漿水平的波動越來越相關。此外,患者傾向於出現涉及L-多巴的胃排空和差的腸攝取的問題。左旋多巴不穩定的胃排空造成運動性的隨機波動。患者表現出帕金森病症狀越來越顯著的擺動,從血漿水平降低時恢復到典型帕金森疾病症狀到L-多巴施用後血漿水平臨時升得過高時所謂的運動障礙。需要提供帕金森患者中運動波動和OFF發作的快速減輕,其中所述效果發生在臨床有意義的時期,並且其中所述效果允許患者充分的響應持續時間。發明概述本發明提供了用於治療帕金森病患者中的OFF發作的方法,包括向患者的肺部系統施用左旋多巴,其中在施用後,所述患者的帕金森病統一評定量表(UnifiedParkinson’sDiseaseRatingScale,UPDRS)第3部分(也稱為「UPDRS第III部分」或「UDPRSIII」)評分與安慰劑對照相比提高例如至少約5個點,和/或其中在施用後,所述患者的帕金森病統一評定量表(UPDRS)第3部分評分與施用前患者的UDPRS第3部分評分相比提高例如至少約5個點。在一個優選實施方案中,患者的UPDRS第3部分評分在例如施用左旋多巴的約60分鐘內提高。本發明還提供了減少平均每日OFF時間的方法和向患者遞送左旋多巴的方法。本發明特別可用於在帕金森患者中降低平均每日OFF時間和OFF發作的持續時間。附圖簡述圖1:90/8/2吸入和口服左旋多巴施用後的平均血漿左旋多巴濃度對時間數據。圖2:與口服施用相比90/8/2吸入後的平均血漿左旋多巴濃度對時間數據。圖3:吸入50mg90/8/2或者在進食和禁食條件下口服施用100mg左旋多巴(CD/LD25/100mg)後個體受試者中的血漿左旋多巴濃度。圖4:左旋多巴AUC0-∞對90/8/2細顆粒劑量。圖5:左旋多巴Cmax對90/8/2細顆粒劑量。圖6:平均血漿濃度的藥代動力學建模。符號表示觀察到的平均濃度,線表示通過模型預測的濃度。圖7:具有和不具有卡比多巴(CD)預治療的情況下的平均左旋多巴血漿濃度。圖8:患者血漿左旋多巴濃度與UPDRS評分相比。圖9:是示出了在作為主要終點的第6次訪問時接受50mg90/8/2細顆粒劑量的劑量水平2的研究藥物的患者和接受安慰劑的患者之間UPDRS第3部分評分對以分鐘為單位的時間的平均變化的線圖。圖10:是示出了在作為主要終點的第4次訪問時接受35mg90/8/2細顆粒劑量的劑量水平1的研究藥物的患者和接受安慰劑的患者之間UPDRS第3部分評分對以分鐘為單位的時間的平均變化的線圖。圖11:表明具有運動障礙的ON時間沒有惡化。圖11A示出了90/8/2與安慰劑相比無麻煩的運動障礙(non-troublesomedyskenisia)時間(小時)隨著時間(周)的變化。圖11B示出了90/8/2與安慰劑相比麻煩的運動障礙(troublesomedyskenisia)時間(小時)隨著時間段(周)的變化。發明詳述定義半衰期(T1/2)是體液或組織中的藥物濃度(C)達到濃度C/2的時間。「CmaxPul」意指在肺部遞送後測量的觀察到的最大血漿濃度(Cmax)。「Cmaxoral」意指口服遞送後測量的觀察到的最大血漿濃度。曲線下面積AUC對應於給定時間間隔的血漿濃度的積分。AUC以質量單位(mg,g)×升-1×小時表示,是藥物的生物利用度的量度。「AUCPul」意指在肺部遞送後測量的血漿濃度對時間曲線下的面積(AUC)。「AUCoral」意指在口服遞送後測量的血漿濃度對時間曲線下的面積(AUC)。術語「變差係數」(CV)以%CV表示,定義為標準偏差σ與平均值μ的比:Cv=σ/μ本文使用的語句「標稱劑量(nominaldose)」或「標稱粉末劑量(nominalpowderdose)」意指容器中包含的顆粒的總質量中存在的左旋多巴的百分比,表示可用來向患者施用的左旋多巴的最大量。「細顆粒分數(fineparticlefraction)」或「FPF」對應於容器中存在的顆粒質量中空氣動力學直徑小於5.6μm的顆粒的百分比。本文使用的術語「細顆粒劑量」定義為標稱劑量乘以FPF。如本文使用的,患者中「平均每日OFF時間的減少」是指在患者日誌中記錄的或通過臨床醫生觀察的患者每日OFF時間的平均減少。本文使用的帕金森病統一評定量表(UPDRS)是用於測量帕金森病的體徵和症狀的良好確定的工具。整個UPDRS由四部分組成。第1、2和3部分包括44道問題。除非另有說明,所有項目從零(正常)到四(嚴重受影響)評定,每個項目用簡短語句定義。UPDRS包括通過臨床醫生(運動檢查)以及心理功能和日常生活活動(通過詢問患者獲得的ADL)的歷史報告二者評分。第1部分測量心理狀態、行為和情緒,包括智力障礙、思維障礙、積極性/主動性和抑鬱症。第2部分測量日常生活活動(ADL),包括講話、唾液分泌、吞咽、書寫、切食物、穿衣服掉落、僵硬行走(freezingwalking)、震顫和感覺主訴(sensorycomplaints)。第3部分是運動檢查,測量包括講話、面部表情、靜止時的震顫、活動震顫、僵硬、手指輕拍(fingertaps)、手運動、手旋前和旋後、腿靈活度、從椅子中起立、擺姿勢、步態、姿態穩定性和身體運動徐緩(bodybradykinesia)。第4部分測量治療的併發症,包括運動障礙持續時間、殘疾疼痛(disabilitypain)、off時期和持續時間、睡眠障礙等。縮寫列表本發明的特徵和其他細節將在權利要求書中更具體描述和指出。應理解的是,本發明的具體實施方案僅以舉例說明的方式示出並且不限制本發明。本發明的原理特徵可以在多個實施方案中使用而不脫離本發明的範圍。如本文和所附權利要求書中使用的,單數形式「一」、「一個」和「所述」包括複數指示物,除非上下文明確指出相反情況。根據本發明,本文中使用的術語「左旋多巴的劑量」意指包含一定量的適於通過吸入向患者遞送的劑型的左旋多巴的製劑。在一個實施方案中,根據本發明的左旋多巴的劑量包括含左旋多巴的顆粒。用於向呼吸系統遞送左旋多巴的顆粒和方法描述在例如美國專利No:6,514,482和美國專利再公布No.RE43711中,兩者的內容通過引用整體併入本文。顆粒優選為乾粉形式,並且通過細顆粒分數(FPF)、幾何尺寸和空氣動力學尺寸及其他性質表徵,如下文進一步描述的。使用階式碰撞取樣器(Cascadeimpactor)的重量分析是測量空氣中顆粒的粒徑分布的方法。Andersen階式碰撞取樣器(AndersenCascadeImpactor,ACI)是8平臺碰撞取樣器,其可以基於空氣動力學粒徑將氣溶膠分離成9種不同級分。每個平臺的截留尺寸取決於操作ACI的流速。優選地ACI以60L/min校準。在一個實施方案中,二平臺縮減ACI(two-stagecollapsedACI)用於顆粒優化。二平臺縮減ACI由八平臺ACI的平臺0、2和F組成並且允許收集兩種分離的粉末級分。在每個平臺,氣溶膠流通過噴嘴並且撞擊在表面。氣溶膠流中具有足夠大慣性的顆粒將撞擊在板上。不具有足夠慣性來撞擊板的較小顆粒將保留在氣溶膠流中並且別攜帶到下一平臺。校準ACI以使得第一平臺上收集的級分被稱為細顆粒級分FPF(5.6)。該FPF對應於空氣動力學直徑小於5.6μm的顆粒的%。通過ACI的第一平臺並且沉積在收集濾器上的粉末級分被稱為FPF(3.4)。這對應於空氣動力學直徑小於3.4μm的顆粒的%。FPF(5.6)級分已被證明與沉積在患者肺中的粉末級分相關,而FPF(3.4)已被證明與到達患者深肺的顆粒級分相關。本發明至少50%顆粒的FPF小於約5.6μm。例如,但不限於,至少60%、或70%、或80%、或90%顆粒的FPF小於約5.6μm。測量空氣中顆粒(airborneparticle)的粒徑分布的另一種方法是多平臺液體碰撞取樣器(multi-stageliquidimpinger,MSLI)。多平臺液體碰撞取樣器(MSLI)以與Anderson階式碰撞取樣器(ACI)相同的原理操作,但不是八個平臺,MSLI中具有五個平臺。此外,並不是每個平臺由固體板構成,每個MSLI平臺由甲醇潤溼的玻璃熔塊構成。潤溼的平臺用於阻止彈跳和再夾帶,這些情況在使用ACI時可能發生。MSLI用於提供粉末流速依賴性的指示。這可以通過以30、60和90L/min操作MSLI並且測量收集在平臺1和收集濾器上的粉末級分來實現。如果不同流速下每個平臺上的級分保持相對恆定,則認為粉末接近不依賴流速。本發明顆粒的振實密度小於約0.4g/cm3。振實密度小於約0.4g/cm3的顆粒在本文中稱為「空氣動力學輕顆粒(aerodynamicallylightparticles)」。例如,顆粒的振實密度小於約0.3g/cm3、或振實密度小於約0.2g/cm3、振實密度小於約0.1g/cm3。可使用本領域技術人員已知的裝置測量振實密度,例如雙平臺微處理器控制的振實密度測試儀(Vankel,NC)或GEOPYCTM裝置(MicrometriesInstrumentCorp.,Norcross,GA30093)。振實密度是包絡質量密度(envelopemassdensity)的標準量度。可使用以下文獻中的方法測量振實密度:USPBulkDensityandTappedDensity,UnitedStatesPharmacopiaconvention,Rockville,MD,第10次增補版,4950-4951,1999。可有助於低振實密度的特徵包括不規則表面紋理和多孔結構。各向同性顆粒的包絡質量密度定義為顆粒的質量除以可以將其包圍在裡面的最小球體包絡體積。在本發明的一個實施方案中,顆粒的包絡質量密度小於約0.4g/cm3。本發明顆粒具有優選尺寸,例如,至少約1微米(μm)的體積中值幾何直徑(volumemediangeometricdiameter,VMGD)。在一個實施方案中,VMGD為約1μm至30μm,或由約1μm至30μm涵蓋的任何子範圍,例如,但不限於,約5μm至約30μm、或約10μm至30μm。例如,顆粒的VMGD為約1μm至10μm、或約3μm至7μm、或約5μm至15μm、或約9μm至約30μm。顆粒的中值直徑、質量中值直徑(massmediandiameter,MMD)、質量中值包絡直徑(massmedianenvelopediameter,MMED)或質量中值幾何直徑(massmediangeometricdiameter,MMGD)為至少1μm,例如,5μm或者接近或大於約10μm。例如,顆粒的MMGD大於約1μm並且至約30μm,或者約1μm至30μm涵蓋的任何子範圍,例如,但不限於,約5μm至30μm,或者約10μm至約30μm。噴霧乾燥顆粒的直徑(例如,VMGD)可以使用雷射衍射儀器(例如,Helos,由Sympatec,Princeton,NJ製造)測量。用於測量顆粒直徑的其他儀器是本領域中周知的。樣品中顆粒直徑的範圍取決於因素如顆粒組成和合成方法。可以選擇樣品中顆粒的粒徑分布以最佳地沉積在呼吸道內的靶部位。空氣動力學輕顆粒的「質量中值空氣動力學直徑」(MMAD)(在本文中也稱為「空氣動力學直徑」優選地為約1μm至約5μm,或者由約1μm至約5μm涵蓋的任何子範圍。例如,MMAD為約1μm至約3μm,或者MMAD為約3μm至約5μm。在實驗中,可以通過使用重力沉降法測定空氣動力學直徑,其中將全部顆粒沉降一定距離的時間用於直接推斷顆粒的空氣動力學直徑。用於測量質量中值空氣動力學直徑(MMAD)的一種間接方法是多平臺液體碰撞取樣器(MSLI)。可以由以下方程式估計空氣動力學直徑daer:daer=dg√ρtap其中dg是幾何直徑,例如MMGD,ρ是粉末密度。振實密度小於約0.4g/cm3,中值直徑為至少約1μm,例如至少約5μm,空氣動力學直徑為約1μm至約5μm,優選約1μm至約3μm的顆粒更加能夠逃脫口咽區的慣性和重力沉積,並靶向氣道,特別是深肺。使用較大、更多孔的顆粒是有利的,因為其比較小、緻密的氣溶膠顆粒(例如目前用於吸入療法的那些)更有效氣溶膠化。與較小、相對緻密的顆粒相比,較大的空氣動力學輕顆粒(優選中值直徑為至少約5μm)可潛在地更成功避免肺泡巨噬細胞的吞噬和從肺部清除,這是因為其尺寸將顆粒排除在吞噬細胞胞質空間之外。隨著顆粒直徑增大超過約3μm,肺泡巨噬細胞對顆粒的吞噬急劇降低。Kawaguchi,H.,等,Biomaterials,7:61-66(1986);Krenis,L.J.和Strauss,B.,Proc.Soc.Exp.Med.,107:748-750(1961);以及Rudt,S.和Muller,R.H.,JContr.Rel.,22:263-272(1992)。對於統計學上各向同性形狀的顆粒,例如具有粗糙表面的球體,顆粒包絡體積約等於巨噬細胞內用於完成顆粒吞噬所需的胞質空間的體積。可以製備具有合適的材料、表面粗糙度、直徑和振實密度的顆粒,以局部遞送至呼吸道的選擇區域,例如深肺或者上或中央氣道。例如,較高密度或較大顆粒可用於上氣道遞送,或者樣品中提供有相同或不同治療劑的不同尺寸顆粒的混合物可在一次施用中施用以靶向肺中的不同區域。對於中央和上氣道遞送,空氣動力學直徑為約3至約5μm的顆粒是優選的。對於深肺遞送,空氣動力學直徑為約1至約3μm的顆粒是優選的。在正常呼吸條件下,氣溶膠的慣性碰撞和重力沉積是氣道和肺腺泡中的主要沉積機制。Edwards,D.A.,J.AerosolSci.,26:293-317(1995)。兩種沉積機制的重要性與氣溶膠的質量成比例增加,而不是顆粒(或包絡)體積。由於氣溶膠在肺中的沉積部位由氣溶膠的質量決定(至少對於平均空氣動力學直徑大於約1μm的顆粒),通過增加顆粒表面不均勻性和顆粒多孔性降低振實密度允許將所有其他物理參數相等的較大顆粒包絡體積遞送到肺部。與實際包絡球體直徑相比,低振實密度顆粒具有小的空氣動力學直徑。空氣動力學直徑daer與包絡球體直徑d通過以下簡化公式相關(Gonda,I.,"Physico-chemicalprinciplesinaerosoldelivery,"於TopicsinPharmaceuticalSciences1991(編輯D.J.A.Crommelin和K.K.Midha)中,第95-117頁,Stuttgart:MedpharmScientificPublishers,1992)):daer=d√ρ其中包絡質量密度的單位是g/cm3。對於約daer=3μm的空氣動力學直徑,在人肺的肺泡區中發生單分散氣溶膠顆粒的最大沉積(~60%)。Heyder,J.等,J.AerosolSci.,17:811-825(1986)。由於其較小的包絡質量密度,包含將表現出最大深肺沉積的單分散吸入粉末的空氣動力學輕顆粒的實際直徑為:d=3/√ρμm(其中ρ_<1g/cm3);其中d始終大於3μm。例如,對於包絡直徑大至9.5μm的顆粒,包絡質量密度μ=0.1g/cm3的空氣動力學輕顆粒將表現出最大沉積。增加粒徑減小了顆粒之間的粘附力。Visser,J.,PowderTechnology,58:1-10。因此,除了有助於較低的吞噬損失以外,大粒徑提高了低包絡質量密度顆粒氣溶膠化至深肺的效率。可以計算空氣動力學直徑以提供在肺內的最大沉積。之前這通過使用直徑小於約5微米,優選約1至約3微米的極小顆粒來實現,其將被吞噬。選擇具有較大直徑但是足夠輕(因此特徵描述「空氣動力學輕」)的顆粒使得同樣遞送至肺,但是較大尺寸顆粒不被吞噬。相對於光滑表面,通過使用具有粗糙或不均勻表面的顆粒可以獲得改善的遞送。在本發明的另一個方面,顆粒的包絡質量密度(在本文中也稱為「質量密度」)小於約0.4g/cm3。在一些實施方案中,顆粒密度為約0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、小於0.1、0.02至0.05、0.02至0.06g/cm3。質量密度,以及質量密度、平均直徑和空氣動力學直徑之間的關係在2001年7月3日公布的Edwards等的美國專利No.6,254,854中有討論,其通過引用整體併入本文。可以通過多種方法產生具有上述組成和空氣動力學特性的顆粒,包括但不限於噴霧乾燥。通常,噴霧乾燥技術例如由K.Masters描述在"SprayDryingHandbook",JohnWiley&Sons,NewYork,1984中。本文使用的術語「有效量」或「治療有效量」意指實現期望效果或效力所需的量。藥物的實際有效量可根據所使用的具體藥物或其組合、配製的具體組成、施用方式,患者的年齡、體重、病症,以及被治療發作的嚴重程度而變化。在多巴胺前體、其激動劑或組合的情況下,其為降低需要治療的帕金森的症狀的量。用於特定患者的劑量在本文中有描述,並且可以由本領域技術人員使用常規考慮(例如,通過合適的常規藥理學方案)來決定。可以通過諸如本領域中已知的裝置向呼吸系統施用顆粒。例如,從吸入裝置如乾粉吸入器(DPI)遞送顆粒。也可使用計量劑量吸入器(Metered-dose-inhaler,MDI)、噴霧器或滴注技術。在一個實施方案中,通過以下文獻中所述的方法將顆粒遞送到肺部系統:題目為「HighEfficientDeliveryofaLargeTherapeuticMassAerosol」的美國專利6,858,199和題目為「HighlyEfficientDeliveryofaLargeTherapeuticMassAerosol」的美國專利7,556,798。這兩篇專利的整個內容均通過引用併入本文。如其中公開的,將顆粒容納、包含、儲存或封閉在容器(receptacle)中。容器,例如膠囊(capsule)或泡罩(blister)的體積為至少約0.37cm3,並且可具有適於在乾粉吸入器中使用的設計。也可以使用體積為至少約0.48cm3、0.67cm3或0.95cm3的較大容器。本文使用的術語「容器」包括但不限於例如膠囊、泡罩、膜覆蓋的容器孔(filmcoveredcontainerwell)、區室(chamber)以及本領域技術人員已知在吸入裝置中儲存顆粒、粉末或可呼吸組合物的其他合適的裝置。在一個實施方案中,容器是膠囊,例如標記有特定膠囊尺寸,例如2、1、0、00或000的膠囊。合適的膠囊可以從例如Shionogi(Rockville,MD)獲得。在一個實施方案中,膠囊殼可包含羥丙基甲基纖維素(HPMC)。在另一個實施方案中,膠囊殼可包含羥丙基甲基纖維素(HPMC)和二氧化鈦。泡罩可從例如HueckFoils,(Wall,NJ)獲得。其他適合於在本發明中使用的容器及其體積是本領域技術人員已知的。在一個實施方案中,本發明提供了以少量步驟,優選以單個呼吸活化步驟向肺部系統施用L-多巴。在一個實施方案中,在單個呼吸活化步驟中將儲存在吸入器容器中的顆粒質量的至少50%遞送到受試者的呼吸系統。在一個實施方案中,在單個呼吸活化步驟中將儲存在吸入器容器中的顆粒質量的至少60%,優選至少70%,優選至少80%遞送到受試者的呼吸系統。在另一個實施方案中,對於封閉在容器中的顆粒,通過單次呼吸施用將至少1至80毫克L-多巴遞送到受試者的呼吸道中。優選地,也可以遞送至少10、15、20、25、30、35、40、50、60、75和80毫克。通過使用以相對低的能量如通常由受試者的吸氣提供的能量分散的顆粒,增強了在單個呼吸驅動步驟中遞送到肺部系統的顆粒。這樣的能量在本文中稱為「低的」。如本文使用的,「低能量施用」是指這樣的施用,其中施加以分散和/或吸入顆粒的能量在吸氣期間受試者通常提供的範圍內。本發明還涉及向肺部系統有效遞送粉末顆粒的方法。例如,但不限於,實際遞送標稱粉末劑量的至少約60%、優選至少約70%或優選至少約80%。在一個實施方案中,本發明中使用的組合物包含適於肺部遞送的顆粒,例如乾粉顆粒,其包含按重量(乾重)計約60-99%的左旋多巴。特別優選的是包含按重量計約75%或更多左旋多巴的顆粒,甚至更優選包含按重量計約90%或更多左旋多巴的顆粒。顆粒可全部由L-多巴構成,或者還可包含一種或多種額外組分。這些合適的額外組分的實例包括但不限於磷脂、胺基酸、糖和鹽。磷脂的具體實例包括但不限於磷脂醯膽鹼二棕櫚醯磷脂醯膽鹼(DPPC)、二棕櫚醯磷脂醯乙醇胺(DPPE)、二硬脂醯磷脂醯膽鹼(DSPC)、二棕櫚醯磷脂醯甘油(DPPG)或其任意組合。本發明顆粒中磷脂如DPPC的量一般小於10wt%。鹽包括少量強電解質鹽,例如但不限於氯化鈉(NaCl)。其他可使用的鹽包括檸檬酸鈉、乳酸鈉、磷酸鈉、氟化鈉、硫酸鈉和碳酸鈣。通常,顆粒中存在的鹽的量小於10wt%,例如小於5wt%。在一個優選實施方案中,適於通過吸入向患者肺部遞送的左旋多巴的製劑包含按重量計90%的左旋多巴、按重量計8%的二棕櫚醯磷脂醯膽鹼(DPPC)和按重量計2%的氯化鈉,其在本文中也稱為「90/8/2」。在一個實施方案中,本發明提供了治療帕金森病患者中的OFF期的方法,包括向患者的肺部系統施用左旋多巴,其中在施用後,所述患者的帕金森病統一評定量表(UPDRS)第3部分評分與安慰劑對照相比提高例如至少約5個點。在一個實施方案中,患者UPDRSIII評分與安慰劑對照相比提高例如至少約8個點,優選至少約10個點,以及優選至少約12個點。在一個實施方案中,向患者施用約30至約60mg細顆粒劑量(fineparticledose,FPD)的左旋多巴,優選90/8/2FPD的左旋多巴。在一個優選實施方案中,向患者的肺部系統施用35mgFPD的左旋多巴。在另一個實施方案中,向患者施用50mgFPD的左旋多巴。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙(dyskinesis)水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,在出現OFF症狀時施用FPD的左旋多巴。在一個實施方案中,本發明提供了治療帕金森病患者中的OFF期的方法,包括向患者的肺部系統施用左旋多巴,其中在施用後,患者的帕金森病統一評定量表(UPDRS)第3部分評分與肺部施用前患者的UPDRSIII評分相比提高例如至少約5個點。在一個實施方案中,患者UPDRSIII評分與安慰劑對照相比提高例如至少約8個點,優選至少約10個點,以及優選至少約12個點。在一個實施方案中,向患者施用約30至約60mg細顆粒劑量(FPD)的左旋多巴,優選90/8/2FPD的左旋多巴。在一個優選實施方案中,向患者的肺部系統施用35mgFPD的左旋多巴。在另一個實施方案中,向患者施用50mgFPD的左旋多巴。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,在出現OFF症狀時施用FPD的左旋多巴。在一個實施方案中,本發明提供了用於減少帕金森病患者中平均每日OFF時間的方法,包括一天至少一次,優選一天至少兩次向患者的肺部系統施用左旋多巴,其中在施用後,患者的平均每日OFF時間減少至少約1小時,優選至少約2小時,優選至少約3小時,優選至少約4小時,優選至少約5小時或更多。在一個實施方案中,向患者施用約30至約60mg細顆粒劑量(FPD)的左旋多巴,優選90/8/2FPD的左旋多巴。在一個優選實施方案中,向患者的肺部系統施用35mgFPD的左旋多巴。在另一個實施方案中,向患者施用50mgFPD的左旋多巴。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,在出現OFF症狀時施用FPD的左旋多巴。在一個實施方案中,本發明提供了向帕金森病患者遞送左旋多巴的方法,包括向患者的肺部系統施用左旋多巴,其中在施用後,患者的帕金森病統一評定量表(UPDRS)第3部分評分與肺部施用所述左旋多巴之前患者的UPDRSIII評分相比提高至少約5至約12個點。在一個實施方案中,向患者施用約30至約60mg細顆粒劑量(FPD)的左旋多巴,優選90/8/2FPD的左旋多巴。在一個優選實施方案中,向患者的肺部系統施用35mgFPD的左旋多巴。在另一個實施方案中,向患者施用50mgFPD的左旋多巴。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,在出現OFF症狀時施用FPD的左旋多巴。在一個實施方案中,在肺部施用左旋多巴之後,患者的UPDRS第3部分評分與安慰劑對照相比提高至少約5至約15個點,優選至少約5至約12個點,優選至少約5至約10個點,優選至少約5至約8個點。在一個實施方案中,在肺部施用左旋多巴之後,患者的UPDRS第3部分評分與安慰劑對照相比提高至少約2至約15個點,優選至少約2至約12個點,優選至少約2至約10個點,優選至少約2至約8個點,優選至少約2至約5個點,優選至少約3至約15個點,優選至少約3至約12個點,優選至少約3至約10個點,優選至少約3至約8個點,優選至少約3至約5個點,優選至少約4至約15個點,優選至少約4至約12個點,優選至少約4至約10個點,以及優選至少約4至約8個點。在一個實施方案中,在肺部施用左旋多巴後約60分鐘內,優選施用後約30分鐘內,優選施用後約20分鐘內,以及優選施用後約10分鐘內,患者的UPDRS第3部分評分與安慰劑對照相比提高。在一個實施方案中,在施用左旋多巴後約60分鐘內,優選約30分鐘內,優選約20分鐘內,以及優選約10分鐘內,患者的UPDRS第3部分評分與安慰劑對照相比提高至少約2個點,優選至少約5個點,優選至少約8個點,優選至少約10個點,優選至少約12個點,以及優選至少約15個點。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,與肺部施用左旋多巴之前患者的UPDRS第3部分評分相比,施用後患者的UPDRS第3部分評分提高至少2個點,優選至少約3個點,優選至少約4個點,優選至少約5個點,優選至少約6個點,優選至少約7個點,優選至少約8個點,優選至少約9個點,優選至少約10個點,優選至少約11個點,優選至少約12個點,優選至少約13個點,優選至少約14個點,優選至少約15個點。在一個實施方案中,與肺部施用所述左旋多巴之前患者的UPDRSIII評分相比,患者的UPDRS第3部分評分在施用左旋多巴後約60分鐘內,優選約30分鐘內,優選約20分鐘內,以及優選約10分鐘內提高。在一個實施方案中,與肺部施用左旋多巴之前患者的UPDRSIII評分相比,患者的UPDRS第3部分評分在施用左旋多巴後約60分鐘內,優選約30分鐘內,優選約20分鐘內,以及優選約10分鐘內提高至少約2個點,優選至少約5個點,優選至少約8個點,優選至少約10個點,優選至少約12個點,以及優選至少約15個點。在一個實施方案中,與肺部施用左旋多巴之前的運動障礙水平相比,患者不經歷增加的運動障礙。在一個實施方案中,施用左旋多巴之前患者具有一天約3至約4次OFF發作。在一個實施方案中,施用左旋多巴之前患者具有一天約4至約8小時的OFF發作。在一個實施方案中,在出現OFF症狀時施用FPD的左旋多巴。在一個實施方案中,通過吸入向患者施用含有所述FPD的左旋多巴的至少一個膠囊的內容物。在一個實施方案中,通過吸入向患者施用含有所述FPD的左旋多巴,優選90/8/2FPD的左旋多巴的至少兩個膠囊的內容物。在一個實施方案中,通過吸入裝置將細顆粒劑量的左旋多巴從至少一個膠囊遞送至肺部系統。在一個是實施方案中,吸入裝置是乾粉吸入器(DPI)或計量劑量吸入器(MDI)。在一個實施方案中,本發明方法提供了快速減輕帕金森病患者中的運動波動。本發明方法特別適用於治療患者中因差的左旋多巴血漿水平控制導致的運動波動。在一個實施方案中,本發明方法包括通過以治療有效濃度吸入來肺部施用左旋多巴,使得與吸入左旋多巴之前患者血漿中的左旋多巴濃度相比,患者的血漿左旋多巴濃度在吸入後的約10分鐘或更短時間內升高至少約200ng/ml,並且其中患者血漿濃度在吸入後至少約15分鐘的時期保持升高至少約200ng/ml。在一個實施方案中,患者的血漿左旋多巴濃度在施用後至少約20分鐘的時期保持升高至少約200ng/ml。在一個實施方案中,患者的血漿左旋多巴濃度在施用後至少約30分鐘的時期保持所述升高至少約200ng/ml。在一個實施方案中,患者的血漿左旋多巴濃度在施用後至少約60分鐘的時期保持所述升高至少約200ng/ml。在另一些實施方案中,升高大於200ng/ml、200至500ng/ml、300至400ng/ml、或250至450ng/ml。在一個實施方案中,患者的血漿左旋多巴濃度在10分鐘內不會升高大於1000ng/ml。在一個實施方案中,本發明方法提供了快速減輕帕金森病患者中的運動波動,包括通過吸入向患者施用約20mg至約75mg左旋多巴,其中所述患者在所述吸入的10分鐘內運動波動得到立即減輕,並且其中所述患者保持所述減輕至少約30分鐘的時期。根據本發明的任何方法,與通過吸入施用左旋多巴之前患者的血漿左旋多巴濃度相比,在通過吸入施用一定劑量的左旋多巴後約10分鐘時,每4mg施用的左旋多巴使患者血漿中左旋多巴的曲線下面積(AUC)提高至少約1000ng-min/ml。在一個實施方案中,與通過吸入施用左旋多巴之前患者的血漿左旋多巴濃度相比,在通過吸入施用一定劑量的左旋多巴後約10分鐘時,每4mg施用的左旋多巴使血漿中所述左旋多巴的AUC提高至少約1000-1500ng-min/ml。根據本發明的任何方法,與通過吸入施用左旋多巴之前患者的血漿左旋多巴濃度相比,在通過吸入施用一定劑量的左旋多巴的約10分鐘內,每10mg遞送的左旋多巴使患者血漿左旋多巴濃度提高至少約175ng/ml,其中所述患者的血漿左旋多巴濃度在施用後至少約15分鐘、優選約20分鐘、優選約25分鐘、優選約30分鐘、優選約45分鐘、或優選約60分鐘的時期保持至少約175ng/ml的所述升高。在一個實施方案中,本發明提供了快速減輕帕金森病患者中的運動波動的方法,包括通過吸入向患者施用約20mg至約75mg左旋多巴,其中CmaxPul/AUCPul除以CmaxOral/AUCOral大於1,其中口服給予的左旋多巴的劑量與通過肺部遞送給予的劑量相對相同。在一個實施方案中,本發明提供了快速減輕帕金森病患者中的運動波動的方法,包括通過吸入施用一個或多個劑量的左旋多巴,其中T1/2/Tmax的比小於1/2,優選小於1/5。在一個實施方案中,本發明任何方法中使用的劑量包括向患者遞送約10mg至約75mg左旋多巴。在一個實施方案中,劑量包括約12mg至約35mg左旋多巴。在一個實施方案中,左旋多巴的劑量包括至少約10mg左旋多巴,優選至少約25mg左旋多巴,優選至少約35mg左旋多巴,優選至少約50mg左旋多巴,以及優選至少約75mg左旋多巴。在一個實施方案中,吸入一個或多個膠囊後,向肺部系統遞送的左旋多巴的量為約25至約60mg左旋多巴。在另一個實施方案中,吸入一個或多個膠囊後,向肺部系統遞送的左旋多巴的量為約35至55mg、約30至50mg、約40至50mg、約45至55mg。在一個實施方案中,本發明任何方法中使用的左旋多巴的劑量包含約30mg至約60mgFPD的左旋多巴。在一個實施方案中,本發明任何方法中使用的劑量為約35mgFPD的左旋多巴。在一個實施方案中,本發明任何方法中使用的劑量為約50mgFPD的左旋多巴。在一些實施方案中,吸入一個左旋多巴膠囊中的粉末後,發生快速的運動減輕或左旋多巴血漿增加。在一些實施方案中,在吸入2、3、4或5個膠囊的粉末後發生快速運動減輕或左旋多巴血漿增加。在一個實施方案中,本發明的任何方法中使用的劑量包含鹽。在一個實施方案中,劑量包含磷脂。在一個實施方案中,本發明的任何方法還包括向患者共施用多巴脫羧酶抑制劑。在一個實施方案中,在通過吸入施用左旋多巴之前、與通過吸入施用左旋多巴同時或在通過吸入施用左旋多巴之後,向患者施用多巴脫羧酶抑制劑。在一個實施方案中,本發明的任何方法還可包括向所述患者施用口服劑量的左旋多巴。在一個實施方案中,本發明的任何方法包括保持運動波動減輕至少2小時,優選至少3小時,優選至少4小時,優選至少5小時以及更優選至少6小時或更久。在一個實施方案中,根據本發明的任何方法治療的帕金森病患者是帕金森病2、3或4期患者。根據本發明的任何方法,左旋多巴的劑量不受中樞神經系統食物效果的影響。在一個優選實施方案中,本發明任何方法中使用的左旋多巴的劑量包含按重量計90%的左旋多巴,按重量計8%的二棕櫚醯磷脂醯膽鹼(DPPC)和按重量計2%的氯化鈉。在根據本發明通過吸入施用左旋多巴的時候,可以同時或順序地提供超過一種多巴胺前體、DOPA脫羧酶抑制劑或其組合的施用,包括但不限於L-多巴、卡比多巴、阿撲嗎啡和苄絲肼。在一個實施方案中,超過一種多巴胺前體或DOPA脫羧酶抑制劑的施用可通過肌肉內、皮下、口服等施用途徑來施用。在一些實施方案中,這些其他藥劑也通過肺部系統共施用。這些化合物或組合物可在通過吸入肺部施用左旋多巴之前、之後或同時施用,並且在與根據本發明所述方法通過吸入施用的左旋多巴相結合時,認為是「共施用」。在一個實施方案中,患者不需要共施用DOPA脫羧酶抑制劑或允許較低或較少頻率劑量的DOPA脫羧酶抑制劑。在另一個實施方案中,患者不需要共施用卡比多巴或者與口服接受L-多巴的患者相比允許較低或較少頻率劑量的卡比多巴。在另一個實施方案中,患者不需要共施用苄絲肼或者與口服接受L-多巴的患者相比允許較低或較少頻率劑量的苄絲肼。在一個實施方案中,在通過肺部途徑施用的左旋多巴和通過口服途徑施用的左旋多巴之間,卡比多巴依賴性之間的關係為:其中「w/oCD」意指不具有卡比多巴,「w/CD」意指具有卡比多吧,「INN」指肺部途徑,oral指向患者遞送卡比多巴的口服途徑。在一個實施方案中,需要精確的左旋多巴劑量以使患者為on。例如,在一個實施方案中,左旋多巴的劑量必須使患者的血漿左旋多巴濃度升高約200ng/ml至500ng/ml。有趣的是,左旋多巴濃度的這種小的升高適用於大範圍的患者給藥方案。可能需要1500-2000ng/ml血漿左旋多巴水平來為「on」的患者可通過血漿中200-500ng/ml的左旋多巴來成為on,而需要500-1000ng/ml血漿左旋多巴水平來為「on」的患者可通過血漿中200-500ng/ml的左旋多巴來成為on。更特別地,可通過使患者血漿濃度升高200-400ng/ml、250-450ng/ml、300-400ng/ml或約375-425ng/ml來使患者為on。可以通過多種方法使患者血漿濃度升高200-500ng/ml。可以口服、通過肺部途徑或胃腸外給予左旋多巴。如果通過肺部途徑給予,可以向患者的肺部系統提供25-50mg劑量的左旋多巴。在一個實施方案中,向患者肺部系統提供的劑量可以為25-35mg、27-32mg、28-32mg、29-31mg或約30mg。向患者肺部系統提供劑量可以通過多種方式進行。在一個實施方案中,膠囊包含35-40mg左旋多巴粉末,所述膠囊向患者的肺部系統提供膠囊中40-60%的粉末,並且所述粉末包含75-98%左旋多巴。以下實施例旨在舉例說明本發明,而不應解釋為限制其範圍。實施例1概要提供90/8/2乾粉左旋多巴製劑,以在成年健康志願者中評估與口服左旋多巴相比施用90/8/2肺部左旋多巴粉末後的安全性、耐受性和左旋多巴藥代動力學(PK)。這些實施例中所述的肺部左旋多巴粉末包含90%左旋多巴、8%二棕櫚醯磷脂醯膽鹼和2%氯化鈉(全部按乾重計)的顆粒,並且在本文中稱為90/8/2。該數據提供了對單吸入劑量的90/8/2之後左旋多巴的PK的描述,以及與禁食或進食條件下口服施用左旋多巴(LD)的比較,以及具有和不具有卡比多巴(CD)預治療的PK的比較。這是如下在健康成年男性和女性受試者中進行的二部分研究:部分A-與口服左旋多巴相比的劑量遞增階段;部分B-90/8/2加或減卡比多巴預治療階段。部分A是開放標記、3階段交叉、單遞增劑量研究。每位受試者在一個時期(session)在進食或禁食狀態下接受單口服劑量的CD/LD(25/100mg),在兩個不同的治療時期(treatmentsession)接受單遞增劑量的兩種不同劑量的吸入90/8/2(10和30mg或20和50mg左旋多巴細顆粒劑量(FPD))。登記兩組,每組9位受試者。部分B是開放標記、隨機化、二階段、階段平衡的交叉研究。在具有和不具有CD預治療的情況下,對8位受試者評估單吸入90/8/2劑量(40mg左旋多巴FPD)施用後的安全性、耐受性和左旋多巴PK。在24小時期間收集血樣並且使用經驗證的液相色譜-串聯質譜(LC-MS-MS)測定來確定血漿左旋多巴濃度,所述測定的定量下限為9.84ng/mL。使用非區室方法(non-compartmentalmethod)接著使用具有滯後時間的二區室模型的PK建模來進行藥代動力學分析。通過吸入以10至50mg左旋多巴FPD的劑量施用的90/8/2產生了快速升高的與劑量成比例的血漿左旋多巴濃度,在健康成年人中20至50mg的細顆粒劑量後5至10分鐘內實現了潛在的治療相關水平。90/8/2吸入後的左旋多巴血漿濃度比禁食狀態下口服施用後的那些升高的更快,比在進食狀態下那些快得多。藥物施用後最初10分鐘的暴露表示為0至10分鐘的血漿濃度對時間曲線下的部分面積AUC(AUC0-10m),給藥後最初10分鐘觀察的最大血漿濃度(Cmax,10m)顯示與口服施用相比90/8/2吸入後早得多的全身性暴露。與口服施用和對於肺部施用所預期的相比,吸入後受試者與受試者之間的血漿濃度變化性極大降低。分析還表明禁食狀態下的口服施用導致與進食狀態相比更快速的吸收,但是依然比吸入後慢得多。藥代動力學建模顯示了與90/8/2吸入後小於0.5分鐘的滯後時間相比,進食或禁食狀態下口服施用後約9至10分鐘的滯後時間。此外,與口服施用相比,吸入後的吸收半衰期更短。在90/8/2吸入後,全身性左旋多巴暴露與施用的90/8/2劑量成比例。施用的90/8/2劑量之間劑量歸一化的Cmax和AUC非常類似。與口服施用相比,吸入後劑量歸一化的(基於估計的細顆粒劑量)暴露基於AUC大1.3至1.6倍,基於Cmax大1.6至2.9倍。如文獻中已經描述的,在口服施用後,在進食受試者中觀察到了相當大的Cmax降低和Tmax延長;但是,進食和禁食受試者之間的AUC類似。在交叉設計中具有或不具有卡比多巴預治療的情況下,來自吸入40mg細顆粒劑量的90/8/2之研究的部分B的血漿濃度顯示快速吸收和達到潛在治療水平的血漿濃度。在沒有CD預治療的情況下,血漿左旋多巴清除快約四倍。相應地,在沒有CD預治療的情況下,Cmax和AUC更低並且Tmax和T1/2稍短。本研究的主要發現是:·吸入90/8/2導致血漿左旋多巴濃度快速升高;·與口服藥物施用相比,利用90/8/2吸入給藥後最初10分鐘基於Cmax和AUC的全身性左旋多巴暴露高得多;·在健康成人中,吸入20至50mg細顆粒劑量後的5至10分鐘內達到了潛在治療相關左旋多巴血漿濃度;·與口服施用和對於肺部施用所預期的相比,吸入後受試者與受試者之間血漿左旋多巴濃度的變化性相當低;·全身性左旋多巴暴露與施用的左旋多巴細顆粒劑量成比例;·藥代動力學建模表明與口服施用相比吸入的90/8/2具有更短的滯後時間和更快的吸收速率;·與口服施用相比,吸入後劑量歸一化的(基於估計的細顆粒劑量)暴露基於AUC大1.3至1.6倍,基於Cmax大1.6至2.9倍;·在沒有卡比多巴預治療的情況下,血漿左旋多巴清除率高約4倍,並且左旋多巴暴露降低。引言在本實施例中,將90/8/2作為患有帕金森病的患者中運動波動(「off發作」)的發作治療進行測試,所述患者對於其標準口服藥物具有間歇性不充分響應。90/8/2可用作患者現有包含多巴脫羧酶抑制劑(即,卡比多巴或苄絲肼)的帕金森病藥物方案的輔助。本研究是利用90/8/2在人中進行的首次研究,並且被設計來在成年健康志願者中評估與口服左旋多巴相比施用90/8/2後的安全性、耐受性和左旋多巴藥代動力學(PK)。已經在臨床試驗中測試了安全性和耐受性結果。本PK數據分析提供了對單吸入劑量的90/8/2之後左旋多巴PK的描述以及與禁食或進食條件下口服施用左旋多巴(LD;L-多巴)的比較,以及具有和不具有卡比多巴(CD)預治療的情況下左旋多巴PK的比較。如組合的卡比多巴/左旋多巴製劑中常規描述的那樣施用口服左旋多巴。研究設計和目的這是如下在健康成年男性和女性受試者中進行的二部分研究:·部分A:與口服左旋多巴相比的劑量遞增方案。·部分B:90/8/2±卡比多巴預治療方案本研究A部分的主要藥代動力學目的是在健康成年人中研究施用單吸入劑量的90/8/2後左旋多巴的藥代動力學。次要目的是探究單吸入劑量施用後左旋多巴的劑量成比例性(doseproportionality)並且將90/8/2的PK與禁食狀態或進食狀態施用的口服左旋多巴相比較。部分B的目的是比較具有和不具有卡比多巴預治療的情況下90/8/2的耐受性和藥代動力學。部分A是開放標記、3階段交叉、單遞增劑量研究。在研究藥物治療的前一天和當天,用口服卡比多巴治療所有受試者。每位受試者在一個時期在進食或禁食狀態下接受單口服劑量的CD/LD(25/100mg),在兩個不同時期接受單遞增劑量的兩種不同吸入劑量的90/8/2。登記兩組,每組9位受試者。部分A的研究設計概括在下表1中:表1:部分A研究設計。*用於90/8/2施用的左旋多巴劑量指示估計的顆粒劑量(FPD;即『肺遞送劑量』);口服CD/LD(25mg/100mg)。部分B是開放標記、隨機化、二階段、階段平衡的交叉研究。在部分A的安全性和PK數據的預審之後,在具有和不具有CD預治療的情況下,以隨機、平衡方式對8位受試者評估單吸入90/8/2劑量(40mg左旋多巴FPD)施用後的安全性、耐受性和左旋多巴PK,使得相等數目的受試者接受下文定義的兩種給藥順序A->B或B->A:方案A:90/8/2具有CD預治療方案B:90/8/2不具有CD預治療研究的部分A和部分B中的卡比多巴治療根據表2中的方案歸一化。在部分A中,在給藥前和口服CD/LD施用後10min、20min、30min、45min、60min、75min、90min、120min、4h、8h、16h和24h採集血樣。在部分A和部分B的90/8/2吸入治療時期期間,在相同時間採集樣品並且加上1、2和5分鐘的額外樣品。使用經驗證的液相色譜-串聯質譜(LC-MS-MS)測定通過SimbecResearchLimited確定血漿左旋多巴濃度,定量的下限為9.84ng/mL(2,3)。表2:卡比多巴治療方案。*當口服和吸入給藥時期按計劃在兩個連續日發生時,第一給藥時期執行的CD給藥方案充分包括了第二給藥時期所需的CD預治療。在接受研究藥物前一天期間,部分A和部分B(+CD)中的受試者接受3個劑量的CD。**不適用於隨機化進食狀態的受試者。***注意:25mg卡比多巴也在T0施用,作為口服CD/LD施用的一部分。藥代動力學分析方法非區室分析對每位受試者和每種治療的血漿濃度和時間進行數據分析,利用專業版本5.3進行非區室分析。使用線性梯形法(lineartrapezoidmethod)評估從時間零到最後可測量時間點的曲線下面積(AUC0-t)。最後三個或更多個時間點的線性回歸用於評估消除速率常數(λ),後者用於由以下方程式評估終末半衰期(T1/2)和從0到無窮的AUC(AUC0-∞):T1/2=ln(2)/λAUC0-∞=AUC0-t+Ct/λ其中Ct是通過回歸線預測的最後可測量濃度。由以下方程式評估血清清除率除以生物利用度(CL/F)和終末階段的表觀分布體積除以生物利用度(Vz/F):CL/F=劑量/AUC0-∞Vz/F=劑量/(λ*AUC0-∞)直接由數據確定最大濃度(Cmax)和觀察到它的最大時間(Tmax)。通過梯形法計算藥物施用後最初10分鐘的部分AUC(AUC0-10m)。確定最初10分鐘觀察到的最大血漿濃度(Cmax,10m),作為從給藥到包含10分鐘取樣時間所觀察到的最高血漿濃度。通過用90/8/2吸入後的劑量歸一化Cmax或AUC除以口服施用後的劑量歸一化參數來計算每個受試者的吸入與口服暴露比。基於AUC的暴露比是吸入藥物對口服藥物的相對生物利用度。利用包括由Cmax除以2計算的血漿濃度的兩個血漿濃度的時間點之間的線性插值計算(MicrosoftExcel)額外參數——達到觀察到的最大血漿濃度的一半的時間(TCmax50)。藥代動力學建模使用專業版本5.3進行藥代動力學建模。評估若干不同模型,包括具有和不具有滯後時間的一和二區室模型。所有評估模型具有一級輸入。基於若干診斷標準評估模型,包括Aikaike信息標準,殘差平方和,估計參數及其各自估計標準誤差的相對值,觀察濃度和預測濃度的相關性,以及預測濃度和觀察濃度之間變化的一般趨勢。最佳描述了大部分血漿濃度對時間曲線的模型是具有滯後時間的二區室模型(模型12)。還通過不具有滯後時間的模型描述了來自接受吸入90/8/2的受試者的大部分數據組,這是因為從這些受試者估計的滯後時間非常短,在大部分情況下小於1分鐘。但是,為了與來自口服施用的數據組進行比較,滯後時間模型用於所有受試者和所有治療。與一區室模型相比,二區室模型更好地描述了大部分數據組。在一些情況下,一區室模型可能不合適。在一區室模型更好的情況下,基於統計學診斷標準,兩個模型之間的差異非常小。因此,本文給出了使用二區室模型建模的結果。二區室模型方案1的模型產生以下的估計:分布體積除以吸收的劑量分數(V/F)、滯後時間(Tlag)和與吸收和消除有關的速率常數(分別為k01和k10),以及區室間速率常數k12和k21。由k12、k21和k10計算與曲線的吸收和消除階段有關的速率常數α和β。由一級參數計算的其他二級參數包括AUC、Cmax、Tmax、CL/F以及與曲線的吸收、分布和消除階段有關的半衰期(T1/2k01、T1/2α、T1/2β)。模型由以下方程式表示:Ct=Ae-αt+Be-βt+Ce-k01tCt是施用後時間t的血漿左多巴濃度,A、B和C是曲線的分布、消除和吸收階段的y軸截距並且由劑量、體積和速率常數計算。方案1在所有分析中使用均勻加權(Uniformweighting),並且報告為低於測定的定量水平(BLQ,<9.84ng/mL)的血漿濃度作為缺失值處理。分析中未排除數據點。結果和討論通過吸入以10至50mg左旋多巴FPD的劑量施用的90/8/2產生了快速升高的與劑量成比例的血漿左旋多巴濃度,在健康成年人中20至50mg左旋多巴的細顆粒劑量後5至10分鐘內實現了潛在的治療相關水平(400至500ng/mL)。圖1表示90/8/2吸入之後以及在進食和禁食條件下的100mg口服劑量之後的平均左旋多巴血漿左旋多巴濃度。對於分別為10mg、20mg、30mg和50mg左旋多巴的每個吸入劑量以及在進食和禁食條件下並且在具有和不具有卡比多巴預治療的情況下口服100mg左旋多巴,計算個別數值和濃度對時間曲線。90/8/2吸入後的血漿左旋多巴濃度比禁食條件下口服施用後的那些更快增加,比進食條件下的那些快得多。在90/8/2吸入後約5分鐘,達到了潛在的治療相關血漿濃度。在吸入20至50mgFPD的90/8/2後的5分鐘內,血漿濃度為400至500ng/mL或更高,觀察的潛在治療相關的範圍(4)。在40和50mgFPD的90/8/2之後達到的血漿濃度與在口服CD/LD(25/100mg)給藥後觀察到的那些在相同範圍(圖3).圖2示出了與口服施用後的那些相比最初10分鐘的平均血漿濃度。藥物施用後最初10分鐘的暴露表示為表3中0至10分鐘的AUC(AUC0-10m)和在最初10分鐘觀察到的最大血漿濃度(Cmax,10m)兩者。在一些個體中,在不到10分鐘觀察到Cmax,10m。禁食狀態下口服施用導致與進食狀態下相比更快速的吸收,但是依然比吸入之後慢得多。如文獻(5)中所述,在口服施用之後,在進食受試者中觀察到了相當大的Cmax降低和Tmax延長,但是,進食和禁食受試者之間AUC(表5)類似。表3:90/8/2吸入或口服左旋多巴施用後的左旋多巴暴露與口服施用之後相比,90/8/2吸入之後的治療後受試者間血漿濃度變化性低得多。參見圖3,在吸入之後(實心符號),大部分接受50mg90/8/2的受試者中的血漿濃度在給藥後10分鐘高於400ng/mL,一些在5分鐘且全部到20分鐘高於400ng/mL。在口服施用之後(空心符號),響應低得多,沒有受試者在給藥的10分鐘內接近400ng/mL。其他劑量組的個體血漿濃度和變化性數據表明,在20mg和以上的左旋多巴FPD劑量下,在一些受試者中在給藥的5至10分鐘之內達到高於400ng/mL的血漿濃度,並且響應變化性比口服施用之後低得多。表4中示出的給定取樣時間治療組內表示為%CV的血漿濃度變化性的程度證明,在給藥的最初30分鐘內,90/8/2治療受試者中的變化性低于禁食口服組中觀察值的一半,為全口服受試者(進食和禁食組合)中的約五分之一。表4:血漿左旋多巴濃度的變化性(%CV)*是指估計的左旋多巴細顆粒劑量**口服左旋多巴劑量100mg表5中示出了通過非區室分析評估的藥代動力學參數的概述。對於分別為10mg、20mg、30mg和50mg的每個吸入劑量以及在禁食和進食條件下並且具有和不具有CD預治療的情況下的100mg口服劑量,由非區室PK分析確定個體的參數估計。結果表明左旋多巴暴露與施用的90/8/2劑量成比例。對於所有90/8/2劑量,劑量歸一化Cmax和AUC非常類似。圖4和圖5中進一步說明了劑量成比例性。所有劑量的T1/2類似。表5:通過非區室分析評估的左旋多巴藥代動力學參數(平均值±SD)*劑量:左旋多巴劑量**是指估計的細顆粒劑量***中值由劑量歸一化AUC0-∞的比計算個體受試者的吸入90/8/2相對於口服左旋多巴的生物利用度。由於研究的部分A中的每位受試者接受一個口服劑量和兩個吸入劑量,所以確定每位受試者的兩個生物利用度估計值,每個吸入劑量一個。還在劑量歸一化Cmax值上進行相對暴露計算。對於在進食和禁食條件下施用的口服劑量,分開進行計算。表6中示出了用於相對生物利用度計算的平均值和標準偏差。計算個別值,作為由劑量歸一化Cmax計算的與卡比多巴/左旋多巴25/100mg)口服施用相比吸入90/8/2(10-50mg左旋多巴細顆粒劑量)之後的相對左旋多巴暴露。似乎沒有進食受試者和禁食受試者之間或劑量組之間的主要差異。與口服施用相比,吸入之後的劑量歸一化的(基於估計的細顆粒劑量)暴露基於AUC大約大1.3至1.6倍,基於Cmax大1.6至2.9倍。表6:吸入90/8/2相比於口服左旋多巴的暴露比(平均值±SD)通過具有一級輸入和滯後時間的二區室模型最佳描述了血漿濃度對時間曲線。在個體數據組上進行建模,並且使用模型12製作觀察的和預測的濃度對時間曲線。在一些情況下,終末半衰期(T1/2β)的估計值非常大,這是因為曲線最終階段中的一些點的濃度類似或波動,導致平緩坡度。在這些情況中的許多中,大的T1/2β產生了非常大的AUC估計值。來自模型的參數估計值中的其他變化性造成一些參數估計值中的一些異常值。這些值不從數據分析中排除或者在統計學上作為極端值處理。相反,通過中值而非平均值概況數據。因此,異常高或低的值保留在展示的數據中,但是不會不當地影響組的概況統計。表7中示出的藥代動力學建模結果表明,口服施用後有約9分鐘的滯後時間。相比之下,與吸入90/8/2相關的滯後時間可忽略,其小於0.5分鐘。另外,吸入90/8/2的吸收速率比禁食狀態下口服施用後的更快(更短T1/2k01),並且是進食狀態下吸收的快約10倍。與口服施用相比,90/8/2吸入後更短的滯後時間和更快的吸收速率解釋了給藥後最初5至10分鐘內觀察到的更大的全身性暴露。計算的參數—達到50%Cmax的時間(TCmax50)還表明,90/8/2吸入產生了比口服施用更早的左旋多巴全身性暴露。除了進食狀態的口服施用之外,吸收比消除快得多。圖6說明了滯後時間和吸收速率對施用後最初數分鐘內血漿濃度的聯合效應,其示出了平均血漿濃度數據的藥代動力學建模。該圖示出了給藥後最初60分鐘90/8/2吸入和口服左旋多巴施用的通過藥代動力學模型預測的濃度。符號表示觀察到的平均濃度,線表示通過藥代動力學模型預測的濃度。預測值和觀察值的良好相關性表明模型非常好地描述了數據。圖還說明了來自研究的其他觀察結果,90/8/2吸入導致血漿左旋多巴濃度快速升高,在給藥的5至10分鐘內可以達到潛在臨床相關血漿濃度,並且暴露與劑量成比例。表7:通過藥代動力學建模評估的藥代動力學參數(中值)*指估計的細顆粒劑量部分B圖7示出了來自研究的部分B的血漿濃度,其中在交叉設計中具有或不具有卡比多巴預治療的情況下吸入40mg左旋多巴FPD的90/8/2。利用卡比多巴預治療時峰值血漿濃度和暴露更高。血漿左旋多巴清除比沒有CD預治療時快約4倍。相應地,在沒有CD預治療的情況下,Cmax和AUC更低,Tmax和T1/2稍微更短(表8)。表8:在具有和不具有卡比多巴預治療的情況下吸入40mg90/8/2後通過非區室分析評估的左旋多巴藥代動力學參數(平均值±SD)*中值結論本研究的主要發現是:(i)吸入90/8/2導致血漿左旋多巴濃度快速升高;(ii)與口服藥物施用相比,利用90/8/2吸入給藥後最初10分鐘基於Cmax和AUC的全身性左旋多巴暴露高得多;(iii)在健康成人中,20至50mg左旋多巴細顆粒劑量的90/8/2給藥後的5至10分鐘內達到了潛在治療相關血漿左旋多巴濃度;(iv)與口服施用相比,吸入後受試者與受試者之間血漿左旋多巴濃度的變化性相當低;(v)全身性左旋多巴暴露與施用的左旋多巴細顆粒劑量成比例;(vi)藥代動力學建模表明與口服施用相比吸入的90/8/2具有更短的滯後時間和更快的吸收速率;vii)與口服施用相比,吸入後劑量歸一化的(基於估計的細顆粒劑量)暴露基於AUC大1.3至1.6倍,基於Cmax大1.6至2.9倍;以及viii)在沒有卡比多巴預治療的情況下,血漿左旋多巴清除率高約4倍,並且左旋多巴暴露降低。實施例2測試兩個劑量的肺部左旋多巴(25mg和50mg研究藥物)的階段2研究是多中心、隨機化、雙盲、安慰劑對照、單劑量、交叉設計,其具有三個臂(安慰劑、25mg和50mg)並且包括「開放標記」的口服Sinemet臂。對本研究中治療的24位PD(24)患者在每次訪問時的L-多巴血漿水平、運動響應(motorresponse)和安全性進行連續評估。在OFF狀態向患者施用研究藥物,連續評估在給藥前開始並且持續至給藥後180分鐘。使用敲擊測試、帕金森病統一評定量表第III部分(UPDRSIII)和主觀評價「有意義的」NO和OFF來測量運動功能。監測的安全性參數包括肺功能、臨床實驗室數據、EGC和生命體徵(血壓、心率和直立血壓(orthostaticbloodpressure))。本研究設計為測量肺部左旋多巴對運動功能的影響的時間、大小和持久性,以評估帕金森病患者中肺部左旋多巴的安全性和耐受性。在藥代動力學參數和藥效學參數的比較中,本發明人發現了處於off狀態的患者和處於on狀態的患者之間出人意料的陡曲線。在圖8中,將患者的血漿左旋多巴濃度與UPDRS評分進行了比較。UPDRS是用於帕金森病患者的標準測試,以測試其對於藥物治療的響應及其疾病進展。由圖8可以看到,處於on的患者和處於off的患者之間存在非常小的左旋多巴血漿濃度差異。低至200-400ng/ml的左旋多巴血漿濃度造成了off狀態和on狀態之間的差異。真正顯著的是四位不同患者在這裡所表現的,其全部具有顯著不同的基線左旋多巴血漿濃度。不同的基線左旋多巴血漿水平涉及每位患者具有不同的有效劑量或有效濃度以使得左旋多巴對於每位患者具有效果的事實。儘管患者群體之間具有不同有效劑量或有效濃度,從off到on所需的血漿濃度的升高非常小。實施例3階段2(b)隨機化、雙盲安慰劑對照的研究利用90/8/2的階段2b研究設計和方法本研究是用於經歷運動波動(OFF發作)的帕金森病(PD)受試者中每日多至3次OFF發作的治療的吸入(吸入的左旋多巴[LD]粉末)或安慰劑的隨機化、雙盲、安慰劑對照的多中心研究。將受試者以1:1比例隨機分配為接受吸入90/8/2(在本文中也稱為「研究藥物」)或安慰劑;通過受試者的Hoehn和Yahr階段(預測的60%的篩選FEV1和≥預測的75%的FEV1/FVC比,且沒有肺病史。評估標準和終點表9中描述了研究目的和變量。表9研究目的和變量縮寫:C-SSRS=Columbia自殺嚴重性評級量表;PD=帕金森病;PDQ-39=39-項目帕金森病問卷;PGI-C=患者變化的整體印象(PatientGlobalImpressionofChange);QUIP=帕金森病中衝動/強迫性障礙問卷;UPDRS=帕金森病統一評定量表。效力由診所和在家(門診)評估二者評估,如通過以下標準概況的:診所標準:UPDRS第3部分運動評分;在診所施用研究藥物後OFF發作消退至ON狀態的時間(每次檢查員評估);研究藥物施用後運動障礙的出現、持續時間和嚴重程度。在家標準:受試者報告的研究藥物施用後OFF發作消退至ON狀態的時間(來自吸入藥物治療記錄表),每日無運動障礙ON時間、具有運動障礙(麻煩的和無麻煩的)ON時間和OFF時間的PD日誌信息。進行以下探究性評估:PGI-C、PDQ-39、如上所述效力標準(評估90/8/2治療臂中2個劑量水平之間的潛在差異)。安全性由體檢、不良事件(AE)報告、標準和直立性生命體徵(血壓和心率)、呼吸率、臨床實驗室值(血液學、生物化學和)、心電圖(ECG)以及用於評估肺功能的呼吸量測定法。此外,用於評價自殺傾向、嗜睡和衝動控制行為的評估在基線和隨訪時進行。基線特徵八十六位患者(86)參與本研究。在訪問2之前的3個連續日中,患者完成篩選PD日誌,記錄其清醒ON/OFF狀態(時間OFF、沒有運動障礙的時間ON、具有無麻煩運動障礙的時間ON、具有麻煩運動障礙的時間ON)和睡眠時間。此外,患者將在訪問2之前的7天完成篩選ON/OFF發作和藥物記錄表,記錄清醒日經歷每次OFF發作的以下信息:OFF發作開始的時間、下一次ON開始的時間以及他們是如何使用他們的標準LD藥物。儘管患者約每三個小時進行其當前左旋多巴治療方案,這些患者報告OFF為其清醒時間的約1/3至1/2(參見表10和11)。表10全部(n=86)年齡(歲)62.4(8.7)自PD的時間Dx(年)9.4(3.9)LD的持續時間Tx(年)7.8(3.9)自波動出現的時間(年)4.3(3.6)每天平均OFF時間(小時)3.5(1.5)–自我5.7(1.8)-PDD*每天平均#OFF發作3.6(1.1)*~1h清晨OFF(總每日OFF時間的15-20%)表11因此,很明顯OFF時期的管理依然是PD患者中重要的未滿足的需求,如表12和13中指出的。表12提供了在接受研究藥物或安慰劑之前每位患者的平均給藥方案。表12表13提供了平均每日OFF和ON時間,如在接受研究藥物或安慰劑之前在日誌中由患者報告的。表13*PD日誌中至少2天的任何運動障礙≥1hr/天在階段2b研究的篩選階段和任一組接受研究藥物或安慰劑之前測量基線UPDRS第3部分評分。數據示於表14。表14暴露於研究藥物或安慰劑的記錄的總研究天數為約6.5患者年數(patientyears)(2,369患者天數)。經治療OFF期的總數等於施用的總劑量,為約4,484,安慰劑施用2314劑量,研究藥物施用2369劑量。用於整個研究的安慰劑或研究藥物的總膠囊為11,115。一位患者由於麻煩的運動障礙而經歷了劑量降低,但是該患者施用的是安慰劑。由於噁心,給予研究藥物中的一位患者劑量降低。基於患者自己的記錄,每天研究藥物的平均使用為每天使用2.1次,其排除早晨「OFF」時間。結果階段2b研究的主要終點是在訪問6(DL2)評估與給藥前相比UPDRS第3部分評分的平均變化(給藥後10-60分鐘)中研究藥物對安慰劑的差異。使用DL1的訪問4和訪問5(DL2的第一劑量)中的相同差異用作次級終點。與UPDRS一致,UPDRS運動評分的臨床重要差異(CID)是最小為2.5個點,中等為5.2個點,大CID為10.8個點(Shulman等,ArchNeurol,第67卷(2010年1月))。90/8/2滿足在50mg劑量訪問6時與安慰劑相比平均UPDRS第3部分運動評分(給藥後10-60分鐘的時期)的統計學上顯著降低的主要終點。在60分鐘時間點,87%的患者實現了UPDRSIII的臨床有意義的降低。此外,在訪問4、5和6評估兩種測試劑量(35mg和50mg)的所有時間點(即,10、20、30和60分鐘),90/8/2顯示出臨床相關的和統計學顯著的降低。在早至給藥後10分鐘,臨床相關UPDRSIII改善就已經明顯。在訪問6,用90/8/2(50mg劑量)治療之後,維持臨床顯著響應直至給藥後至少60分鐘。在每個給藥後時間點,90/8/2和安慰劑之間的差異是統計學顯著的。表15提供了初篩以及訪問4(V4)、訪問5(v5)和訪問6(v6)時研究藥物組和安慰劑組之間給藥前UPDRS評分的比較。在訪問4時遞送劑量水平1(DL1),而在訪問5和訪問6時遞送劑量水平2(DL2)。表15如圖9和10中所示,在每個時間點,以50mgFPD施用的研究藥物(圖9)和以35mg施用的研究藥物(圖10)之間具有統計學差異。表16提供了訪問4-6各自的平均最佳UPDRS第3部分變化。平均值(SEM)*所有訪問統計學顯著差異表17示出了訪問4-6各自的平均最佳百分比(%)UPDRS第3部分變化。平均值(SEM)*所有訪問統計學顯著差異總結根據本文提供的數據,階段2b研究達到了其主要終點,表現為與安慰劑相比在訪問6的給藥後10至60分鐘平均UPDRS第3部分評分與給藥前相比具有統計學顯著的平均變化。數據還表明UPDRS時間曲線的形狀指示快速和持久的響應,35mg劑量(DL1)具有與50mg劑量(DL2)類似的振幅,但是效果的持續潛在地稍微更短。所有訪問和劑量中UDPRS第3部分評分的最佳變化和最佳百分比變化也是統計學顯著的,甚至在安慰劑響應衰減之前的V4(DL1),具有顯著分離。數據一起表現出每日OFF時間的強烈的臨床有意義和統計學顯著的改善,而不增加具有運動障礙的ON時間,如圖11所示。圖11示出了報告與安慰劑組相比在研究藥物組中測試的患者的麻煩的和無麻煩的運動障礙的數據(如在其各自PD日誌中自我報告的)。實施例1和2以及本實施例的研究還表明,在所有階段1、2a和2b研究測試的所有劑量水平,藥物是安全的並且良好耐受。本文引用的所有專利和科技文獻建立了本領域技術人員可獲得的知識。本文引用的所有美國專利和公開的或未公開的美國專利申請通過引用併入本文。本文引用的所有公開的外國專利和專利申請通過引用併入本文。所有其他公開的文獻、文檔、手稿和科技文獻通過引用併入本文。儘管參考本發明的優選實施方案特別示出和描述了本發明,本領域技術人員將理解的是,可以在其中進行各種形式和細節的變化,而不脫離由所附權利要求包括的本發明的範圍。還應該理解,根據本發明,本文描述的實施方案不互相排斥,並且來自多個實施方案的特徵可全部或部分組合。當前第1頁1 2 3 
