多孔碳納米棒在近紅外光誘導雙重光療中的應用的製作方法
2023-12-01 13:30:41 1
本發明屬於先進納米材料及生物、醫學治療領域,具體涉及多孔碳納米棒在近紅外光誘導雙重光療中的應用。
背景技術:
近紅外光治療技術(光動力學治療、光熱療)利用近紅外激發等作為光源照射光轉換劑產生大量的活性氧(ROS)以及熱量,達到以高濃度的活性氧和高溫殺死癌症細胞的目的。近紅外光治療技術具有穿透深度大、選擇性高、損傷小等優點,是近年來發展起來的一種備受關注的微創治療腫瘤新技術。
研究發現,將光動力學治療與光熱療結合即雙重光療可以產生良好的協同效應,獲得「1+1>2」的腫瘤治療效果。目前,研究比較多的雙重光療納米治療劑主要分為兩類:第一類是利用光熱轉換納米材料如金納米棒、石墨烯、二硫化鉬納米片等負載有機光敏劑(Nano Research 2014,7,1291–1301;ACS Nano 2011,5,7000-7009;Nanoscale 2014,6,11219-11225);其缺陷在於有機光敏劑抗光漂能力差,長時間易光降解且活性氧產生效率低,有機光敏劑與光熱轉換納米材料的波長吸收不一致,需要不同波長的雷射交替照射。第二類是無需負載有機光敏劑,單一激發光源照射可同時實現活性氧與熱量的高效轉化的納米材料,如海膽狀金納米粒子,硫化銅納米晶(Adv.Mater.2014,26,6689–6695;ACS Nano 2015,9,1788-1800)等;該類型的雙重光療納米治療劑相比第一類提高了雷射能量利用率,簡化了操作步驟。因此,設計合成新型的類似第二類的多功能光敏材料實現單一激發光源下,光動力學治療、光熱療同步高效協同治療,對臨床腫瘤的高效微創治療具有重要意義。
本發明利用多孔碳納米棒為基體吸收近紅外光,轉化產生高能熱量和高濃度的活性氧,使其同時作為光熱治療劑和光動力學治療劑用於殺死腫瘤細胞。該多孔碳納米棒具有製作成本低廉,生物相容性好,光熱轉化率高,活性氧產率高的特點,有利於提高雷射能量利用率,增強對癌細胞的殺傷效率。
技術實現要素:
本發明的目的在於提供多孔碳納米棒在近紅外光誘導雙重光療中的應用。該納米材料可作為納米協同治療劑通過近紅外光誘導產生光熱療與光動力雙機制殺死腫瘤細胞,增強對癌細胞的殺傷效率,為更有效的納米療法找到了新的方向。
本發明的技術方案是:以金屬有機骨架材料為模板經高溫碳化並酸性溶解去除金屬氧化物後得到多孔碳納米棒,該多孔碳納米棒具有近紅外光誘導產生光熱療與光動力雙機制殺死腫瘤細胞的作用。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,所述的多 孔碳納米棒以金屬有機骨架材料為模板經高溫碳化並酸性溶解去除金屬氧化物後得到。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,所述的金屬有機骨架材料碳化條件為保護氣氛下高溫煅燒;其中,煅燒溫度為600-1200℃;煅燒時間為3-12h;保護氣氛為氮氣、氦氣、氖氣、氬氣、氪氣或氙氣中的一種或幾種。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,所述的去除碳化產物中殘餘金屬成分所需的酸性環境為1-20wt%鹽酸、硝酸、硫酸或氫氟酸中的一種或二種以上。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,多孔碳納米棒吸收近紅外光轉化產生高能熱量和高濃度活性氧的測定是將多孔碳納米棒分散於水相介質後測得的。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,所述的多孔碳納米棒吸收近紅外光殺死腫瘤細胞的應用環境為腫瘤細胞攝取多孔碳納米棒後施加近紅外光照射,高能熱量和高濃度活性氧引發腫瘤細胞死亡;條件為近紅外光需要持續照射腫瘤細胞5-30min。
本發明提供的多孔碳納米棒在近紅外光誘導雙重光療中的應用,近紅外光近紅外光波長範圍為700-1100nm。
多孔碳納米棒用於近紅外光誘導雙重光療,有以下優點:
(1)多孔碳納米棒具有形貌單一,尺寸可調,高比表面積,高孔容的特性;其製備工藝簡單,產率高,成本低廉,生物相容性好。
(2)克服有機光敏劑抗光漂能力差,長時間易光降解且活性氧產生效率低的弱點;避免使用不同波長的雷射交替照射,簡化了操作步驟。
(3)光熱轉化率高、活性氧產率高,擴展了雙重光療納米治療劑的種類,對實現臨床腫瘤的高效微創協同治療具有重要意義。
附圖說明
圖1是實施例1中多孔碳納米棒的TEM圖;從圖中可看出,多孔碳納米棒尺寸較小且具有發達的孔結構。
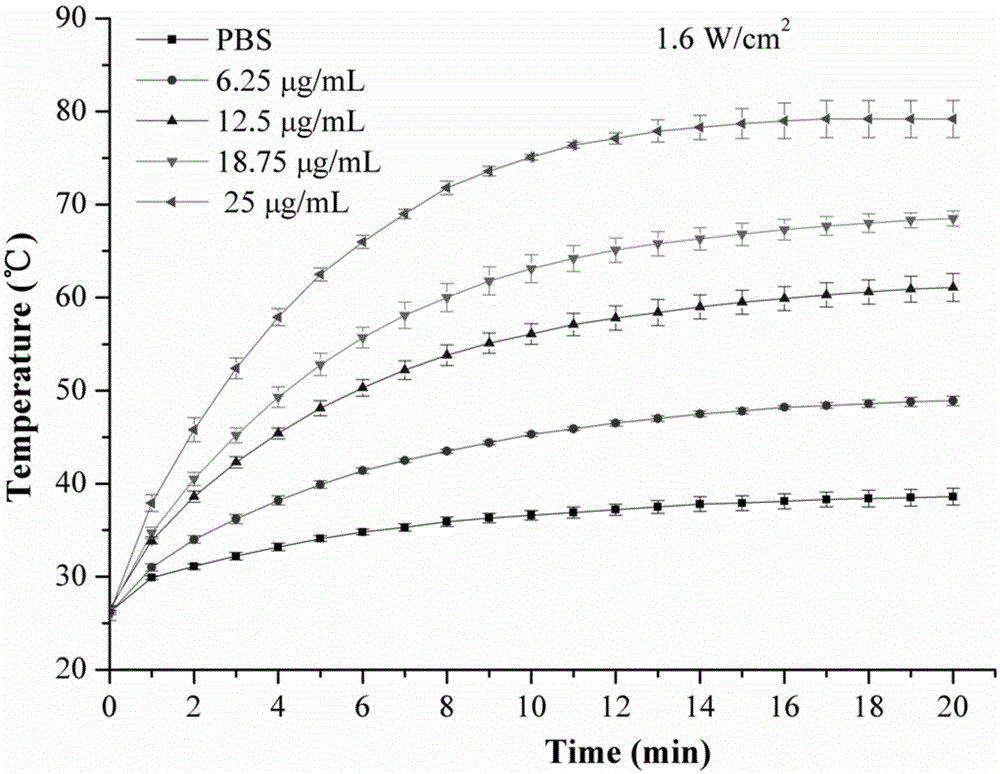
圖2是實施例1不同濃度的多孔碳納米棒溶液在808nm雷射照射下的溫度變化曲線(1.6W/cm2,20min);從圖中可看出,樣品的升溫效果隨樣品濃度的變化而變化,樣品濃度高,升溫效果好,當樣品濃度達到25μg/mL時,在1.6W/cm2,808nm雷射的照射下,10分鐘內,溫度可上升約50℃;然而50μg/mL的空心碳球在在2.4W/cm2,808nm雷射的照射下,10分鐘內,溫度僅上升約8℃(J.Am.Chem.Soc.2015,137,1947-1955)。
圖3是實施例1不同濃度的多孔碳納米棒溶液在808nm雷射照射下的活性氧含量變化曲線(1.6W/cm2,20min);曲線至上而下分別為25μm/mL,18.75μm/mL,12.5μm/mL,6.25μm/mL,PBS,從圖中可看出,樣品在808nm雷射誘導下活性氧產生含量隨樣品濃度的變化而變化,樣品濃度越高,活性氧產量越 高,同樣處理條件下的單純的分散介質無法產生活性氧。
具體實施方式
本發明通過採用多孔碳納米棒作為近紅外雷射響應材料,可以吸收雷射能量轉化產生熱量及活性氧,即發揮光熱與光動力的雙重治療作用,增強對癌細胞的殺傷效率。
下面的實施例將對本發明予以進一步的說明,但並不因此而限制本發明。
實施例1
將摩爾比為1:1的均苯三甲酸與醋酸鋅分別溶解後,混合超聲反應,離心、洗滌、乾燥製得鋅金屬有機骨架材料;氮氣氛下800℃煅燒5h並使用氫氟酸浸泡12h除去金屬氧化物,得到多孔碳納米棒。多孔碳納米棒超聲分散於PBS,配製梯度濃度的材料溶液。將多孔碳納米棒溶液置於808nm雷射下照射,光功率密度為1.6W/cm2,照射時間為20min,間隔1min,記錄材料溶液溫度的變化;加入ROS指示劑DCFH-DA,檢測溶液內ROS含量的變化。
實施例2、
將摩爾比為1:1的均苯三甲酸與硝酸鋅分別溶解後,混合加入三乙胺室溫反應,離心、洗滌、乾燥製得鋅金屬有機骨架材料;氮氣氛下800℃煅燒5h並使用氫氟酸浸泡12h除去金屬氧化物,得到多孔碳納米棒。多孔碳納米棒超聲分散於PBS,配製梯度濃度的材料溶液。將多孔碳納米棒溶液置於808nm雷射下照射,光功率密度為1.6W/cm2,照射時間為20min,間隔1min,記錄材料溶液溫度的變化;加入ROS指示劑DCFH-DA,檢測溶液內ROS含量的變化。
實施例3、
將摩爾比為1:2的均苯三甲酸和醋酸鋅分別溶解後,混合超聲反應,離心、洗滌、乾燥製得金屬有機骨架材料;氮氣氛下800℃煅燒5h並使用氫氟酸浸泡12h除去金屬氧化物,得到多孔碳納米棒。多孔碳納米棒超聲分散於PBS,配製梯度濃度的材料溶液。將多孔碳納米棒溶液置於808nm雷射下照射,光功率密度為0.8W/cm2,照射時間為20min,間隔1min,記錄材料溶液溫度的變化;加入ROS指示劑DCFH-DA,檢測溶液內ROS含量變化。
