確定血液或血漿中的抗凝劑的測定的製作方法
2023-12-05 02:12:11 1
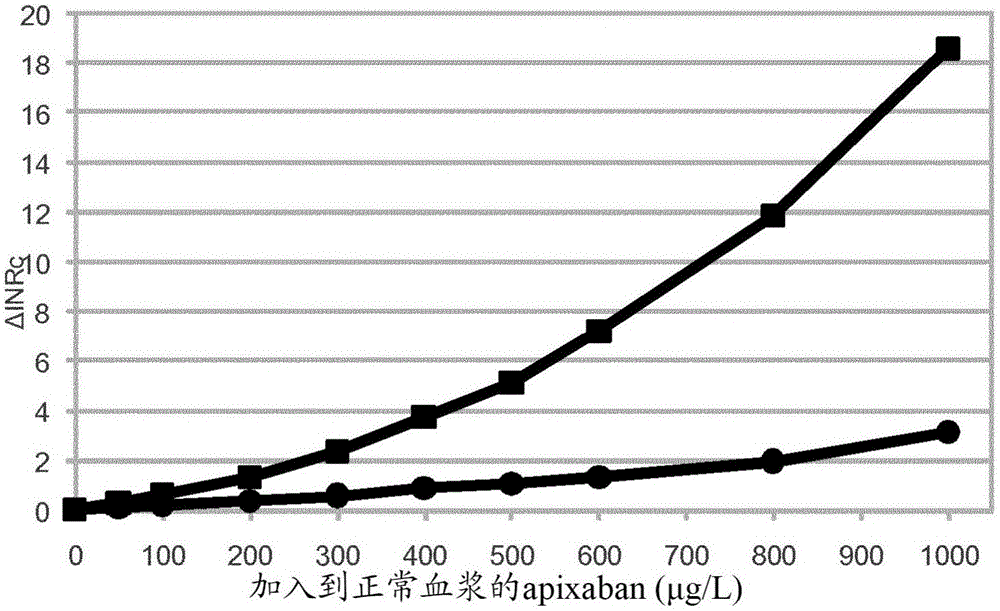
本公開內容涉及確定血液或血漿樣品中的抗凝劑的測定。背景抗凝劑是抑制、減少或消除血液或血漿凝結的能力的物質–抗凝劑減少纖維蛋白原被轉化為纖維蛋白的速率。一些抗凝劑是天然存在的、內源的,並在限制體內血液凝結的發作、蔓延速度和空間擴展中起到重要的生理作用。其他抗凝劑在病理條件下出現。在蛇毒素和在蚊子、水蛭、蝙蝠和壁蝨的分泌物中發現了抗凝劑。一個越來越多的抗凝劑的組是為了治療和預防血栓栓塞紊亂的目的產生的人造物質。血液凝結是複雜的現象,包括在血漿中或在參與的細胞表面上發現的許多相互作用的分子。存在許多細胞和分子相互作用,包括可被抗凝劑的作用下調或破壞的許多酶催化反應。直接作用的抗凝劑抑制、妨礙或消除凝血過程中關鍵酶(凝血酶(FIIa)或活化的凝血因子X(FXa))的一種或二者的酶促作用。間接作用的抗凝劑以一些其他方式起作用,其中之一是增強直接作用抑制劑的功效。在一般治療使用的抗凝劑之中,肝素是間接作用抗凝劑且維生素-K拮抗劑(華法林(warfarin))是凝血因子水平的一般減少者。直接作用抗凝劑是水蛭素(水蛭的一種蛋白)和最近產生的FIIa或FXa的抑制劑。這些新的直接作用抗凝劑,特別是可口服施用的那些,DOAC或還稱為NOAC(非維生素K口服抗凝劑),正在導致臨床和實驗室醫學中的顯著變化。抗凝劑具有不同作用模式的事實對實驗室醫學在設計可確定抗凝劑的方法方面構成挑戰。在一定程度上,這一挑戰被在產生治療血栓栓塞紊亂的新物質方面的最近藥理學成功加劇,參見例如J.Harenburg,S.Marx和R.Determinationoftheanticoagulationeffectsoftheneworalanticoagulants:anunmetneed,ExpertReviewofHaematology,February2012,Vol.5,No.1,Pages107-113。在有許多可用的檢測和合格的人員來解釋結果的中心醫院實驗室,檢測和確定DOAC表現為相對直接-FIIa抑制劑和FXa抑制劑可分別通過凝血酶時間(TT)檢驗或FXa檢驗來測定。如果這些檢驗的標準變化形式不滿足要求,標準變化形式的一些修改或「稀釋」將滿足要求。在初級護理中心和在醫院內但遠離中心實驗室的位置、場所,「場所外(off-site)」,情況是不同的。在POC場所(床邊護理(PointofCare))的實驗室醫學的特徵是,不同的實驗室檢驗的數目是有限的,因為此類實驗室場所的物理空間是有限的且因為合格的實驗室人員的可用性是有限的。在凝血中,最可用的POC檢驗是凝血酶原檢驗(PT-檢驗),結果以INR(國際歸一化比率,即,樣品的PT與通過對歸一化指數(一種靈敏度指數)加權而歸一化的常態PT之間的比率)表示。其他「例行」或「常見」凝血檢驗是活化的部分促凝血酶原激酶時間(APTT)、活化的凝血時間(ACT)和所提到的TT。凝血領域中理想主義專家希望,這些「例行」或「常見」凝血檢驗可被調整、修改、「稀釋」,以滿足測定「新」抗凝劑特別是NOAC中的POC需求。此類想法/希望例如由E.J.Favaloro和G.Lippi,Theneworalanticoagulantsandthefutureofhaemostasislaboratorytesting,BiochemiaMedica2012;22(3):329-41表述。由於PT-INR是用於凝血測量的最常見可用的POC檢驗,可藉以確定NOAC的修改的PT檢驗或「稀釋的PT」是高度期望的。存在在此類方向的已報導的研究工作。大多數PT檢驗對於直接FXa抑制劑諸如利伐沙班(rivaroxaban)的低靈敏度是已知的。C.Kluft在EP2405274A1中公開,被某種蛇毒RVV-V影響的PT檢驗還顯示對利伐沙班的靈敏度,並公開了利用此類促凝血酶原激酶的PT檢驗的使用。發現通過一些PT檢驗(無論修改與否)確定NOAC的方式的希望,在近年已經下降。在2014年1月,T.Lindahl,瑞典的凝血的外部質量團體(coagulationoftheexternalqualityorganizationofSweden),EQUALIS的專家組成員,報告了由專家組對一種FXa抑制物質aprixaban進行的研究。結論是,許多市售可得的PT或APTT檢驗都不能用於在臨床相關濃度確定血漿中的aprixaban。另一方面,FXa檢驗針對此目的工作良好。必須提到的是,由於在用維生素K拮抗劑治療的患者的血液中發現的非功能性凝血因子pivka的可變抗凝作用而校正PT結果的努力。US7,767,459B2(J.Horsti)通過由任何給定PT方法的標準程序測量血漿的PT,和在用生理緩衝液諸如9g/lNaCl預稀釋血漿後測量血漿的PT,來提供此。隨後將表示為秒或INR的PT結果對最終血漿稀釋的程度繪圖並外推到零。血漿在零的最終稀釋的PT,減去正常血漿的,被作為pivka作用的量度,並用於校正原始PT結果。已經設想了新的凝血檢驗,目的是確定數種不同種類的抗凝劑,特別是肝素和NOAC。這些努力證明了確定這些抗凝劑的臨床重要性。參見CalatzisA,PeletzD,HaasS,SpannaglM,RudinK,WilmerM,Prothromibnase-inducedClottingTimeAssayforDeterminationoftheAnticoagulantEffectsofUFHandLMWH,Fondaparinux,andThrombinInhibitors,AmJClinPathol2008;130:446-454,和SamamaMM,MartinoliJL,LeFlemL,GuinetC,Plu-BureauG,DepasseF,Assessmentoflaboratoryassaystomeasurerivaroxaban–anoral,directfactorXainhibitor,ThrombHaemost2010;103/4:815-825。本發明的相關背景是溼化學方法和幹化學方法之間的區別。溼化學定義為在血液或血漿的凝血測定中,混合一定體積的樣品和一定體積的試劑。因此,樣品在反應混合物中被稀釋至某一程度。在幹化學中,這種稀釋不發生。將樣品與乾燥形式的試劑物質混合或接觸,且無樣品的稀釋。大多數POC檢驗是幹化學檢驗,因為它們通常可以容易使用的形式例如條帶或晶片展示。操作者通常僅需要加入小體積的樣品。幹化學方法的缺點是,檢驗更難以修改。溼化學程序賦予的一個自由度因素,樣品稀釋的程度的變化,對於幹化學不可用。每次提到「例行」檢驗的「稀釋」修改是以溼化學作為前提。概述本公開內容的目的是提供確定血液或血漿樣品中的抗凝劑的測定,所述測定包括用至少兩種溼化學凝血酶原時間(PT)方法的分析,所述測定被設計以可適用於確定血液或血漿樣品中直接和間接抗凝劑二者。本發明由所附的獨立權利要求限定。在從屬權利要求、附圖和以下描述中列出了實施方案。根據第一方面,提供了一種確定血液或血漿樣品中的抗凝劑的測定,其中所述測定包括用至少兩種溼化學凝血酶原時間(PT)方法的分析。所述測定包括以下步驟:a)在用第一PT方法的第一PT分析中,在包含在第一體積的包含促凝血酶原激酶、纖維蛋白原和凝血因子V的液體試劑中稀釋的第一體積的血液或血漿的第一反應混合物中測量PT,b)在用第二PT方法的第二PT分析中,在包含在第二體積的液體試劑中稀釋的第二體積的血液或血漿的第二反應混合物中測量PT,其中所述第二反應混合物中血液或血漿的濃度不同於所述第一反應混合物中血液或血漿的濃度。所述至少兩種PT方法被校正以當用於分析缺少該測定感興趣的抗凝劑的參考血液或血漿時給出相同或大致相同的PT結果。所述測定還包括步驟c)計算來自步驟a)和b)中的測量結果的PT差異,其中如果PT差異是1)顯著的,這指示血液或血漿樣品中抗凝劑的存在,或2)不顯著的,這指示血液或血漿樣品中不存在高於可檢測水平的抗凝劑。用至少兩種PT方法的分析在本文是指,該測定可包括用2、3、4、5或多達6種PT方法的分析。PT差異在本文是指絕對差異或相對差異。該測定中使用的至少兩種PT方法可以是基本上相同的PT方法,但具有一些可表現不顯著的差異。此類差異,除了由本發明提供的差異,即樣品體積和試劑體積之間的關係的差異以外,可以是進行測量的溫度的差異和反應混合物的離子強度或pH的差異。溼化學PT方法在本文是指Owren型PT方法。反應混合物中血液或血漿的體積與液體試劑的體積之間的比率可取決於PT試劑的特徵和樣品中待檢測的抗凝劑的濃度而大大變化。當實踐測定時,不存在血液或血漿樣品可在PT試劑中如何少和如何大範圍稀釋的嚴格限制,限制是實踐性質的。血液或血漿樣品稀釋在液體試劑中的較低水平是約1:2。在較低稀釋度,測定的一些有利的特徵可能失去,例如檸檬酸化的樣品不再是可分析的。最高的可能的稀釋度將是明顯較高的,約1:200。如此高的稀釋度可以是可能的,由於反應混合物的纖維蛋白原和FV的必需水平不必來自樣品。這是因為,Owren類型的液體PT試劑,除了促凝血酶原激酶以外,還包含有效水平的纖維蛋白原和FV。還是對於Owren類型的液體試劑,對最終樣品稀釋的程度存在實踐限制。在反應混合物中非常低水平的血液或血漿樣品下,FVII、FX和FII的水平也如此低,以至於凝血時間(PT)變得如此長,以至於檢測變得困難或不可能。因此,在實踐本發明時,血液或血漿的體積與反應混合物中液體試劑的體積之間的比率可以在1:2和1:200之間變化。優選的比率範圍可以是在1:5和1:100之間或1:10和1:50之間。在本測定中,在至少兩種反應混合物中分析PT,所述至少兩種反應混合物具有在反應混合物中不同濃度的血液或血漿。第一反應混合物中血液或血漿的濃度可以比第二反應混合物中血液或血漿的濃度高約1.5至100倍、1.5至50倍、1.5至25倍、1.5至10倍或1.5至5倍。1.5至5倍的濃度差異對於實現是實際的,並在本測定顯示允許確定在臨床相關濃度範圍中的抗凝劑。然後,第二反應混合物中血液或血漿的濃度可以比可能的第三反應混合物中血液或血漿的濃度高約1.5至100倍、1.5至50倍、1.5至25倍、1.5至10倍或1.5至5倍。儘管反應混合物中血液或血漿濃度的差異,測定的所有兩種或更多種不同PT方法被用缺少感興趣的抗凝劑的相關參考血液或血漿樣品校準,以給出相同或大致相同的PT結果。這一PT以使其可能的方式表示。以通常的時間單位表示將不可行,因為這些將在方法之間變化,並是其原樣(不能被校準)。具有低濃度的血液或血漿的反應混合物顯示長的PT:s且反之亦然。表示PT的一種普通方式是以INR(國際化標準化比率),但其他表達方式,各種合成的(synthetic)時間樣單位、或其比率,是可能的。重要的是,提供的缺少抗凝劑的相關樣品,經兩種或更多種PT方法分析,將產生儘可能接近相同的結果。比較來自一種PT方法的結果與來自另一種PT方法的結果的一個普通方式是平均PT結果和比較的CV(變異係數)。校準是使得,缺少抗凝劑的多個相關樣品的平均PT結果對於所有的兩種或更多種PT方法應儘可能接近地相同,且比較的CV應儘可能低。至少兩種PT方法可被校準,使得當用於分析來自正常個體的參考血液或血漿和此類參考血液或血漿的稀釋物時,給出相同或大致相同的PT結果。來自正常個體的參考血液或血漿在本文是指來自未經受抗凝劑處理的一個或數個表面上健康的人的血液或血漿或此類樣品的集合(pool)。至少兩種PT方法可被校準,使得當用於分析這樣的血液或血漿時給出相同或大致相同的PT結果,該血液或血漿缺少本測定感興趣的抗凝劑(來自單個或許多個體或來自不同個體的樣品的集合)且該血液或血漿通過一種或數種已建立的PT方法確定具有高於正常的PT值。在測定的步驟c)中,計算PT測量結果之間PT的絕對或相對差異。術語「顯著」和「不顯著」在本文以其常規統計學定義提供。然後,顯著差異是2倍CV或更多的相對差異,不顯著差異小於2倍CV。儘管表述不同,觀察到的差異如果在由測定確定缺少抗凝劑的樣品群體中具有低的發生概率,則是顯著的。這一概率可設置在不同水平。通常水平是5%(p<0.05)或1%(p<0.01)。如果在步驟c)中計算的PT差異是顯著的且已知抗凝劑的身份,則可計算血液或血漿樣品中抗凝劑的濃度。如果在步驟c)中計算的PT差異是不顯著的且已知抗凝劑的身份,則可指定抗凝劑不以高於其的水平存在於所述血液或血漿樣品中的水平。如果在步驟c)中計算的PT差異是顯著的,則在抗凝劑的不存在下血液或血漿樣品中估計的PT是可計算的。僅當抗凝劑的身份是已知的或推測的時,可進行血液或血漿樣品中抗凝劑濃度的計算。如果已經進行了用兩種PT方法的分析,使用PT結果的差異和來自具有最高樣品稀釋度的分析的PT結果用於這一計算可以是方便的。在最高稀釋度的PT結果將最接近無抗凝劑存在時的PT結果。利用INR形式體系,這一假想的PT結果稱為INRo。依據對抗凝劑水平的劑量響應是否是線性的,INRo可通過減去差異的分數或減去差異的函數來獲得。由於劑量響應可依賴於這一INRo和依賴於進行確定的溫度,差異的大小向抗凝劑濃度的轉化可要求許多所謂的標準曲線。可選地,多維函數可被採用來計算INRo和抗凝劑水平。如果用多於兩種PT方法的分析已被進行以實踐本發明的測定,可計算多於一種差異,且這些若干差異、和在最高樣品稀釋度獲得的PT值,可被用於計算INRo和可能的抗凝劑水平(取決於抗凝劑的身份)。偏好差異之一作為最有用的也是可能的,因為其是用於確定的有利範圍。PT測量可在17℃至45℃的範圍、優選地在18℃至30℃的範圍、更優選地在21℃至30℃的範圍,且最優選地在25℃至30℃的範圍內的環境溫度進行。低於但不遠離30℃的此類溫度區間是有利的,因為該溫度幾乎不影響PT,從而改進提供的PT分析的精確度。此外,在以下實施例中,較低的溫度增加抗凝劑的測定靈敏度。在本測定中可確定的抗凝劑是包括活化的凝血因子IIa和Xa的直接作用抑制劑的組的成員,其可選自包括達比加群(dabigatran)、apixaban、rivaroxaban或水蛭素的組,或是包括活化的凝血因子IIa和Xa的間接作用抑制劑的組的成員,其可選自包括分級的或未分級的肝素的組。第一反應混合物中液體試劑的第一體積可等於第二反應混合物中液體試劑的第二體積。在液體試劑中稀釋的血液或血漿的體積可以是在1至20μL的範圍中。可以用端對端毛細管將血液或血漿的體積加入到液體試劑。反應混合物中血液或血漿的體積與液體試劑的體積之間的比率可以是1:2至1:200、1:5至1:100或1:10至1:50。第一反應混合物中血液或血漿的濃度可以比第二反應混合物中血液或血漿的濃度高約1.5至100倍、1.5至50倍、1.5至25倍、1.5至10倍或1.5至5倍。反應混合物可包括在10至50mM的範圍、在10至30mM的範圍或在10至24mM的範圍的最終濃度的鈣離子。反應混合物中鈣的最終濃度在本文是指反應混合物中的總鈣,其主要作為游離Ca2+,但還有絡合的鈣離子。對於包含所示濃度的鈣的反應混合物,凝血抑制劑可通過測定確定的靈敏度可被增強。過度高的鈣水平應被避免,由於增加的Ca2+水平將漸進地延長凝血時間,這通常是不利的。反應混合物的克分子滲透壓濃度可以是約0.3至0.5Osm/kg、或約0.3至0.4Osm/kg。這樣的克分子滲透壓濃度水平可通過增加PT試劑中的NaCl水平以使PT試劑高滲(比血漿和其他生理溶液更高的滲透壓),因此也使得反應混合物高滲,來獲得。這樣的克分子滲透壓濃度水平可增加抗凝劑測定靈敏度。然而,如果NaCl水平過高,凝血時間可變得過度長。反應混合物中增加的克分子滲透壓濃度和增加的鈣水平的組合可增加抗凝劑測定的靈敏度以給出最有利的高靈敏度。附圖簡述圖1是顯示在正常血漿中用本測定測量的apixaban含量的圖。圖2是圖1的圖的部分的放大。圖3是顯示在正常血漿中用本測定測量的apixaban含量的圖(原始數據:PT以秒計)。圖4是圖3的圖的部分的放大。圖5是顯示在正常血液中用本測定測量的apixaban含量的圖。圖6是圖5的圖的部分的放大。圖7是顯示在正常血液中用本測定測量的達比加群含量的圖。圖8是圖7的圖的部分的放大。圖9是顯示在正常血漿中用本測定測量的肝素含量的圖。圖10是圖9的圖的部分的放大。圖11是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品時,對於5μl和20μl方法,PT20c/PT5c針對平均PTc的相對差異的圖。圖12是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品時,對於5μl和20μl方法,PT20c-PT5c針對平均PTc的絕對差異的圖。圖13是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品和來自用達比加群治療的患者的樣品時,對於5μl和20μl方法,PT20c/PT5c針對平均PTc的相對差異的圖。圖14是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品和來自用達比加群治療的患者的樣品時,對於5μl和20μl方法,PT20c-PT5c針對平均PTc的絕對差異的圖。圖15是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品和來自用達比加群治療的患者的樣品時,對於5μl和20μl方法,PT20/PT5針對平均PT的相對的未校準差異的圖。圖16是顯示,當測量來自正常個體和用華法林治療的患者的參考樣品和來自用達比加群治療的患者的樣品時,對於5μl和20μl方法,PT20c/PT5c針對平均校準的PT的相對的校準差異的圖。詳細描述提供了以下實施例,並非限制本發明的範圍,而是進一步解釋和描述本發明,和鼓勵在這一重要醫學診斷領域中的開發。實驗工作用市售可得的環境室溫凝血儀器SimpleSimonPTZafenaAB,Sweden進行,其功能在EP1636595B2中描述。對於每種PT方法使用一個儀器或讀取器(reader)。可選地,對於所有PT方法可使用相同的儀器。在實施例1至6中,對於三種PT方法即20μL方法、10μL方法和5μL方法的每一種,使用一個特定讀取器。在與實驗室的環境室溫熱平衡的實驗臺上,一起使用彼此相鄰放置的三個儀器。對於給定的PT確定,每個儀器以秒展示PT,如在表2中報告的。而且,經由每個讀取器的內部數據處理能力,展示了對於每種PT方法,樣品INR的粗略估值。這些粗略INR估值在表1、3和4中報告。由於,在每個系列的實驗中,還分析了相關參考樣品,來自每種PT方法的結果可在完成實驗系列後在單獨的辦公室臺階段(officedesksession)中校準。無論由不同PT方法的兩種或更多種確定的原始PT數據如何表示,在利用參考樣品校準後,不同的PT方法顯示儘可能接近的相同PT。在進行研究工作的實驗室中的環境室溫在21℃和26℃之間變化。低於但不遠離30℃的溫度區間是有利的,因為該溫度此後幾乎不影響PT,從而改進提供的PT分析的精確度。此外,在以下實施例中,較低溫度增加抗凝劑的測定靈敏度。然而,在17-45℃的範圍中的溫度進行測定是可能的。PT試劑是與SimpleSimonPT產品的批次N223M一起分發的PT試劑,是Owren類型的試劑,因此含有有效量的促凝血酶原激酶、纖維蛋白原和FV(兔腦來源的促凝血酶原激酶和牛血漿來源的纖維蛋白原和FV)。也可使用其他Owren類型的試劑。試劑是以200μL的份,向其加入樣品檸檬酸化的血液或檸檬酸化的血漿並混合。加入通過安裝在管狀主體一端的端對端塑料毛細管進行,該管狀主體在另一端帶有替換機械,這是為了允許方便地混合樣品和試劑。帶有10μL毛細管的此類Mixxocaps與SimpleSimonPT產品一起供應。為了進行所描述的實驗,對一些Mixxocaps安裝20μL毛細管或5μL毛細管,代替由製造商與其一起供應的10μL毛細管。可選地,可使用標準移液管或類似物混合血液或血漿樣品與液體試劑。實驗中使用的血液或血漿體積與液體試劑的體積之間的比率是1:11、1:21和1:41。可使用在1:5與1:100的範圍或在1:2與1:200的範圍中的其他比率。實驗的測定中使用的不同反應混合物之間血液或血漿濃度的差異是在1.5至5倍之間。然而,濃度的差異可以是約1.5倍至100倍。抗凝血的正常血漿是NKP產品GHI-163批次10188,MediRoxAB,Sweden。包含100mg/L的達比加群(Pradaxa,Boehringer-Ingelheim)和apixaban(Eliquis,Bristol-MeyersSquibb)的儲備溶液是DepartmentofExperimentalMedicineofUniversity的TomasLindahl教授所贈。未分級肝素是HeparinLeo批次A6888B,LeoPharmaA/S,Ballerup,Denmark。實施例1apixaban是活化的凝血因子X(FXa)的直接作用抑制劑。其是抗凝血藥物Eliquis,Bristol-MeyersSquibb的活性化合物。測量血漿中在範圍50至1000μg/L中的apixaban是臨床上感興趣的。為了製備合適的樣品,將小體積的apixaban儲備溶液加入正常血漿即對照血漿NKP,以得到apixaban含量在範圍0至1000μg/L中的正常血漿。這些具有apixaban的正常血漿,包括無攙雜的正常血漿(NKP)和在9g/LNaCl中1:2稀釋的NKP(NKP1:2),都由SimpleSimonPT來分析,該分析以在200μL試劑中20μL、10μL和5μL的樣品添加進行,從而對於三種PT方法,使用根據本發明的反應混合物中的不同樣品含量。還相關的是,根據本發明,校準了所有三種PT方法,對於無攙雜的NKP顯示INR1.000和,且對於NKP1:2顯示INR1.357。所有原始INR值,即在儀器屏幕(對於每種PT方法使用一個儀器或讀板器讀取器)顯示的結果,從而通過式A*INRexp(B)轉化為校正的/校準的INRc,其中a和b被選擇以分別為NKP和NKP1:2給出其期望值,分別為1.000和1.357。NKP1:2的INR值通過Lindahl等的對於對應50%(等於INR1.000的100%的一半)的PT活性的INR的公式計算。數據處理在表1中示出。在INR校準的列(INRc)上方存在上方數字(uppernumber)和下方數字(lowernumber),這些分別是以上提到的A和B。表1顯示了正常血漿的apixaban含量的兩種測量結果:更靈敏的量度,即PT方法提供的20μL樣品和5μL樣品的INRc的差異;和較不靈敏的量度,即10μL和5μL之間的INRc差異。INRc差異在此處顯示為絕對差異,但相對INRc差異已經可以同等良好地使用。將INRc差異對正常血漿的apixaban含量繪圖,如在圖1的圖中所示的。正方形符號是20μL方法的結果與5μL方法的結果之間的INRc差異,且圓形符號是10μL方法的結果與5μL方法的結果之間的INRc差異。指出了,在抗凝劑的不存在下估計正常血漿的INR即INRo是可能的。在以上,這以較不複雜的方式進行。從5μL樣品方法的INRo結果減去較小INRo差異的部分(56%),結果明顯最接近INRo。這些簡單的INRo估值令人驚訝地好,只有在最高apixaban含量(1000μg/L)的一個偏離多於十分之一的INR單位。圖1和2顯示圖,其中apixaban含量的測量值的增加速率隨著含量增加。然而,對於領會/偏好線性劑量響應關係的那些許多,此類關係在本文由低1個INR單位的apixaban測量值展示,如在圖2的圖中觀察到的,其中圖2顯示圖1的圖的部分的放大。圖1和2顯示的數據處理對於不熟悉INR的環境室溫確定的人們可能是令人困惑的。代替已經由儀器/讀取器的計算針對溫度效應校正的原始INR結果,我們可以改為考慮以秒計的PT。進行此以增加描述本發明的清楚性,儘管由於在進行測定的時間段期間不嚴格恆定的溫度(溫度從22.3℃到24.2℃變化)引入誤差。儘管存在這一偏差,結果仍然是足夠好以令人信服的,並更清楚地解釋,因為其允許本領域技術人員熟悉的數據處理,即,通過將PT(以秒計)除以正常PT,和用等價於ISI的歸一化常數對比率加權來計算INR。在表2中,顯示了對具有加入的apixaban的正常血漿(NKP)進行的測定的結果,但原始數據在此處是以按秒計的PT計的,且數據通過除以正常血漿的PT並將比率經受ISI的加權來轉化為INRc,上方數字和下方數字分別在INRc列的上方顯示。由於視為相關,上方數字被選擇以使NKP1:2顯示INRc1.357。在表2中,數據被從頂部的22.3℃到底部的24.2℃運行的溫度梯度偏置。然而,這幾乎不幹擾總的圖。使用的PT方法即環境溫度Owrens方法,對抑制劑比其他更靈敏,仍然明顯的是,單個選擇的PT方法在較低水平的apixaban將不會提供較有用的信息。表2假設你利用三種方法中對apixaban最靈敏的方法,具有20μL樣品的方法,且你獲得35.2秒的PT。這比正常血漿(NKP)的32.8秒要多,但PT的增加是否是由於抗凝劑,或是由於凝血因子的低含量(NKP1:2的PT是36.9秒)?你如何判斷?測定的實踐,用在反應混合物中具有不同樣品含量的PT方法進行兩種或更多種PT確定的測定實踐,提供了更清楚的描繪。由於被校準以顯示相同PT(在本文相同的INR稱為INRc,c代表校準的)的方法對於缺少待確定的抗凝劑的樣品是不同的,在具有低凝血因子含量的樣品的INRc結果之間將存在較少差異或無差異,即無顯著差異。在本實施例中,已知樣品包含抗凝劑apixaban,因為其已被加入,且出現INRc結果的差異。在本實施例中存在根據本發明使用的三種PT方法,且在INRc結果中存在可被檢查的三種差異(三種中的兩種在表2中顯示),且對於具有50μg/Lapixaban的正常血漿的測定,所有三種差異指示抗凝劑的存在。如果抗凝劑的身份是已知的,其含量可被估計。INRc差異在此處顯示為絕對差異,但相對INRc差異已經可以同等良好地使用。還可估計在抑制劑的不存在下樣品的預計INRc即INRo。表2顯示以秒計的PT,澄清了實踐本發明的實用性。預計表2中顯示的結果與表1中的那些接近相同,且它們相當良好地一致。對具有最高apixaban含量的樣品注意到的差異歸咎於溫度效應。當進行實驗系列時,溫度升高約2℃。在報告表1中顯示的INR值之前,儀器已經補償了這一溫度轉變的效應。當然,表2中顯示的PT值(以秒計的凝血時間)未對這一溫度效應校正(以秒計的PT是其原樣)。因此在表1和表2中顯示INR的小差異。在圖3和4的圖中,已經插入了來自表2的數據。將INRc差異對正常血漿的apixaban含量繪圖(由PT方法提供的20μL樣品與5μL樣品之間的INRc差異(方形)、和10μL與5μL之間的INRc差異(點))。圖4中的圖是圖3的圖的部分的放大。實施例2將在0至1000μg/L的範圍中的apixaban加入到正常的檸檬酸化的血液。這些血液樣品和具有INR2.3的血液樣品由SimpleSimonPT利用200μL試劑中20μL、10μL和5μL的樣品體積分析。INR的原始結果和在相關校準後的INRc在表3中展示。0,870,931,010,961,101,151,5apixabanINRINRINRINRcINRcINRcΔINRcΔINRcμg/L20μL血液10μL血液5μL血液20μL血液10μL血液5μL血液20μL-5μL10μL-5μLINRo10008,763,502,216,943,692,514,431,180,747146,062,781,874,882,862,082,800,780,915004,582,271,663,732,291,811,920,481,092502,611,641,322,181,601,390,790,211,071251,751,321,131,491,261,160,320,101,02631,411,191,041,211,121,060,150,060,9601,161,060,001,001,001,000,00-0,01N-血液0,371,161,060,991,001,001,000,00-0,01C-血液2,32,762,272,052,302,302,300,000,00表3在這裡對所有三種PT方法進行了判定,無apixaban添加的正常血液顯示INRc1.00,且由中心醫院實驗室報告顯示INR2.3的檸檬酸化血液在這裡顯示INRc2.30。如在前面的實施例中的,INRc結果的絕對差異(可選地可使用相對差異)被視為抗凝劑含量(這裡是apixaban含量)的量度,並就三種可能的此類差異的兩種對已知的apixaban含量繪圖和展示在圖5和6中。PT方法提供的20μL樣品與5μL樣品之間的INRc差異顯示為方形,且10μL與5μL之間的INRc差異顯示為點。圖6中的圖是圖5的圖的部分的放大。本發明的抗凝劑方法的劑量響應顯示血液中臨床上感興趣的apixaban的範圍內的良好陽性劑量響應特徵。劑量響應對於小於1的INRc差異也是線性的,參見圖6。實施例3達比加群是當含達比加群酯(dabigatran-etexilate)的藥物製劑Pradaxa,Boehringer-Ingelheim經口,即口服,施用時,體內形成的活性化合物。感興趣的臨床水平範圍從血漿中50至1000μg/L。此類樣品通過向正常血漿NKP加入小體積的達比加群儲備溶液來產生。結果和數據處理與實施例1的相似,顯示在表4中。表4比較表4與實施例1中的表1時,表現為,本發明展示的實施方案對於血漿中的達比加群不如對於apixaban靈敏。當比較圖7和8中的圖與實施例1的相應圖時,這一印象被加強。圖(參見圖8,圖7中的圖的部分的放大)的線性部分中更靈敏的INRc差異(20μL減5μL,在圖7和8中顯示為方形)在約200μg/L達比加群達到0.5,而在約80μg/Lapixaban達到相同數目,參見圖2,即,多於兩倍的靈敏度差異。而且,50μg/L達比加群的達比加群水平表現為可檢測的。不令人驚訝地,確定抗凝劑的測定對不同抗凝劑顯示不同的靈敏度。此外,以不同試劑和進行PT分析的不同溫度預計不同的靈敏度。實施例4肝素是一種抗凝劑,其難以在護理場所諸如在外科病房可靠地確定。需要更方便的方法。在這方面,本測定確定抗凝劑的實用性在以下示例。本實施例是用未分級的肝素,其通常在大量外科手術中用作抗凝血劑。樣品通過向正常血漿NKP加入小體積的肝素儲備溶液來製備。在選擇的校準中,分別對NKP和NKP1∶2分配INR1.000和INR1.357,這與以上實施例1和3中選擇的相關校準相同。實驗細節與實施例1和3相同,且結果和數據處理在表5顯示。0,950,940,961,321,120,98NKPINRcINRcINRcΔINRcΔINRc0,43肝素U/ml20μL樣品10μL樣品5μL樣品20μL樣品10μL樣品5μL樣品20μL-5μL10μL-5μLINRo56,472,101,3511,172,161,299,880,870,912,52,461,401,133,121,371,082,040,290,961,21,471,191,111,581,141,060,520,081,030,61,261,121,081,291,061,030,260,031,0201,041,061,051,001,001,000,000,001,00NKP1,041,061,051,001,001,00NKP1∶21,311,391,431,361,361,36表5將正常血漿中抗凝劑含量的量度即可能的三種差異的兩種的INRc的絕對差異(可選地可使用相對差異)對肝素含量繪圖,得到圖9和10中的圖。如從表5和圖9和10觀察到的,肝素可在約0.2U/mL被檢測到和在濃度範圍0.2至5U/mL中確定,這是臨床相關的。實施例5根據本抗凝劑測定,兩種或更多種PT方法(其中一種在反應混合物中具有比另一種更大比例的樣品)被校準以對缺少感興趣的抗凝劑(即,缺少可被本測定確定的抗凝劑)的參考樣品顯示儘可能接近相同的PT。在定義上,參考樣品的PT是已知的,其作為一組參考樣品的平均值或是單獨的。在本實施例中參考樣品有兩種;來自正常個體的血漿樣品(n=34)和來自用華法林治療的患者的血漿樣品(n=30)。參考樣品的PT是由在UniversityHospitalofSweden的中心實驗室進行的參考分析已知的。正常個體和華法林患者的平均參考PT分別是23.1和51.5秒。本抗凝劑測定的兩個PT方法,一個是20μL樣品加入到200μLPT試劑(反應混合物中較高比例的樣品),另一個是5μL樣品加入到200μL相同試劑(反應混合物中較低比例的樣品)。這兩種方法對於正常個體和華法林患者的參考樣品分別顯示32.8和65.3秒、以及41.8和104.3秒的平均PT。兩種PT方法即20μL方法和5μL方法然後被校準以顯示相同的平均PT(以合成的(synthetic)秒計),作為用於兩組參考樣品的參考方法。這通過常數A20和B20、以及A5和B5,由表達式PTc=A*PTexpB分別將20μL方法和5μL方法的PT轉化為校準的PT值(PTc)來實現。計算兩種方法對每種樣品的PTc的差異,表示為比率(PT20c/PT5c)或以絕對方式(PT20c減PT5c),並將其對兩種方法的平均PTc繪圖,參見圖11和12。患者組(圖中標為X)中兩份參考樣品顯示統計學上在由其他參考樣品(方形)定義的差異的正常分布之外的差異。這些偏離的樣品可包含抗凝劑肝素,肝素是可被本抗凝劑測定確定的抗凝劑(參見實施例4),且其在華法林治療無效時被用於治療一些住院華法林患者。使用在測定的兩種PT方法的校準的PT結果之間的相對差異(圖11)或絕對差異(圖12)是一種選擇。這裡,表示為比率的相對差異由於標準偏差在正常的PT範圍中與升高的PT範圍中大致相同,分別是0.054和0.044,展示了益處,。懷疑含有肝素的患者樣品的PTc比率展示與平均值的陽性偏差為由其他28份患者樣品定義的標準偏差的3.0和4.5倍。在統計學上,這兩個偏離值不太可能是由其他患者樣品定義的PTc比率的分布的部分,p<0.05。用於分析正常個體的34份參考血漿和華法林患者的30份參考血漿的相同實驗設置也用於分析來自正在經歷達比加群(一種抑制凝血酶的NOAC)或將要開始此類治療的患者的血漿樣品(n=13)。13份患者血漿樣品來自DepartmentofAcuteInternalMedicineoftheUniversityHospitalofSweden。將表示為比率或絕對數目的患者血漿(標為X)的PT20c和PT5c的差異,引入參考樣品(標為方形)的圖中,如在圖13和14中分別觀察到的。3個NOAC患者顯示的PTc差異升高在由參考樣品定義的正常分布以外。根據確定達比加群的已建立的方法,即稀釋的凝血酶時間(dTT)方法,顯示升高的PTc差異的三份樣品分別含有172、224和350μg/L達比加群。來自NOAC患者的其他10份血漿樣品,都未顯示升高的PTc差異,根據dTT方法都包含<30μg/L達比加群。有趣的是,在13份達比加群患者樣品中有數份樣品以20μL方法和5μL方法顯示升高的PTc值,但方法之間無顯著差異。該發現與華法林治療的作用而不是達比加群治療的作用一致。因此,公開的抗凝劑測定能夠進行區分。因此,該測定能夠估計樣品的PT和NOAC(抗凝劑)含量二者。樣品對達比加群的不包含,即<30μg/L,由不顯著的PTc差異展示。這一發現由用於達比加群確定的已建立方法(dTT)證實。根據dTT確定,通過本測定13份樣品中具有不顯著的PTc差異的的所有10份,包含<30μg/L。在實踐抗凝劑測定時,兩種PT方法(一種具有反應混合物中高樣品含量和一種具有反應混合物中低樣品含量)被校準以數字上顯示PT的參考水平。此處,在本實施例中,測定的兩種方法的PT結果被校準以顯示所謂的合成時間,不是實際的秒,而是反映參考方法的以秒計的PT的數值。如果參考樣品的PT以INR表示,則本發明的方法被校準以提供與這些參考樣品儘可能地接近的相同INR。如果參考樣品的參考PT以正常PT的百分比表示,則這些值被用在校準中。實施例6如以上實施例5中的,本抗凝劑測定的兩種或更多種PT方法(一個具有比另一個高的反應混合物中樣品含量),都被校準以顯示兩組參考樣品的參考PT結果;34份血漿來自正常個體且30份血漿來自華法林治療的患者。所有參考PT值由UniversityHospitalofSweden的中心實驗室確定。如在實施例5A中的,兩種PT方法,一種是20μL樣品加入到200μLPT試劑,另一種是5μL樣品加入到相同PT試劑。未校準的PT結果稱為PT20和PT5,且校準的PT結果分別稱為PT20c和PT5c。還由該兩種PT方法分析了來自在DepartmentofAcuteInternalMedicineoftheUniversityHospitalofSweden的達比加群治療的患者的血漿樣品(n=20)。根據也在實施例5中提到的已建立的dTT方法,所有20份血漿樣品具有高於34μg/L的達比加群水平。在圖15和16中,分別在校準之前和之後,將測定的兩種PT結果之間的差異(以比率表示)對兩種PT結果的平均值繪圖。在圖中,方形顯示參考樣品的結果,且X顯示NOAC(達比加群)樣品的結果。校準前,圖15,正常參考樣品顯示約35秒的平均PT,且華法林患者參考樣品顯示範圍從約65至110秒的平均PT。校準後,圖16,正常參考樣品的平均PT(平均PTc)是23.1–不是實際的秒而是合成的–且華法林患者參考樣品的平均PTc範圍從約40至70。校準後,當然,這些平均值和範圍與通過參考方法獲得的那些非常接近相同,即,它們反映參考值。在比較圖15和圖16時,明顯的是,校準導致本抗凝劑測定的決定性的改進。直接統計分析顯示,約80%的臨床達比加群樣品(參見圖16)具有可檢測水平的抗凝劑(PTc比率高於正常參考樣品的平均值加2*SD)。在校準之前,這是僅70%,參見圖15。如果未進行校準,需要設想更複雜、較不直覺的統計分析。校準後,達比加群樣品顯示範圍更寬、更適合定量NOAC確定的PT差異(PTc差異)。並非最不重要的是測定的邏輯,如由操作者構思的。校準後,反應混合物中較高比例樣品的一種PT方法將對具有抗凝劑的樣品顯示比利用較低比例樣品的PT方法更高的PT值-如果樣品中不存在可檢測水平的抗凝劑,兩種PT方法當然將顯示大致相同。如果沒有校準,沒有如此直接的邏輯。抗凝劑測定的兩種PT方法可被校準以顯示參考樣品的參考值,無論參考值被如何表示。參考值可(如在本實施例中的)以PT(秒)表示,或它們可以INR表示或表示為正常活性的分數。在所有情形中,校準是可能和有利的。實施例7實施例5和6顯示增加使用的抗凝劑測定的靈敏度的需要,因為僅約80%的具有高於30μg/L(根據已建立的達比加群方法(dTT))的達比加群水平的臨床樣品展示高於測定的檢測限值的抗凝劑水平,參見圖16(注意,檢測限值實際上是沿著1.1的水平線)。本實施例描述目的是改進測定的靈敏度而進行的實驗。表6展示來自其中PT液體試劑(批次P161)包含4、8、16或32mM的各種水平的加入的CaCl2的實驗的數據。對於每一種試劑,由抗凝劑測定的兩種PT方法即20μL方法和5μL方法分析三種樣品。兩種樣品是參考樣品即對照血漿NKP和ZAP,分別具有1.00和2.50的已建立的INR值。第三種樣品是已向其加入小體積的apixaban儲備溶液以得到500μg/L的apixaban濃度的NKP。然後校準每種試劑的結果以對NKP顯示1.00的INRc和對ZAP顯示2.50的INRc。帶有500μg/Lapixaban的NKP(NKP+500)然後顯示多種INR20c和INR5c結果。針對每種試劑計算表示為比率INR20c/INR5c的差異,並展示在表6中右邊第二列中。為了獲得靈敏度的量度,從對NKP+500樣品觀察的比率INR20c/INR5c估計檢測限值。這一估計在以下假設下進行i)對於所有試劑,正常參考血漿的比率的SD是0.052(這一值從實施例6中的數據獲得,和ii)比率減一與成比例地從零增加達比加群水平。在這些假設下,對每種試劑的檢測限值計算為比率達到一加0.104(2*SD)時的達比加群水平。計算的檢測限值在表6的最右列中展示。最高檢測限值(最低靈敏度)是約94μg/L,以包含4mMCaCl2的試劑獲得。對於包含8mMCaCl2的試劑,靈敏度更高且檢測限值是約70μg/L,且對於包含16mMCaCl2的試劑,靈敏度又更高且檢測限值是38μg/L。更高的試劑CaCl2含量(24和32mM)不進一步增加靈敏度和檢測限值,保持在與試劑中16mMCaCl2大致相同的水平。表6表6顯示,PT試劑中範圍為約10至50mM的離子化的鈣的含量導致本抗凝劑測定的增加的靈敏度。這表現為降低的檢測限值。由於試劑僅被樣品的加入少量地稀釋,反應混合物中離子化鈣的水平與PT試劑中的大致相同(20μL方法中稀釋約10%,且5μL方法中稀釋約3%)。結果是令人驚訝和出乎意料的,因為離子化鈣的水平在標準PT方法的反應混合物中通常是約8mM。這一水平通常通過加入可溶的鈣鹽CaCl2到PT試劑來達到,但其他鈣離子來源是可能的,包括氫氧化鈣、乳酸鈣和其他包含非幹擾性陰離子的可溶的鈣鹽。甚至加入金屬鈣是可能的,儘管較不實際。PT反應混合物中離子化鈣濃度的增加導致達到凝血點所需的時間即凝血時間的逐步增加。對於5μL方法和NKP樣品(INR1.00),對於反應混合物中約4、8、16、24和32mM的鈣離子濃度,凝血時間分別是42.1、47.4、52.5、70.1和82.1秒。高於測定靈敏度的有利增加所需水平的離子化鈣水平的增加,由於增加凝血時間被認為是不利的。因此,優選的離子化鈣離子濃度水平在10和30mM之間的範圍中,或甚至在10和24mM之間的範圍中。在凝血反應中,離子化的鎂通常可代替離子化鈣的功能。在此處也可以如此。因此,陳述的離子化鈣水平的限值可視為離子化鈣水平和離子化鎂水平的總和的限值。在目的是增加抗凝劑測定的靈敏度的另外的實驗中,增加PT試劑中的NaCl水平以使PT試劑高滲(比血漿和其他生理溶液更高的滲透壓),因此也使得反應混合物高滲。這增加抗凝劑測定的靈敏度。抗凝劑測定靈敏度被增加的克分子滲透壓濃度的增加也在範圍上受限,因為如果NaCl水平過高,凝血時間可變的過度長。在實踐中,為了增加抗凝劑測定的靈敏度,反應混合物的克分子滲透壓濃度可被增加到0.3至0.5Osm/kg的範圍,或可甚至更限於0.3至0.4Osm/kg的範圍。通常,PT方法的反應混合物的克分子滲透壓濃度非常接近生理0.308Osm/kg,這與0.154MNaCl溶液相同。可設想的是,增加抗凝劑測定的靈敏度的以上描述的措施的組合可被組合以提供最有利的高靈敏度。反應混合物可通過加入NaCl到0.3至0.4Osm/kg之間的範圍並具有在範圍12至30mM的離子化鈣水平來變得高滲。當前第1頁1 2 3 
